1 . 下列说法正确的是
A.基态某原子的价层电子排布式为 ,推断该元素位于第五周期第IA族 ,推断该元素位于第五周期第IA族 |
B. (硒)的电负性依次减小 (硒)的电负性依次减小 |
C.C、N、O三种元素第一电离能从大到小的顺序是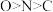 |
D.硼原子核外电子由 ,原子放出能量 ,原子放出能量 |
您最近半年使用:0次
名校
2 . 下列说法中不正确的是
| A.同一基态原子中,4px、4py、4pz轨道上电子的能量相同 |
| B.s-s轨道可以形成的σ键,s-p轨道也可以形成的σ键, |
| C.某原子价电子排布式是6s26p2,则该元素位于元素周期表的p区 |
| D.CH4中4个C-H键的键长、键能不完全相同 |
您最近半年使用:0次
解题方法
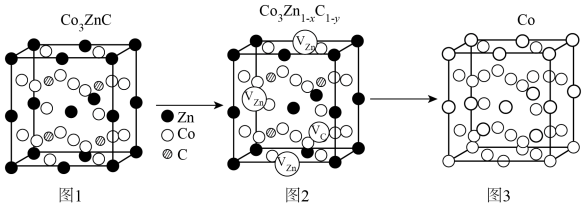
3 . 某课题组用过渡金属碳化物(Co3ZnC)合成了具有催化活性位点的钴单质催化剂。下列叙述错误的是
②NA代表阿伏加德罗常数的值,Co晶胞的底边长和高均为2apm,宽为apm。
②NA代表阿伏加德罗常数的值,Co晶胞的底边长和高均为2apm,宽为apm。
| A.1个Co3ZnC晶胞中含5个原子 |
| B.上述晶胞涉及的元素位于周期表3个区 |
C.1个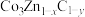 晶胞的质量为 晶胞的质量为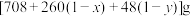 |
D.钴晶体的密度为 |
您最近半年使用:0次
名校
4 . 钨(W)常用于制造白炽灯、碘钨灯等。工业上以黑钨矿(主要成分是 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。
请回答下列问题:
(1)基态 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是__________ ;Mn位于元素周期表__________ 区。
(2)“粉碎”的目的是__________ ;从“浸取”得到的浸渣中分离出 的操作方法是
的操作方法是__________ 、过滤、洗涤、干燥。
(3)根据“转化”,判断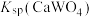
__________ 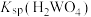 (填“>”或“<”)。
(填“>”或“<”)。
(4)“灼烧”中盛装固体的仪器是__________ (填名称);发生反应的化学方程式为______________________________ 。
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm, 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为__________  (列出计算式即可)。
(列出计算式即可)。
 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。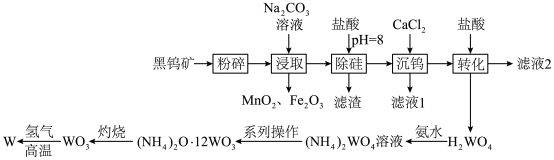
请回答下列问题:
(1)基态
 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是(2)“粉碎”的目的是
 的操作方法是
的操作方法是(3)根据“转化”,判断
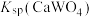
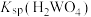 (填“>”或“<”)。
(填“>”或“<”)。(4)“灼烧”中盛装固体的仪器是
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm,
 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为 (列出计算式即可)。
(列出计算式即可)。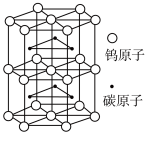
您最近半年使用:0次
昨日更新
|
42次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
5 . 下列有关原子结构和元素周期律表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为22的元素位于元素周期表的第四周期ⅡA族
⑤同周期相邻主族元素的原子序数之差不一定为1
⑥同一元素的各种同位素的物理性质、化学性质均相同
⑦金属元素原子的最外层电子数一定≤4
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为22的元素位于元素周期表的第四周期ⅡA族
⑤同周期相邻主族元素的原子序数之差不一定为1
⑥同一元素的各种同位素的物理性质、化学性质均相同
⑦金属元素原子的最外层电子数一定≤4
| A.②⑤ | B.①②④ | C.②⑤⑦ | D.③④⑤⑥⑦ |
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
| A.某短周期元素最外层有2个电子,则其一定是金属元素 |
| B.主族元素的单原子阳离子一定具有稀有气体的电子层结构(H+除外) |
| C.元素周期表有7个主族、8个副族,副族均由长周期元素组成 |
| D.主族元素在周期表中的位置只取决于该元素的电子层数 |
您最近半年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素,回答下列问题:___________ 。
(2)上表短周期元素中,金属性最强的是___________ (填元素名称);最高价氧化物对应水化物中酸性最强的物质___________ (填化学式,下同);简单气态氢化物最稳定的是___________ 。
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是___________ (用离子符号表示)。
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为___________ 。

(2)上表短周期元素中,金属性最强的是
(3)表中E、F、G三元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小顺序是
(4)H是目前人类使用最广泛的金属元素。B的最高价含氧酸稀溶液与足量H单质发生反应生成BO的离子方程式为
您最近半年使用:0次
名校
8 . 几种短周期元素的原子半径及主要化合价见下表,分析判断下列说法正确的是
| 元素符号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4,-4 | -1 | +5,-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.064 | 0.066 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A.A单质能从B的简单氢化物中置换出B单质 |
| B.A、H、J的离子半径由大到小的顺序是H>J>A |
| C.某溶液焰色反应呈黄色,则该溶液的溶质一定为J的最高价氧化物的水化物 |
| D.I在DB2中燃烧生成两种化合物 |
您最近半年使用:0次
9 . 化学与生活息息相关。下列叙述错误的是
| A.加入助剂后的聚氯乙烯可以制成雨衣、桌布等产品 |
| B.基于界面效应的新型开关中含有的碲元素和钛元素都是过渡元素 |
| C.高吸水性树脂可在干旱地区用于农业、林业上抗旱保水,改良土壤 |
| D.在规定的范围内合理使用食品添加剂,对人体健康不会产生不良影响 |
您最近半年使用:0次
解题方法
10 . 下列说法正确的是
| A.碱金属和碱土金属元素均位于元素周期表的p区 |
B.NaCl中化学键的离子键百分数比 中的低 中的低 |
C. 中存在 中存在 与 与 之间的强烈相互作用 之间的强烈相互作用 |
D. 中 中 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近半年使用:0次



