下列说法正确的是
A.基态某原子的价层电子排布式为 ,推断该元素位于第五周期第IA族 ,推断该元素位于第五周期第IA族 |
B. (硒)的电负性依次减小 (硒)的电负性依次减小 |
C.C、N、O三种元素第一电离能从大到小的顺序是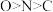 |
D.硼原子核外电子由 ,原子放出能量 ,原子放出能量 |
更新时间:2024-05-11 20:53:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W为短周期元素,X原子的质子数等于Z与Y的质子数之和;Z与Y位于同一周期;Y2常用做保护气,一般由分馏液态空气得到;非金属Z的一种固体单质可导电;W原子半径是短周期元素中最大的。下列说法正确的是
| A.四种元素中简单离子半径由大到小的顺序W、X、Y、Z |
| B.X、Z、W的最高价氧化物的水化物可两两发生反应 |
| C.氢化物沸点最高的是Z的氢化物 |
| D.随着温度升高,Y2的化学活性增强,可能与W单质发生化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z是
| A.Mg 、Al 、Si | B.Li 、Be、 Mg | C.N 、O 、S | D.P、 S、 O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一种钴的配合物乙二胺四乙酸合钴的结构为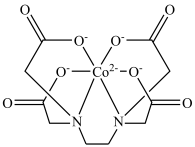 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A. 的价电子排布式为 的价电子排布式为 | B.碳原子的杂化轨道类型为 和 和 |
C.该配合物中配位原子是 和 和 | D. 该配合物形成的配位键有 该配合物形成的配位键有 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是原子序数依次增大的4种短周期元素,X、Y、Z位于同一周期,XZ3与YW3之间能以配位键相结合,XY的熔点高、硬度大,下列说法不正确的是
| A.XZ3与YW3的空间结构一样 |
| B.Z的氢化物的稳定性比Y的氢化物的稳定性强 |
| C.Y与W可形成既含极性键又含非极性键的化合物 |
D. XZ3中X原子杂化前,处于激发态的X原子的价电子轨道表示式为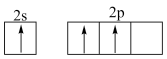 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据如图所示,下列说法正确的是
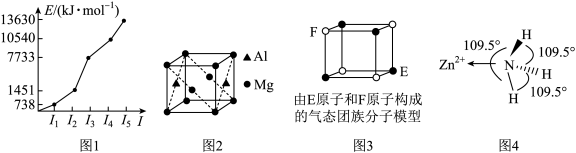

| A.第三周期某元素的前5个电子的电离能如图1所示,该元素是Al |
| B.铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有12个镁原子最近且等距离 |
| C.某气态团簇分子结构如图3所示,该气态团簇分子的分子式为EF或FE |
D.图4所示是 的部分结构,其中H-N-H键的键角比 的部分结构,其中H-N-H键的键角比 的键角大,与 的键角大,与 中N原子的孤电子对在该配离子中转化为成键电子对有关 中N原子的孤电子对在该配离子中转化为成键电子对有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、M的原子序数依次增大,Z的基态原子的2p轨道半充满,M的最高正价与最低负价的绝对值之差为4,由这4种元素组成的一种分子的结构如图所示。下列说法正确的是
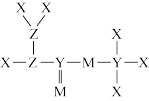

A.电负性: |
B.简单气态氢化物的热稳定性: |
C.第一电离能: |
| D.X与Z、M形成的化合物中,一定不含离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】元素F、Cl、Br、I位于周期表VIIA族。下列事实不能通过比较元素电负性解释的是
| A.F-F键的键能小于Cl-Cl键的键能 |
| B.CF3I与水发生反应的产物是CF3H和HIO |
| C.AlF3属于离子化合物,AlCl3属于共价化合物 |
| D.气态氟化氢中存在(HF)2,而气态氯化氢中是HCl分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对下列事实的解释错误的是
选项 | 事实 | 解释 |
A |  的沸点较低 的沸点较低 |  存在分子内氢键 存在分子内氢键 |
B |  可发生反应: 可发生反应: |  中N的一个 中N的一个 杂化轨道上有未成对电子,易两分子 杂化轨道上有未成对电子,易两分子 结合形成 结合形成 键 键 |
C |  与 与 加成的主要产物是 加成的主要产物是 |  中 中 的电负性较大,使双键电子云向中心碳原子偏移; 的电负性较大,使双键电子云向中心碳原子偏移; 中带正电性的 中带正电性的 易连在带负电性中心碳原子上 易连在带负电性中心碳原子上 |
D | 利用“杯酚”可分离 和 和 | 超分子具有自组装的特征 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 、
、 、
、 、
、 是原子序数依次增大的短周期主族元素,基态
是原子序数依次增大的短周期主族元素,基态 个能级中容纳的电子数之比为
个能级中容纳的电子数之比为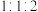 ,基态
,基态 个未成对电子,且
个未成对电子,且 所示,
所示,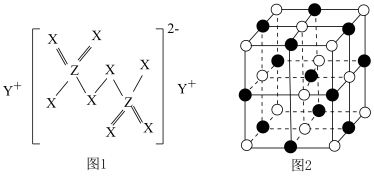

 个
个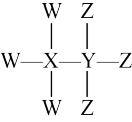
 和
和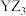 均为极性分子
均为极性分子

