17. 某兴趣小组探究镁跟碱性银氨溶液反应。实验步骤及现象如下。
Ⅰ.将
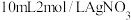
溶液和10mL6mol/L的氨水在锥形瓶中混合,测得pH=12。
Ⅱ.加入1g去掉氧化层的镁条,十几秒后有许多气泡生成,用集气瓶排水集气,气体体积先增大后减小然后不变。同时锥形瓶中有灰白色沉淀生成。
Ⅲ.取出镁条过滤洗涤得到灰白色固体。
Ⅳ.取少量灰白色固体于试管中加入稀

,沉淀全部溶解,并有无色的气体生成,且在试管口部气体变成红棕色,将其溶解后的溶液加入稀盐酸,产生大量白色沉淀。
回答下列问题:
(1)步骤Ⅱ产生不溶于水的气体是
________,易溶于水的气体是
________,该气体使湿润的红色石蕊试纸变蓝色,生成该气体的反应的离子方程式为:
________。
(2)步骤Ⅳ的现象证明灰白色固体一定含有
________。证明灰白色固体中有

,需要的试剂有稀盐酸和
________。
(3)向水中加入1g去掉氧化层的镁条,几乎看不见气泡产生。镁跟碱性银氨溶液反应能迅速产生气泡的原因:
________。
(4)向pH相同的氢氧化钠溶液中加入1g去掉氧化层的镁条,看不见气泡产生,其原因是:
________。