名校
解题方法
1 . 第二主族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
| A.Mg | B.Ca | C.Be | D.Ba |
您最近一年使用:0次
2020-03-06更新
|
240次组卷
|
2卷引用:四川省南充市阆中中学2020届高三化学选择题专项训练(15)
19-20高二·浙江·期末
解题方法
2 . 某同学设计如下元素周期表,以下说法正确的是( )
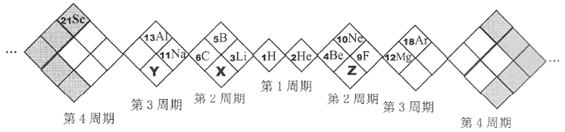

| A.白格中都是主族元素,灰格中都是副族元素 |
| B.原子半径:Z>X>Y |
| C.Z的最高价含氧酸是强酸 |
| D.X、Y、Z的气态氢化物中最稳定的是Z的氢化物 |
您最近一年使用:0次
3 . 如图是部分短周期元素化合价与原子序数的关系图
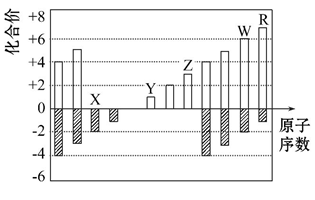
请回答下列问题(用元素符号表达):
(1) X、Y、Z 三种元素的原子半径大小顺序是____________
(2)X 与 Y 形成化合物Y2X2,写出该化合物的电子式____________
(3)RX2是一种强氧化性气体,可用于污水处理,能将 CN-氧化,生成两种无毒气体,该反应离子方程式为____________
(4)某阴离子 Wa2-(a 为2 − 6之间的数字)在碱性溶液中被 BrO3‾离子氧化为 WO42-,而BrO3-离子被还原为Br-,反应中消耗的 BrO3-离子和 OH ‾离子的物质的量之比为 2:3,则 a =____________ 。

请回答下列问题(用元素符号表达):
(1) X、Y、Z 三种元素的原子半径大小顺序是
(2)X 与 Y 形成化合物Y2X2,写出该化合物的电子式
(3)RX2是一种强氧化性气体,可用于污水处理,能将 CN-氧化,生成两种无毒气体,该反应离子方程式为
(4)某阴离子 Wa2-(a 为2 − 6之间的数字)在碱性溶液中被 BrO3‾离子氧化为 WO42-,而BrO3-离子被还原为Br-,反应中消耗的 BrO3-离子和 OH ‾离子的物质的量之比为 2:3,则 a =
您最近一年使用:0次
4 . 碳及其化合物在生产、生活中有广泛的用途。
I.金刚砂SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为____________ ,R的电子式为______________ ;
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为_____________ ,除去粗产品中少量钠的试剂为______________ ;
(3)碳还原制取SiC,其粗产品中杂质为Si和SiO2。先将20.0g SiC粗产品加入到过量NaOH溶液中充分反应,收集到0.1 mol氢气,过滤SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为____________________ ,硅酸盐的物质的量浓度为____________ 。
II.工业上向氨化的CaSO4悬浊液中通入适量CO2,可制取(NH4)2SO4,其流程如图所示。已知CaSO4的KSP=9.1×10-4,CaCO3的KSP=2.8×10-4。请回答:
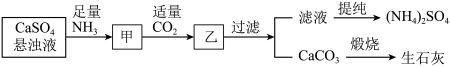
(1)向甲中通入过量CO2__________ (填“有”或“不”)利于CaCO3和(NH4)2SO4的生成,原因是_________________ 。
(2)直接蒸干滤液得到的(NH4)2SO4主要含有的杂质是____________ (填含量最多的一种)。
(3)锅炉水垢中含有的CaSO4,可先用Na2CO3溶液浸泡,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为___________________________ ;
②请分析CaSO4转化为CaCO3的原理:___________________________ 。
I.金刚砂SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为
(3)碳还原制取SiC,其粗产品中杂质为Si和SiO2。先将20.0g SiC粗产品加入到过量NaOH溶液中充分反应,收集到0.1 mol氢气,过滤SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为
II.工业上向氨化的CaSO4悬浊液中通入适量CO2,可制取(NH4)2SO4,其流程如图所示。已知CaSO4的KSP=9.1×10-4,CaCO3的KSP=2.8×10-4。请回答:

(1)向甲中通入过量CO2
(2)直接蒸干滤液得到的(NH4)2SO4主要含有的杂质是
(3)锅炉水垢中含有的CaSO4,可先用Na2CO3溶液浸泡,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为
②请分析CaSO4转化为CaCO3的原理:
您最近一年使用:0次
名校
解题方法
5 . 有X、Y、Z、W四种短周期主族元素,它们在周期表中的位置如图所示,已知Y是地壳中含量最高的金属元素,则下列说法中正确的是( )
| X | |||
| Y | Z | W |
| A.简单离子半径:Y>W |
| B.Y的最高价氧化物的水化物和X的最高价氧化物的水化物可反应 |
| C.X的简单氢化物比Z的简单氢化物更稳定、沸点更高 |
| D.非金属性:W>X |
您最近一年使用:0次
2019-12-31更新
|
556次组卷
|
3卷引用:华南师范大学附中2020届高三上学期第三次月考理综化学试题
18-19高三·浙江·期中
6 . 下图是元素周期表的一部分。
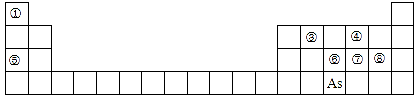
Ⅰ.(1)④、⑤、⑧的离子半径由大到小的顺序为_________ (用离子符号表示)。
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。(用化学式表示)
(3) 由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂,
由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂, 可与
可与 的水溶液反应,产物有
的水溶液反应,产物有 的最高价含氧酸,该反应的化学方程式为
的最高价含氧酸,该反应的化学方程式为_______________ 。
Ⅱ.以下框图中的物质均为中学中常见的化合物或单质(部分产物略去),已知化合物 为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
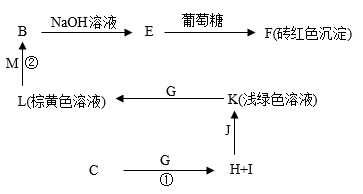
(1)化合物 的电子式为
的电子式为______________ , 的化学式为
的化学式为____________ 。
(2)写出反应①和反应②的离子方程式
①________________________________________ 。
②________________________________________ 。

Ⅰ.(1)④、⑤、⑧的离子半径由大到小的顺序为
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)
 由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂,
由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂, 可与
可与 的水溶液反应,产物有
的水溶液反应,产物有 的最高价含氧酸,该反应的化学方程式为
的最高价含氧酸,该反应的化学方程式为Ⅱ.以下框图中的物质均为中学中常见的化合物或单质(部分产物略去),已知化合物
 为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
(1)化合物
 的电子式为
的电子式为 的化学式为
的化学式为(2)写出反应①和反应②的离子方程式
①
②
您最近一年使用:0次
名校
7 . 根据 A-I 在周期表中的位置,用元素符号或化学式回答下列问题。
(1)表中元素,化学性质最不活泼的是_____ ,只有负价而无正价的是_____ ,氧化性最强的单质是____ ;
(2)最高价氧化物的水化物碱性最强的是_____ ,酸性最强的是_____ ,呈两性的是_____ ;
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是_____ ;
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是_____ ;
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是_______ 可以验证该结论的实验是_ 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
2019-10-25更新
|
118次组卷
|
2卷引用:上海外国语大学附属外国语学校2017-2018学年高二12月月考化学试题
解题方法
8 . W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
2019-09-26更新
|
386次组卷
|
2卷引用:学科网2019年高三11月大联考(样卷)化学试题
13-14高一·全国·课时练习
名校
解题方法
9 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序是________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________ 。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________ 。
A.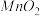 B.
B.
C. D.
D.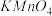
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
A.
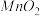 B.
B.
C.
 D.
D.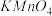
您最近一年使用:0次
2019-08-20更新
|
164次组卷
|
7卷引用:2014年高一化学人教版必修2 模块水平检测1练习卷
(已下线)2014年高一化学人教版必修2 模块水平检测1练习卷(已下线)2013-2014山东省淄博市高一下学期期末考试化学试卷2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷2015-2016学年山西省长治一中高一平行班下期中化学试卷云南省峨山彝族自治县第一中学2017-2018学年高二上学期期末市统测模拟考化学试题百所名校联考-必修二模块综合检测山东省泰安市新泰市第二中学2019-2020学年高一下学期期中考试化学试题
名校
10 . X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
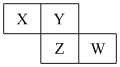

A.Y的价层电子排布式是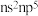 |
| B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物 |
| C.Y、Z之间可形成离子型化合物 |
| D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸 |
您最近一年使用:0次
2019-08-13更新
|
1534次组卷
|
5卷引用:新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题



