30. 工业制硝酸的主要反应为 4NH
3(g)+5O
2(g)
⇌4NO(g)+6H
2O(l)
△H
(1)已知:氢气的燃烧热为285.8 kJ•mol
-1N
2(g)+3H
2(g)
⇌2NH
3(g)
△H=-92.4 kJ•mol
-1N
2(g)+O
2(g)
⇌2NO(g)
△H=+180.6 kJ•mol
-1则上述工业制硝酸的主要反应的
△H=
______。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 浓度 | c(NH3)(mol•L-1) | c(O2)(mol•L-1) | c(NO)(mol•L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2 min | 0.6 | a | 0.2 |
| 第4 min | 0.3 | 0.975 | 0.5 |
| 第6 min | 0.3 | 0.975 | 0.5 |
| 第8 min | 0.7 | 1.475 | 0.1 |
①反应在第2 min到第4 min内,O
2的平均反应速率为
______。
②反应在第6 min时改变了条件,改变的条件可能是
______(填序号)。
A 使用催化剂 B 升高温度
C 减小压强
D 增加O
2的浓度
③下列说法中能说明4NH
3(g)+5O
2(g)
⇌4NO(g)+6H
2O(g)达到平衡状态的是
______(填序号)。
A 单位时间内生成n mol NO的同时,生成n mol NH
3B 条件一定,混合气体的平均相对分子质量不再变化
C 百分含量w(NH
3)=w(NO)
D 反应速率v(NH
3)∶v(O
2) ∶v(NO) ∶v(H
2O)=4∶5∶4∶6
E 若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH
3OH-O
2燃料电池的工作原理如图所示。
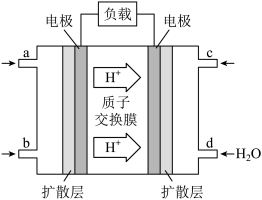
①该电池工作时,b口通入的物质为
______。
②该电池正极的电极反应式为
______。