四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
(1)写出B原子的电子排布式______ 。写出C原子的电子排布式______
(2)四种元素中非金属性最强的元素是______ ,金属性最强的元素是______ ,第一电离能最大的元素是______ ;
(3)一定条件下B、C单质间能反应,相应的反应方程式为______ 。
(4)已知S+6HNO3=H2SO4+6NO2↑+2H2O,该反应表明利用硝酸可以制取硫酸,但该反应不能用于说明氮元素的非金属性比硫元素的强,理由是______ 。
| 元素 | A | B | C | D |
| 性质 结构 信息 | 核外电子共有7种运动状态 | 原子的M层有1对成对的p电子 | 一种核素的中子数为35、质量数为64 | 有多种同位素,其中一种用做测量相对原子质量的校准 |
(1)写出B原子的电子排布式
(2)四种元素中非金属性最强的元素是
(3)一定条件下B、C单质间能反应,相应的反应方程式为
(4)已知S+6HNO3=H2SO4+6NO2↑+2H2O,该反应表明利用硝酸可以制取硫酸,但该反应不能用于说明氮元素的非金属性比硫元素的强,理由是
更新时间:2019-08-13 20:52:48
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁、铬、锰、镍及化合物在生产生活中应用广泛。
(1)铁元素在元素周期表中位置为____ 。KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为____ 。
(2)Ni原子基态原子价层电子排布式为____ ,区分晶体Ni和非晶体Ni最可靠的科学方法为_____ 。
(3)六羰基铬[Cr(CO)6]用于制造高纯度铬粉,它的沸点为220℃,Cr(CO)6的晶体类型为____ ,Cr(CO)6中键和π键的个数之比____ 。
(4)P、S的第二电离能(I2)的大小关系为I2(P)____ I2(S),原因是_____ 。β—MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。
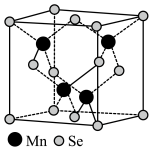
①β—MnSe中Mn的配位数为____ 。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为____ pm。
(1)铁元素在元素周期表中位置为
(2)Ni原子基态原子价层电子排布式为
(3)六羰基铬[Cr(CO)6]用于制造高纯度铬粉,它的沸点为220℃,Cr(CO)6的晶体类型为
(4)P、S的第二电离能(I2)的大小关系为I2(P)

①β—MnSe中Mn的配位数为
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】过渡元素 等在生产、生活和科研中都有着广泛用途和重要的研究价值。回答下列问题:
等在生产、生活和科研中都有着广泛用途和重要的研究价值。回答下列问题:
(1)基态Co原子中,核外电子占据的最高能层符号为_______ ;基态 的价电子排布式为
的价电子排布式为_______ 。
(2)Ag元素在元素周期表中与Cu处于相邻周期,则Ag元素在元素周期表分区中属于_______ 区。
(3)① 有顺式和反式两种结构,则
有顺式和反式两种结构,则 分子的空间构型为
分子的空间构型为_______ (填“平面四方”或“正四面体”)形,其中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B. C.
C. D.
D.
②电子亲和能反映的是元素的气态原子结合电子的难易程度。N、Cl的第一电子亲和能:N_______ Cl(填“>”或“<”)。
(4) 熔点为
熔点为 ,
, 熔点为
熔点为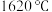 ,
, 熔点更高的原因是
熔点更高的原因是_______ 。
(5)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(x、y方向的夹角为 ,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示;晶胞中碳原子的投影位置如图乙所示。
,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示;晶胞中碳原子的投影位置如图乙所示。
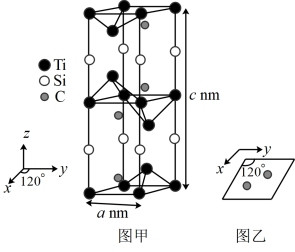
①该钛硅碳新型材料的化学式为_______ 。
②已知该新型材料的摩尔质量为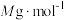 ,密度为
,密度为 ,阿伏加德罗常数的值用
,阿伏加德罗常数的值用 表示,则c的长度为
表示,则c的长度为_______ nm(用含a、b、 的计算式表示)。
的计算式表示)。
 等在生产、生活和科研中都有着广泛用途和重要的研究价值。回答下列问题:
等在生产、生活和科研中都有着广泛用途和重要的研究价值。回答下列问题:(1)基态Co原子中,核外电子占据的最高能层符号为
 的价电子排布式为
的价电子排布式为(2)Ag元素在元素周期表中与Cu处于相邻周期,则Ag元素在元素周期表分区中属于
(3)①
 有顺式和反式两种结构,则
有顺式和反式两种结构,则 分子的空间构型为
分子的空间构型为A.sp B.
 C.
C. D.
D.
②电子亲和能反映的是元素的气态原子结合电子的难易程度。N、Cl的第一电子亲和能:N
(4)
 熔点为
熔点为 ,
, 熔点为
熔点为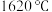 ,
, 熔点更高的原因是
熔点更高的原因是(5)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(x、y方向的夹角为
 ,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示;晶胞中碳原子的投影位置如图乙所示。
,z方向垂直于x、y方向,底面棱长均为anm,侧面棱长为cnm),其晶胞结构如图甲所示;晶胞中碳原子的投影位置如图乙所示。
①该钛硅碳新型材料的化学式为
②已知该新型材料的摩尔质量为
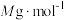 ,密度为
,密度为 ,阿伏加德罗常数的值用
,阿伏加德罗常数的值用 表示,则c的长度为
表示,则c的长度为 的计算式表示)。
的计算式表示)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钠是一种活泼金属,其单质及化合物在科研、生产中有重要的作用。
(1)基态钠原子核外电子的空间运动状态有___________ 种。
(2)冰晶石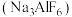 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。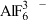 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是___________ (填字母)。
A. B.
B. C.
C. D.
D.
② 晶体中存在的作用力有
晶体中存在的作用力有___________ (填字母)。
A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3) 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是___________ 。
(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为___________ ,硼氢化钠晶胞中与 紧邻的
紧邻的 个数是
个数是___________ 。
(5)有研究表明,在超高压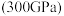 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成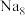 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示: 的最短距离为
的最短距离为___________  (用含a的代数式表示)。
(用含a的代数式表示)。
(1)基态钠原子核外电子的空间运动状态有
(2)冰晶石
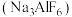 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。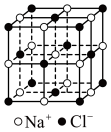
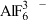 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是A.
 B.
B. C.
C. D.
D.
②
 晶体中存在的作用力有
晶体中存在的作用力有A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3)
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。
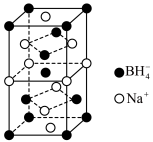
 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为 紧邻的
紧邻的 个数是
个数是(5)有研究表明,在超高压
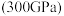 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成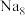 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示: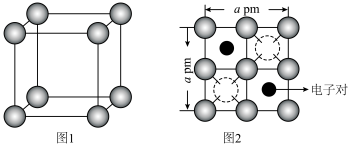
 的最短距离为
的最短距离为 (用含a的代数式表示)。
(用含a的代数式表示)。
您最近半年使用:0次
【推荐1】金属在自然界中广泛存在,在生活中应用极为普遍,是在现代工业中非常重要和应用最多的一类物质。海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有锰、铁、钴、锌等元素。
(1) 中Co2+的配位数为4,基态Co2+的价电子排布式为
中Co2+的配位数为4,基态Co2+的价电子排布式为___________ ;根据价层电子对互斥理论,预测配体 的空间构型为
的空间构型为___________ 形,该配离子中各元素第一电离能由大到小顺序为___________ (填元素符号),配体中N原子杂化方式为___________ ;请写出一种该配离子中配体的等电子体离子:___________ ; 含
含___________ molσ键。
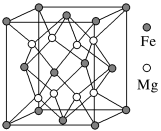
(2)铁镁合金MgxFey是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。储氢时,H2分子在晶胞的体心和棱的中心位置,且最近的两个氢分子之间的距离为anm。该镁合金的化学式为___________ ,在铁镁合金晶体中,与铁原子等距离且最近的铁原子数为___________ ,该铁镁合金储氢后的晶体密度为___________  (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)
 中Co2+的配位数为4,基态Co2+的价电子排布式为
中Co2+的配位数为4,基态Co2+的价电子排布式为 的空间构型为
的空间构型为 含
含(2)铁镁合金MgxFey是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。储氢时,H2分子在晶胞的体心和棱的中心位置,且最近的两个氢分子之间的距离为anm。该镁合金的化学式为
 (用
(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)
(1)D位于周期表中_______ 区,E的核外电子排布式是_____________________ 。
(2)B、C、D第一电离能由大到小为__________________ 。
(3)A和C形成的常见分子中,中心原子的杂化方式为_________ 。
(4)1molABC分子中含有σ键数目为_________ 。
(5)与化合物BD互为等电子体的阴离子化学式为_________ 。
(6)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是__________________ 。
| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数为偶数 |
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)
(1)D位于周期表中
(2)B、C、D第一电离能由大到小为
(3)A和C形成的常见分子中,中心原子的杂化方式为
(4)1molABC分子中含有σ键数目为
(5)与化合物BD互为等电子体的阴离子化学式为
(6)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是
您最近半年使用:0次
【推荐3】短周期的7种元素A、B、C、D、E、F、G的原子序数依次增大,其中A原子中的电子只有1种运动状态,且与B同主族,C的基态原子2p能级上只有1个电子,F与A可形成两种常温下的液态化合物;F与G同主族。根据上述描述,请回答下列问题:
(1)上述7种元素中电负性最小的元素与A元素形成的化合物的电子式为______ (用具体元素符号表示电子式),基态原子的一电离能最大的元素是_____ (填元素符号)。
(2)1molD3A6链状分子中含有的σ键数为________ 。
(3)已知A2F2的分子结构如图所示:
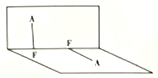
①用电离方程式表示呈弱酸性的原因:______________ 。
②A2F2的沸点比A2F高的原因:_______________ 。
(1)上述7种元素中电负性最小的元素与A元素形成的化合物的电子式为
(2)1molD3A6链状分子中含有的σ键数为
(3)已知A2F2的分子结构如图所示:

①用电离方程式表示呈弱酸性的原因:
②A2F2的沸点比A2F高的原因:
您最近半年使用:0次



