28. 钒、砷均属于第四周期元素,最高正价均为+5价。 羰基铁[Fe(CO)
5]会使合成甲醇和合成氨等生产过程中的催化剂中毒。请回答下列问题:
(1)Fe(CO)
5中铁的化合价为0,写出铁原子的基态外围电子排布式
___________。
(2)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子中C原子的杂化类型为
___________杂化。与CO分子互为等电子体的分子和离子各写出1种,分别为
_____和
______(填化学式)。
(3)Fe(CO)
5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断Fe(CO)
5晶体类型为
___________。
(4)科学家通过X射线探明,MgO、CaO的晶体结构与NaCl的晶体结构相似(如图所示)
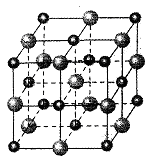
①比较晶体熔点的高低MgO
___________CaO(填“高于”或“低于”) ,
②Mg
2+的配位原子所构成的立体几何构型为
___________,
③MgCO
3晶格能大于CaCO
3,为何MgCO
3更易分解
___________。
(5)Ni的堆积与MgO中氧原子堆积相同,Ni可以吸附H2,氢以单个原子形式填入四面体空隙,则Ni最大量吸收H2后,n(Ni): n(H)=
___________。