23. 电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①HCOONa、NaCN、NaHCO
3、Na
2CO
3这四种溶液的阴离子结合质子能力最强的是
______。
②体积相同、
c(H
+)相同的三种酸溶液a.HCOOH;b.HCN;c.H
2SO
4分别与浓度相等的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填序号)
_____。
③向NaCN溶液通入少量CO
2反应的化学方程式是
_______。
(2)一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是
____,此时,

=
_____。
(3)常温下,向20 mL 0.1 mol/L Na
2CO
3溶液中逐滴加入0.1 mol/L HCl溶液40 mL,溶液中含碳元素的各种微粒(CO
2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
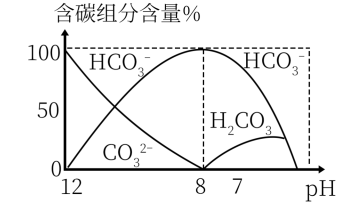
回答下列问题:
在同一溶液中H
2CO
3、

、
 ______
______(填“能”或“不能”)大量共存。
②当pH=7时,溶液中含碳元素的主要微粒为
_____,溶液中各种离子(

除外)的物质的量浓度的大小关系为
______。
③已知在25℃时,

水解反应的平衡常数即水解常数
Kh=
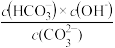
=2.0×10
-4,当溶液中
c(

):
c(

)=2:1时,溶液pH=
______。
(4)已知CaCO
3的
Ksp=2.8×10
-9,现将浓度为2×10
-4 mol/L Na
2CO
3溶液与CaCl
2溶液等体积混合,则生成CaCO
3沉淀所需CaCl
2溶液的最小浓度为
________mol/L。