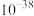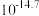名校
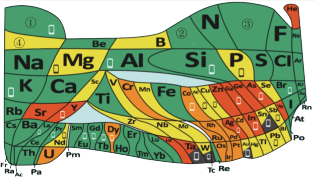
1 . 化学教材后的元素周期表为通用元素周期表,2019年是门捷列夫提出元素周期表诞生150周年,联合国宣布2019年为“国际化学元素周期表年”。同年,欧洲化学学会(EuChemS)发布了1张“扭曲”的元素周期表,指出:由于过度使用,部分元素可能在未来的100年内从地球上消失。每种元素在周期表上所占面积的大小,呈现出元素的稀缺程度。___________ ;④是手机电池的主要构成元素,④的单质在③的常见单质中点燃的方程式为___________ 。
(2)用电子式表示①与③形成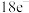 化合物的过程:
化合物的过程:___________ 。
(3)①和②能形成多种化合物,下图模型表示的分子中,不可能由①②形成的有___________ (填序号)。___________ 。
(5)一种新型除草剂的结构如下图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M与Z同主族,W是最不稀缺的元素。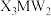 与NaOH溶液反应只生成一种盐,则
与NaOH溶液反应只生成一种盐,则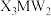 与足量NaOH溶液反应的离子方程式为
与足量NaOH溶液反应的离子方程式为___________ 。
② 可做火箭推进剂的燃料,优点之一是其与
可做火箭推进剂的燃料,优点之一是其与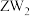 反应的产物绿色无污染,请写出相应的化学方程式
反应的产物绿色无污染,请写出相应的化学方程式___________ 。
(2)用电子式表示①与③形成
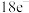 化合物的过程:
化合物的过程:(3)①和②能形成多种化合物,下图模型表示的分子中,不可能由①②形成的有
a. 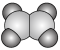 b.
b.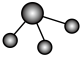 c.
c. 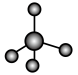 d.
d.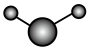
(5)一种新型除草剂的结构如下图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M与Z同主族,W是最不稀缺的元素。
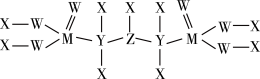
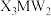 与NaOH溶液反应只生成一种盐,则
与NaOH溶液反应只生成一种盐,则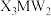 与足量NaOH溶液反应的离子方程式为
与足量NaOH溶液反应的离子方程式为②
 可做火箭推进剂的燃料,优点之一是其与
可做火箭推进剂的燃料,优点之一是其与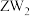 反应的产物绿色无污染,请写出相应的化学方程式
反应的产物绿色无污染,请写出相应的化学方程式
您最近一年使用:0次
2 .  是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:
(1)写出 在周期表中的位置
在周期表中的位置___________ 。
(2)将 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为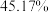 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式___________ (已知:固体残留率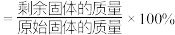 )。
)。
(3)将固体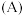 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比___________ 。
(4)该正极材料充电一段时间后变为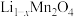 ,为测定
,为测定 的值。称取
的值。称取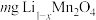 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为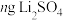 ,写出
,写出 的表达式
的表达式___________ 。
 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:(1)写出
 在周期表中的位置
在周期表中的位置(2)将
 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为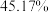 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式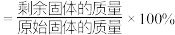 )。
)。(3)将固体
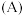 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比(4)该正极材料充电一段时间后变为
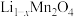 ,为测定
,为测定 的值。称取
的值。称取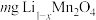 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为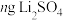 ,写出
,写出 的表达式
的表达式
您最近一年使用:0次
解题方法
3 . 碲 被誉为尖端技术等工业的维生素。工业上常以粗铜精炼的阳极泥(主要成分是
被誉为尖端技术等工业的维生素。工业上常以粗铜精炼的阳极泥(主要成分是 ,含
,含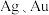 等杂质)为原料提取碲并回收金属,其工艺流程如下图所示:
等杂质)为原料提取碲并回收金属,其工艺流程如下图所示: 与S同一主族,比S原子多2个电子层;
与S同一主族,比S原子多2个电子层; 是两性氧化物,微溶于水。请按要求回答下列问题:
是两性氧化物,微溶于水。请按要求回答下列问题:
(1)碲在元素周期表中的位置_______ ;其最高价氧化物对应的水化物化学式为_______ 。
(2) 与稀
与稀 反应的离子方程式为
反应的离子方程式为_______ 。
(3)步骤①中 发生了(填“氧化”或“还原”或“非氧化还原”)
发生了(填“氧化”或“还原”或“非氧化还原”)_______ 反应;此过程控制 不宜过低的原因是
不宜过低的原因是_______ ;“加压”的目的是_______ 。
(4)步骤②当温度过高时,会导致碲的浸出率降低,原因是_______ 。为提 等滤渣酸浸速率,除适当升温外,还可采取的措施是
等滤渣酸浸速率,除适当升温外,还可采取的措施是_______ (写出1条)。
(5)步骤③铜从(填“阳”或“阴”)_______ 极得到。写出步骤④的离子方程式:_______ 。
(6)常温下,往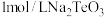 溶液中滴加盐酸,当溶液
溶液中滴加盐酸,当溶液 时,溶液中
时,溶液中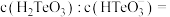
_______ (已知: 的
的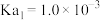 ,
,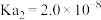 )。
)。
 被誉为尖端技术等工业的维生素。工业上常以粗铜精炼的阳极泥(主要成分是
被誉为尖端技术等工业的维生素。工业上常以粗铜精炼的阳极泥(主要成分是 ,含
,含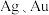 等杂质)为原料提取碲并回收金属,其工艺流程如下图所示:
等杂质)为原料提取碲并回收金属,其工艺流程如下图所示:
 与S同一主族,比S原子多2个电子层;
与S同一主族,比S原子多2个电子层; 是两性氧化物,微溶于水。请按要求回答下列问题:
是两性氧化物,微溶于水。请按要求回答下列问题:(1)碲在元素周期表中的位置
(2)
 与稀
与稀 反应的离子方程式为
反应的离子方程式为(3)步骤①中
 发生了(填“氧化”或“还原”或“非氧化还原”)
发生了(填“氧化”或“还原”或“非氧化还原”) 不宜过低的原因是
不宜过低的原因是(4)步骤②当温度过高时,会导致碲的浸出率降低,原因是
 等滤渣酸浸速率,除适当升温外,还可采取的措施是
等滤渣酸浸速率,除适当升温外,还可采取的措施是(5)步骤③铜从(填“阳”或“阴”)
(6)常温下,往
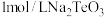 溶液中滴加盐酸,当溶液
溶液中滴加盐酸,当溶液 时,溶液中
时,溶液中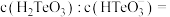
 的
的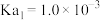 ,
,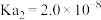 )。
)。
您最近一年使用:0次
名校
解题方法
4 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 、
、 、
、 、
、 、
、 、
、 )实现镍、钴、镁元素的回收。
)实现镍、钴、镁元素的回收。 )的电离第一步完全,第二步微弱。
)的电离第一步完全,第二步微弱。
2.25℃时,相关物质的 如下:
如下:
回答下列问题:
(1)Ni属于元素周期表的________ 区。
(2)混合气在“氧化”中,产生 ,其中S的化合价为
,其中S的化合价为________ 。
(3)“滤渣”的成分之一是软锰矿的主要成分,由 氧化产生,该反应的离子方程式为
氧化产生,该反应的离子方程式为________ ;其可用于实验室制取氯气,该反应的离子方程式为________ 。
(4)若使 沉淀完全(浓度
沉淀完全(浓度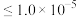 ),需调节pH不低于
),需调节pH不低于________ 。
(5)上述表格中a________ b(填“大于”、“小于”或“无法确定”)。
(6)“沉钴镍”后需将钴镍渣洗涤干净,实验室检验其是否洗净的方法是________ 。
(7)滤液2中含有的金属阳离子是________ 。
 、
、 、
、 、
、 、
、 、
、 )实现镍、钴、镁元素的回收。
)实现镍、钴、镁元素的回收。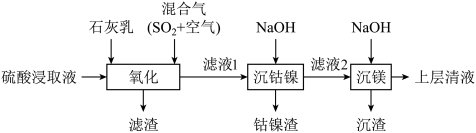
 )的电离第一步完全,第二步微弱。
)的电离第一步完全,第二步微弱。2.25℃时,相关物质的
 如下:
如下:物质 |
|
|
|
|
|
|
| a | b |
(1)Ni属于元素周期表的
(2)混合气在“氧化”中,产生
 ,其中S的化合价为
,其中S的化合价为(3)“滤渣”的成分之一是软锰矿的主要成分,由
 氧化产生,该反应的离子方程式为
氧化产生,该反应的离子方程式为(4)若使
 沉淀完全(浓度
沉淀完全(浓度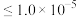 ),需调节pH不低于
),需调节pH不低于(5)上述表格中a
(6)“沉钴镍”后需将钴镍渣洗涤干净,实验室检验其是否洗净的方法是
(7)滤液2中含有的金属阳离子是
您最近一年使用:0次
2024-06-06更新
|
188次组卷
|
2卷引用:辽宁省大连市2023-2024学年高三下学期第二次模拟考试化学试卷
5 . 一种超导材料(仅由Cs、Ag、F三种元素组成)的长方体晶胞结构如图所示(已知 ),下列说法错误的是
),下列说法错误的是
 ),下列说法错误的是
),下列说法错误的是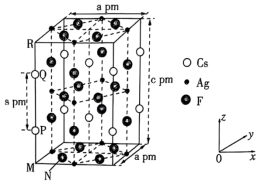
| A.基态47Ag位于元素周期表的ds区 |
B.若N点原子分数坐标为(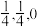 ),则P点原子分数坐标为( ),则P点原子分数坐标为(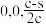 ) ) |
C.M、N之间的距离为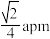 |
D.该化合物的密度为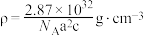 |
您最近一年使用:0次
2024-05-13更新
|
140次组卷
|
2卷引用:东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题
名校
6 . 钨(W)常用于制造白炽灯、碘钨灯等。工业上以黑钨矿(主要成分是 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。
请回答下列问题:
(1)基态 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是__________ ;Mn位于元素周期表__________ 区。
(2)“粉碎”的目的是__________ ;从“浸取”得到的浸渣中分离出 的操作方法是
的操作方法是__________ 、过滤、洗涤、干燥。
(3)根据“转化”,判断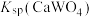
__________ 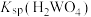 (填“>”或“<”)。
(填“>”或“<”)。
(4)“灼烧”中盛装固体的仪器是__________ (填名称);发生反应的化学方程式为______________________________ 。
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm, 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为__________  (列出计算式即可)。
(列出计算式即可)。
 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。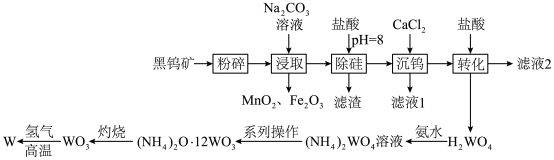
请回答下列问题:
(1)基态
 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是(2)“粉碎”的目的是
 的操作方法是
的操作方法是(3)根据“转化”,判断
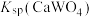
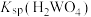 (填“>”或“<”)。
(填“>”或“<”)。(4)“灼烧”中盛装固体的仪器是
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm,
 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为 (列出计算式即可)。
(列出计算式即可)。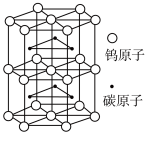
您最近一年使用:0次
2024-05-11更新
|
70次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
名校
解题方法
7 . 新型储氢合金材料的研究和开发将为氢气作为能源的实际应用起到重要的推动作用。两种常见储氢合金的晶胞结构如图所示。设阿伏加德罗常数为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是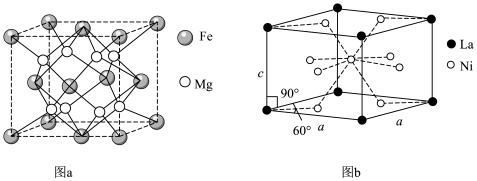
| A.图中涉及的四种元素均为d区元素 |
B.图b晶体的化学式为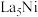 |
C.图a晶体晶胞边长为dpm,该合金的密度为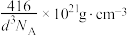 |
D.图a晶体储氢时,储存的氢相当于 分子在晶胞的体心和棱心位置,则含24g Mg的该储氢合金储存的 分子在晶胞的体心和棱心位置,则含24g Mg的该储氢合金储存的 在标准状况下的体积约为11.2L 在标准状况下的体积约为11.2L |
您最近一年使用:0次
2024-05-09更新
|
278次组卷
|
4卷引用:辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷
名校
8 . 镓(Ga)是非常重要的稀土金属,其化合物广泛应用于诸多领域。
(1)镓元素在元素周期表中的位置是___________ 。
(2)GaN作为第三代半导体材料,广泛应用于大功率充电器和5G通讯技术。工业上利用炼锌矿渣[主要含可溶性铁酸镓 、铁酸锌
、铁酸锌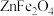 ]制备并提取GaN,工艺流程如下:
]制备并提取GaN,工艺流程如下:
①“酸浸”过程中 发生的反应的离子方程式为
发生的反应的离子方程式为___________ 。
②利用上述工艺,酸浸后的酸浸液应加入___________ 固体充分反应后再进行萃取。
③“反萃取”后,溶液中镓元素的存在形式为___________ (填离子符号)。
④回收金属元素时,锌主要从___________ 中回收。
A.浸出渣 B.酸浸液 C.水相 D.有机相
(3)MOCVD法是通过 与
与 反应得到GaN和另一种产物,该反应的化学方程式为
反应得到GaN和另一种产物,该反应的化学方程式为___________ 。
(4)该流程中,可以循环使用的物质是___________ 。
(1)镓元素在元素周期表中的位置是
(2)GaN作为第三代半导体材料,广泛应用于大功率充电器和5G通讯技术。工业上利用炼锌矿渣[主要含可溶性铁酸镓
 、铁酸锌
、铁酸锌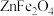 ]制备并提取GaN,工艺流程如下:
]制备并提取GaN,工艺流程如下: 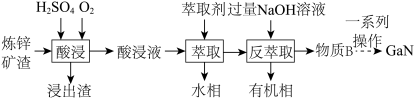
| 金属离子 |  |  |  |  |
| 萃取率/% | 0 | 0 | 99 | 97~98.5 |
 发生的反应的离子方程式为
发生的反应的离子方程式为②利用上述工艺,酸浸后的酸浸液应加入
③“反萃取”后,溶液中镓元素的存在形式为
④回收金属元素时,锌主要从
A.浸出渣 B.酸浸液 C.水相 D.有机相
(3)MOCVD法是通过
 与
与 反应得到GaN和另一种产物,该反应的化学方程式为
反应得到GaN和另一种产物,该反应的化学方程式为(4)该流程中,可以循环使用的物质是
您最近一年使用:0次
名校
9 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
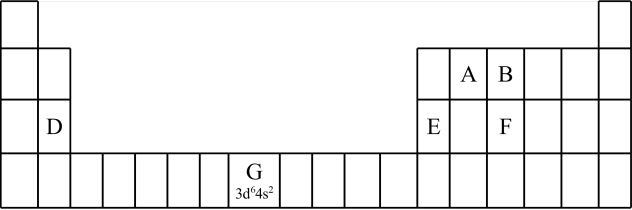
(1)认识元素周期表的结构:___________ 区。
②2017年5月9日我国发布了113号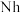 、115号
、115号 、117号
、117号 、118号
、118号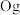 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D_______ E(填“>” “<”或“=”)。
②气态氢化物的沸点:B_____ F (填“>”“<”或“=”),理由是___________ 。B的另一种氢化物可以作为火箭推进剂的燃料之一,其电子式为___________ 。
(1)认识元素周期表的结构:
②2017年5月9日我国发布了113号
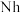 、115号
、115号 、117号
、117号 、118号
、118号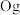 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
2024-04-26更新
|
58次组卷
|
2卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
名校
解题方法
10 . I.氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式___________ 。
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为___________ 。
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是___________ ,其中 H2S在该反应中___________ (填序号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是___________ (填“还原性”或“氧化性”)。
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:___________ 。
(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式___________ 。
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是___________ 。
(8)比较④与⑨的简单气态氢化物的稳定性___________ >___________ (填化学式)。
(9)由下列元素形成的化合物中含有离子键的是___________。
(10)写出⑤在空气中燃烧产物的电子式:___________ 。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是
(8)比较④与⑨的简单气态氢化物的稳定性
(9)由下列元素形成的化合物中含有离子键的是___________。
| A.①③ | B.②③ | C.①④ | D.⑥⑨ |
您最近一年使用:0次