解题方法
1 . 如图显示元素周期表中钾元素的部分信息,其中“39.10”表示________ 。
B.钾元素的相对原子质量
C.钾元素的原子序数
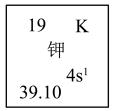
B.钾元素的相对原子质量
C.钾元素的原子序数
您最近一年使用:0次
名校
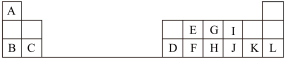
2 . 如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)___ 。
(2)元素E的最高价氧化物的电子式是____ 。
(3)某三原子分子有18个电子,该分子的空间构型为____ 。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为____ 。
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为____ 。
(6)元素B的最高氧化物的水化物的电子式是___ ,其中含有的化学键为____ 。
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为____ (填元素名称),该原电池的负极电极反应式____ 。
(2)元素E的最高价氧化物的电子式是
(3)某三原子分子有18个电子,该分子的空间构型为
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为
(6)元素B的最高氧化物的水化物的电子式是
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为
您最近一年使用:0次
解题方法
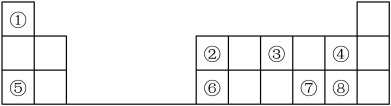
3 . 下表是元素周期表的一部分,①~⑧代表对应的元素,回答下列问题:___________ 。
(2)⑦在元素周期表中的位置是___________ ;⑧的原子结构示意图为___________ 。
(3)②③⑧的最高价氧化物对应水化物酸性由强到弱为___________ (填化学式),③的单质的结构式为___________ 。
(4)④⑤⑧的简单离子半径大小顺序是___________ (填离子),④的单质和 发生置换反应的化学方程式为
发生置换反应的化学方程式为___________ 。
(5)写出⑥的单质与⑤最高价氧化物水化物反应的离子方程式:___________ 。
(6)下列方法能比较⑤和⑥的金属性强弱的是___________(填标号)。
(2)⑦在元素周期表中的位置是
(3)②③⑧的最高价氧化物对应水化物酸性由强到弱为
(4)④⑤⑧的简单离子半径大小顺序是
 发生置换反应的化学方程式为
发生置换反应的化学方程式为(5)写出⑥的单质与⑤最高价氧化物水化物反应的离子方程式:
(6)下列方法能比较⑤和⑥的金属性强弱的是___________(填标号)。
| A.相同条件下,比较⑤、⑥的单质与水反应的剧烈程度 |
| B.比较⑤、⑥最高价氧化物水化物的碱性强弱 |
| C.比较⑤、⑥简单离子所带电荷的多少 |
| D.将⑤的单质投入⑥的盐溶液中,观察实验现象 |
您最近一年使用:0次
名校
解题方法
4 . 元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。 在元素周期表中的位置为:
在元素周期表中的位置为:_____ (写出周期和族)。
(2) 的最高正价为
的最高正价为_____ , 的气态氢化物的化学式为
的气态氢化物的化学式为_____ 。
(3)根据元素周期律推断,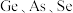 三种元素的原子半径
三种元素的原子半径由小到大 的顺序是____ (填元素符号);阴影部分元素的氢化物最稳定的是_____ (填化学式); 和
和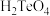 的酸性强弱:
的酸性强弱:
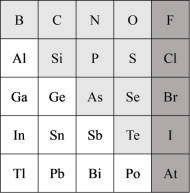
_____ (填“>”“<”或“=”)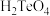 。
。
(4)可在图中分界线(明暗交界处)附近寻找_____(填字母)。
(5)硒( )化铟(
)化铟( )是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
(6)工业上提取纳米硒的第一步是向浆化的电冶铜的阳极泥中通入氯气, 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为____ 。
 在元素周期表中的位置为:
在元素周期表中的位置为:(2)
 的最高正价为
的最高正价为 的气态氢化物的化学式为
的气态氢化物的化学式为(3)根据元素周期律推断,
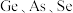 三种元素的原子半径
三种元素的原子半径 和
和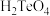 的酸性强弱:
的酸性强弱:
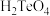 。
。(4)可在图中分界线(明暗交界处)附近寻找_____(填字母)。
| A.农药 | B.合金材料 | C.半导体材料 | D.优良的催化剂 |
 )化铟(
)化铟( )是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。A.原子半径: | B. 的金属性比 的金属性比 强 强 |
C. 的金属性比 的金属性比 弱 弱 | D.硒化铟的化学式为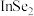 |
 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
5 . 下图是元素周期表的一部分,回答下列问题:___________ 。
(2)元素③和⑤能形成多种化合物,其中可作供氧剂的化合物电子式为___________ 。
(3)元素⑤⑥⑧最高价氧化物对应水化物碱性由强到弱顺序为___________ (填化学式)。元素⑥、⑦最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(4)元素⑩的原子序数为35,该元素简单离子的结构示意图为___________ 。
(5)下列可用于判断元素④⑦非金属性强弱的是___________。
(6)从形成化学键类型角度分析,元素①与③易形成多种元素组成的___________ 化合物,一种绿色氧化剂可用于除甲醛(分子式为 )气体,生成两种无毒的氧化物,写出该反应的化学方程式为
)气体,生成两种无毒的氧化物,写出该反应的化学方程式为___________ 。

(2)元素③和⑤能形成多种化合物,其中可作供氧剂的化合物电子式为
(3)元素⑤⑥⑧最高价氧化物对应水化物碱性由强到弱顺序为
(4)元素⑩的原子序数为35,该元素简单离子的结构示意图为
(5)下列可用于判断元素④⑦非金属性强弱的是___________。
| A.氢化物水溶液的酸性强弱:⑦>④ | B.与氢气反应的剧烈程度:④>⑦ |
| C.简单阴离子的还原性:⑦>④ | D.用④的单质与⑦的钠盐溶液反应 |
(6)从形成化学键类型角度分析,元素①与③易形成多种元素组成的
 )气体,生成两种无毒的氧化物,写出该反应的化学方程式为
)气体,生成两种无毒的氧化物,写出该反应的化学方程式为
您最近一年使用:0次
解题方法
6 . 1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。元素周期表的意思远远超出了化学领域本身,他体现了科学规律的本质。如图是元素周期表的一部分,回答下列问题:
(1)元素周期表中位于金属和非金属的交界处,容易找到的元素是___________。
(2)已知核内有48个中子的硒元素的同位素,下列表示该核素的符号正确的是___________。
(3)硒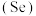 被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
(4)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用 清除人体内的活性氧,此时
清除人体内的活性氧,此时 表现出
表现出___________ 性。(填“氧化”或“还原”)
| B | C |  |  |
 |  |  |  |
 |  | 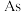 |  |
 |  |  |  |
 |  |  | 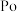 |
| A.制备农药的元素 | B.用于制作半导体材料的元素 |
| C.耐高温的合金元素 | D.制备催化剂的元素 |
A.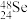 | B. | C.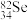 | D.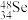 |
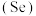 被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。| A.富硒大米中的“硒”指硒元素 | B.最高价氧化物是 |
| C.单质常温下呈固态 | D.硒原子最外层核外电子数为6 |
 清除人体内的活性氧,此时
清除人体内的活性氧,此时 表现出
表现出
您最近一年使用:0次
解题方法
7 . 元素在元素周期表中的位置,反映了元素的原子结构和元素的性质,如下图所示是短周期元素在周期表中的位置。
请回答以下问题:
(1)碳元素在元素周期表中的位置为___________ ,第三周期ⅥA族的元素是___________ (写元素名称)。
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4___________ (填“>”或“<”)HNO3;
②稳定性强弱:H2O___________ (填“>”或“<”)H2S;
③离子半径大小关系:O2-___________ (填“>”或“<”)Mg2+。
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为___________ ,甲的单质与水反应的离子方程式___________ 。
(4)标准状况下,22.4 LCl2的物质的量为___________ mol,质量为___________ g,含有的原子总数为___________ (用NA表示阿伏加德罗常数的数值)。
| 周期 | ⅠA | 0 | ||||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | He | ||
| 2 | Li | Be | B | C | N | O | F | Ne | ||
| 3 | Na | Mg | …… | Al | Si | P | S | Cl | Ar | |
(1)碳元素在元素周期表中的位置为
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4
②稳定性强弱:H2O
③离子半径大小关系:O2-
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为
(4)标准状况下,22.4 LCl2的物质的量为
您最近一年使用:0次
解题方法
8 . 历史上,为了寻求各种元素及其化合物间的内在联系和规律桂,人们进行了许多尝试,并最终绘制成元素周期表。 年量子力学应用于化学开始,化学键建立了比较完整的理论。揭示了物质的特性和结构之间的本质。
年量子力学应用于化学开始,化学键建立了比较完整的理论。揭示了物质的特性和结构之间的本质。
(1)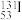 可用于治疗甲亢,有关
可用于治疗甲亢,有关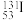 的说法正确的是 ___________ 。
的说法正确的是 ___________ 。
(2)二氧化碳的化学用语错误的是 ___________ 。
(3)下列各组物质中,含有化学键类型都相同的是 ___________ 。
(4)将 和
和 分别溶于水。下列说法正确的是 ___________ 。
分别溶于水。下列说法正确的是 ___________ 。
(5)最早编制元素周期表的科学家是 ___________ 。
(6)如图是某元素原子的原子结构示意图,下列关于该元素的判断错误的是 ___________ 。
(7)相同条件下,下列氢化物中最稳定的是 ___________ 。
(8)氯元素原子结构示意图为___________ 。
(9)钠、铝、铁三种金属中,___________  填名称
填名称 是地壳中含量最高的金属元素,在周期表中位于第
是地壳中含量最高的金属元素,在周期表中位于第 ___________ 周期 ___________ 族。
(10)浓硫酸具有强氧化性,它与铜反应的化学方程式为:___________ 。
(11)列举一个可以说明氯和硫的非金属性强弱的事实:___________ 。
 年量子力学应用于化学开始,化学键建立了比较完整的理论。揭示了物质的特性和结构之间的本质。
年量子力学应用于化学开始,化学键建立了比较完整的理论。揭示了物质的特性和结构之间的本质。(1)
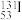 可用于治疗甲亢,有关
可用于治疗甲亢,有关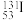 的说法正确的是 ___________ 。
的说法正确的是 ___________ 。A.中子数为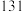 | B.质子数为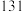 | C.电子数为 | D.质量数为 |
(2)二氧化碳的化学用语错误的是 ___________ 。
A.电子式: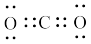 | B.分子式: |
C.结构式: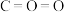 | D.空间填充模型: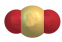 |
(3)下列各组物质中,含有化学键类型都相同的是 ___________ 。
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
(4)将
 和
和 分别溶于水。下列说法正确的是 ___________ 。
分别溶于水。下列说法正确的是 ___________ 。A. 的离子键被破坏 的离子键被破坏 | B. 的共价键被破坏 的共价键被破坏 |
C. 和 和 的化学键遭破坏 的化学键遭破坏 | D. 和 和 的化学键均未遭破坏 的化学键均未遭破坏 |
(5)最早编制元素周期表的科学家是 ___________ 。
| A.居里夫人 | B.卢瑟福 | C.汤姆逊 | D.门捷列夫 |
(6)如图是某元素原子的原子结构示意图,下列关于该元素的判断错误的是 ___________ 。
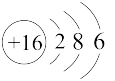
| A.位于第三周期 | B.属于VI 族元素 族元素 | C.最高正价为 价 价 | D.属于非金属元素 |
(7)相同条件下,下列氢化物中最稳定的是 ___________ 。
A. | B. | C. | D. |
(8)氯元素原子结构示意图为
(9)钠、铝、铁三种金属中,
 填名称
填名称 是地壳中含量最高的金属元素,在周期表中位于第
是地壳中含量最高的金属元素,在周期表中位于第 (10)浓硫酸具有强氧化性,它与铜反应的化学方程式为:
(11)列举一个可以说明氯和硫的非金属性强弱的事实:
您最近一年使用:0次
解题方法
9 . 如图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:______ (填元素符号,稀有气体除外),化学性质最不活泼的元素是______ (填“元素名称”)。最高价氧化物对应的水化物碱性最强的是______ (填物质的化学式)
(2)元素⑧的离子结构示意图为______ ,请用电子式表示化合物④和⑧的形成过______ 。
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:____________ 。
(4)元素⑧单质的水溶液中通入元素⑦的某种氧化物,该氧化物被氧化为元素⑦的最高价氧化物的水化物,反应的化学方程式为______ 。
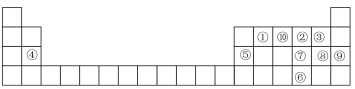
(2)元素⑧的离子结构示意图为
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:
(4)元素⑧单质的水溶液中通入元素⑦的某种氧化物,该氧化物被氧化为元素⑦的最高价氧化物的水化物,反应的化学方程式为
您最近一年使用:0次
10 . 观察下面的周期表,并回答问题____ 。
(2)a与e可以形成一种二元化合物,可以做供氧剂,请写出该化合物的电子式_______ ,该化合物中存在的化学键为______ 。
(3)b、d、e、f元素的简单氢化物最稳定的是____ (填化学式)
(4)e与i的简单离子半径较大的是____ (用离子符号表示),现有一化合物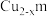 ,(其中
,(其中 元素只有+1价和+2价,无0价),计算
元素只有+1价和+2价,无0价),计算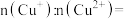
_____ (用含x的式子表示)
(5)e、j能形成一种三原子二元化合物分子,其中所有原子都满足8电子稳定结构,请写出该分子的结构式_______ ,该化合物与 溶液反应生成“84”消毒液,请写出反应的化学方程式
溶液反应生成“84”消毒液,请写出反应的化学方程式______ 。
(6)某同学想在实验室验证b、d、g三种元素的非金属性强弱,设计如图装置:_____ 。
②根据现象____ (填“能”或“否”)得出实验结论,若能请写出三种元素的非金属性强弱顺序,若不能请说明理由______ 。
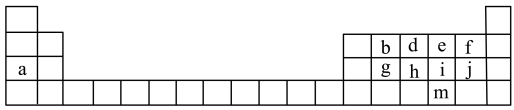
(2)a与e可以形成一种二元化合物,可以做供氧剂,请写出该化合物的电子式
(3)b、d、e、f元素的简单氢化物最稳定的是
(4)e与i的简单离子半径较大的是
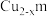 ,(其中
,(其中 元素只有+1价和+2价,无0价),计算
元素只有+1价和+2价,无0价),计算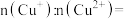
(5)e、j能形成一种三原子二元化合物分子,其中所有原子都满足8电子稳定结构,请写出该分子的结构式
 溶液反应生成“84”消毒液,请写出反应的化学方程式
溶液反应生成“84”消毒液,请写出反应的化学方程式(6)某同学想在实验室验证b、d、g三种元素的非金属性强弱,设计如图装置:
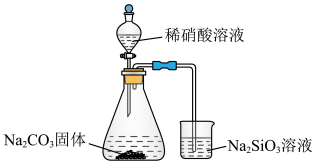
②根据现象
您最近一年使用:0次



