1 . 超导体是由 、
、 、
、 三种元素组成,回答下列问题:
三种元素组成,回答下列问题:
(1) 元素属于元素周期表的
元素属于元素周期表的___________ 区元素,其价电子排布式是___________ 。
(2)基态 原子核外电子排布式为
原子核外电子排布式为___________ 。
 、
、 、
、 三种元素组成,回答下列问题:
三种元素组成,回答下列问题:(1)
 元素属于元素周期表的
元素属于元素周期表的(2)基态
 原子核外电子排布式为
原子核外电子排布式为
您最近一年使用:0次
2 . 据报道,某些花岗岩会产生氡(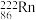 ),对人体产生伤害,如图为
),对人体产生伤害,如图为 的原子结构示意图。
的原子结构示意图。 在元素周期表中的位置为
在元素周期表中的位置为___________ 。
(2)预测氡气的化学性质___________ 。
A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等活泼金属反应
C.不太活泼,与氮气性质相似
D.很难与其他物质发生反应
选择该选项的理由是:___________ 。
(3)研究发现,镭能蜕变为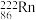 ,故称
,故称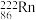 为镭射气;钍能蜕变为
为镭射气;钍能蜕变为 ,故将
,故将 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为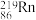 ,故将
,故将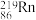 称为锕射气。则
称为锕射气。则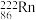 、
、 、
、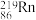 是___________。
是___________。
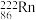 ),对人体产生伤害,如图为
),对人体产生伤害,如图为 的原子结构示意图。
的原子结构示意图。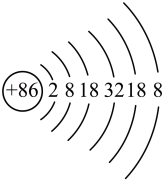
 在元素周期表中的位置为
在元素周期表中的位置为(2)预测氡气的化学性质
A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等活泼金属反应
C.不太活泼,与氮气性质相似
D.很难与其他物质发生反应
选择该选项的理由是:
(3)研究发现,镭能蜕变为
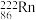 ,故称
,故称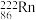 为镭射气;钍能蜕变为
为镭射气;钍能蜕变为 ,故将
,故将 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为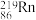 ,故将
,故将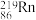 称为锕射气。则
称为锕射气。则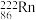 、
、 、
、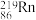 是___________。
是___________。| A.同种元素 | B.同位素 | C.同位核素 | D.同种原子 |
您最近一年使用:0次
3 . 下图是元素周期表的一部分,表中所列数字①~⑧分别代表某种化学元素。请依据这8种元素回答下列问题。___________ 。(填元素符号 )
(2)下列有关性质的比较,不能用元素周期律解释的是___________。
(3)④的单质在 中燃烧,生成的淡黄色物质的化学式为
中燃烧,生成的淡黄色物质的化学式为___________ ,该化合物的电子式:___________ 。
(4)从原子结构的角度解释非金属性:② ③,
③,___________ 。
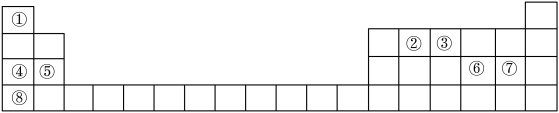
(2)下列有关性质的比较,不能用元素周期律解释的是___________。
A.酸性: | B.金属性: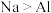 |
C.碱性: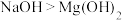 | D.热稳定性: |
(3)④的单质在
 中燃烧,生成的淡黄色物质的化学式为
中燃烧,生成的淡黄色物质的化学式为(4)从原子结构的角度解释非金属性:②
 ③,
③,
您最近一年使用:0次
解题方法
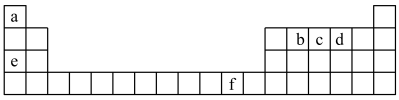
4 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。
(1)元素b位于周期表中_____ 区,其基态原子核外有_____ 种运动状态不同的电子。
(2)基态c原子中有_____ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为_____ 形。
(3) 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为__________ 。
(4)基态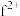 外围电子的轨道表示式为
外围电子的轨道表示式为____________ ,已知高温下化合物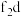 比化合物
比化合物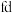 更稳定,试从核外电子排布的角度解释原因
更稳定,试从核外电子排布的角度解释原因_____________ 。
(5)b、c、d三种元素的第一电离能由大到小的顺序为__________ (填元素符号)。
(1)元素b位于周期表中
(2)基态c原子中有
(3)
 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为(4)基态
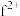 外围电子的轨道表示式为
外围电子的轨道表示式为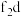 比化合物
比化合物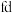 更稳定,试从核外电子排布的角度解释原因
更稳定,试从核外电子排布的角度解释原因(5)b、c、d三种元素的第一电离能由大到小的顺序为
您最近一年使用:0次
解题方法
5 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)在此元素周期表的一部分中,金属性最强的元素是___________ (填元素符号)。
(2)②、⑤、⑥的原子半径由大到小的顺序为___________ (填元素符号)。
(3)⑦、⑧两种元素的氢化物稳定性较强的是___________ (用化学式表示)。
(4)⑤、⑧的最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
| 族 周期 | ⅠA | O | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、⑤、⑥的原子半径由大到小的顺序为
(3)⑦、⑧两种元素的氢化物稳定性较强的是
(4)⑤、⑧的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
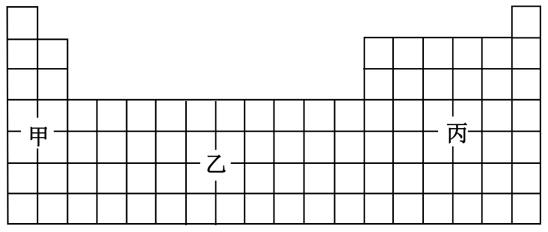
6 . 元素周期表是化学领域的重要工具,在材料、能源、环境和生命科学研究中发挥着重要作用。下面是元素周期表的一部分:_____ 。
2.根据 的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在_____ 族。
2.根据
 的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,可将氢元素放在
您最近一年使用:0次
7 . 德米特里·伊万诺维奇·门捷列夫是著名的俄国化学家,他对化学发展作出了卓越的贡献。请根据实际情况回答下列问题:
1.门捷列夫的突出贡献是
2.某元素的原子L层电子数比K层电子数多3个,与该元素同一主族的短周期元素是___________ 。
3.C、O、Na的原子半径从大到小的顺序为___________ 。
1.门捷列夫的突出贡献是
| A.提出原子学说 | B.发现元素周期律 | C.提出分子学说 | D.发现氧气 |
3.C、O、Na的原子半径从大到小的顺序为
您最近一年使用:0次
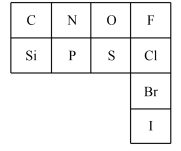
8 . 元素周期表是指导我们系统学习化学的重要工具。下图是元素周期表的一部分。___________ 相同。
2.氮元素的最低化合价为___________ ,其气态氢化物与同主族的元素热稳定性比较___________ >___________ (写化学式,下同);上表中所列元素的最高价氧化物对应水化物中酸性最强的是___________ 。
2.氮元素的最低化合价为
您最近一年使用:0次
9 . 硫元素在周期表中的位置是:第___________ 周期,___________ 族。
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在⑤~⑧元素中,原子半径最大的是_______ (填元素符号,下同),非金属性最强的元素是_______
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有_______ 。
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_______ 。
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是_______ (填离子符号)。
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_______ (填化学式);呈两性的氢氧化物是_______ (填化学式)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
您最近一年使用:0次



