名校
解题方法
1 . 下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
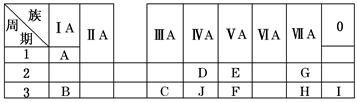
(1)表中元素,化学性质最不活泼的是________ ,只有负价而无正价的元素是________ 。
(2)C元素在元素周期表中的位置是第三周期第________ 族。
(3)最高价氧化物的水化物酸性最强的是________ ,呈两性的是________ 。
(4)A分别与E、G、H形成的化合物中,最稳定的是________ 。
(5)在B、C、E、F中,原子半径最大的是________ 。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________ 。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__________________________ 。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________________________________________________________________________ 。

(1)表中元素,化学性质最不活泼的是
(2)C元素在元素周期表中的位置是第三周期第
(3)最高价氧化物的水化物酸性最强的是
(4)A分别与E、G、H形成的化合物中,最稳定的是
(5)在B、C、E、F中,原子半径最大的是
(6)B、H两种元素所形成的化合物所含的化学键类型为
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
2018-02-11更新
|
1888次组卷
|
5卷引用:人教版2017-2018学年高一化学必修二同步训练:第一章 物质结构 元素周期律
2 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______________________________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布为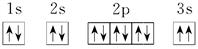 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了_____________________________________ 。
(4)G位于________ 族________ 区,价电子排布式为________ 。
(5)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因是_____________________________________________________________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(4)G位于
(5)检验F元素的方法是
您最近一年使用:0次
2018-02-10更新
|
564次组卷
|
3卷引用:人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质2
名校
解题方法
3 . 下表中的A、B、C、D表示元素周期表中的四个区域:
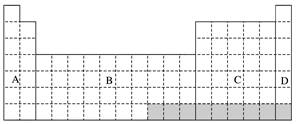
(1)全部是金属元素的区域为____________ 。
(2)短周期甲元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,甲的原子序数是________ 。
(3)短周期乙元素的原子核外第三层电子数与第一层电子数相等,则乙元素位于元素周期表的第_______ 周期第______ 族。
(4)用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置________ 。

(1)全部是金属元素的区域为
(2)短周期甲元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,甲的原子序数是
(3)短周期乙元素的原子核外第三层电子数与第一层电子数相等,则乙元素位于元素周期表的第
(4)用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置
您最近一年使用:0次
2017-12-22更新
|
226次组卷
|
2卷引用:人教版高中化学必修2第一章《物质结构 元素周期律》测试卷
名校
解题方法
4 . 下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。

(1)上述元素的单质可能是电的良导体的是_______ (填字母代号)。
(2)下表是一些气态原子的第一、二、三、四级电离能(kJ·mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:______________________________________ 。
②表中的Y可能为以上13种元素中的_________ (填元素符号)元素,用元素符号表示X和j按原子个数1:1形成化合物的电子式___________________________ 。
(3)根据构造原理,用电子排布式表示e的核外电子排布式_______________ 。
(4)以上13种元素中,________ (填元素符号)元素原子失去核外第一个电子需要的能量最多。
(5)a、e、f三种元素的最高价氧化物的水化物显碱性,其碱性最强的为_______ (用化学符号作答)。f的氧化物具有两性,写出其与NaOH溶液反应的离子方程式___________________ 。

(1)上述元素的单质可能是电的良导体的是
(2)下表是一些气态原子的第一、二、三、四级电离能(kJ·mol-1):
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
②表中的Y可能为以上13种元素中的
(3)根据构造原理,用电子排布式表示e的核外电子排布式
(4)以上13种元素中,
(5)a、e、f三种元素的最高价氧化物的水化物显碱性,其碱性最强的为
您最近一年使用:0次
2016-12-09更新
|
252次组卷
|
4卷引用:第1章 原子结构与元素性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)
(已下线)第1章 原子结构与元素性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)2015-2016学年西藏日喀则一中高二10月月考化学试卷河南省漯河市南街高中2018-2019学年高二下学期期中考试化学试题(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测
12-13高一下·广东揭阳·阶段练习
解题方法
5 . 元素X、Y、Z原子序数之和为36,Y、Z在同一周期,X与Z在同一主族,X原子最外层电子数是Y原子最外层电子数的3倍。
(1)写出下列元素符号:X______ ,Y______ ,Z______
(2)X与Y两元素可形成化合物属______ (“离子”或“共价”)化合物。
(3)写出X与Z所形成的化合物的化学式:______
(1)写出下列元素符号:X
(2)X与Y两元素可形成化合物属
(3)写出X与Z所形成的化合物的化学式:
您最近一年使用:0次
10-11高一下·浙江杭州·期中
解题方法
6 . 3.2 g某元素A 的单质与氢气化合生成3.4 g气态氢化物H2A,已知A 的原子核中质子数和中子数相等,则:
(1) A的原子序数为______ ;
(2) 元素A位于元素周期表中位置:____ _____ ;
(3) 气态氢化物的化学式是_____ ,并书写气态氢化物的电子式_______ 。
(1) A的原子序数为
(2) 元素A位于元素周期表中位置:
(3) 气态氢化物的化学式是
您最近一年使用:0次
10-11高一下·河北·期中
解题方法
7 . 元素X、Y、Z、W均为短周期元素,且原子序数依次增大。已知Y原子最外层电子数占核外电子总数的3/4,W-、Z+、X+的离子半径逐渐减小,化合物XW常温下为气体,Z是本周期中除稀有气体元素外,原子半径最大的元素。据此回答下列问题:
(1)W在元素周期表中的位置___________________ ,实验室制取W单质的离子方程式是____________________________________________________________ ;
(2)A、B均由上述四种元素中的三种组成的强电解质,A是一种强碱,B是某种家用消毒液的有效成分,则A、B的化学式分别为___________ 、____________ ;
(3)C是由Y和Z两种元素组成的一种化合物,其中Y和Z的原子个数比为1∶1,则C的电子式是____________ ;
(1)W在元素周期表中的位置
(2)A、B均由上述四种元素中的三种组成的强电解质,A是一种强碱,B是某种家用消毒液的有效成分,则A、B的化学式分别为
(3)C是由Y和Z两种元素组成的一种化合物,其中Y和Z的原子个数比为1∶1,则C的电子式是
您最近一年使用:0次



