21-22高一上·山东临沂·期末
名校
1 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,相关信息如表。
(1)元素Y在元素周期表中的位置是____ 。
(2)Z在氧气中完全燃烧所得产物的电子式为____ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是____ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。
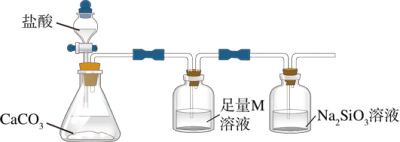
已知:H2SiO3是一种难溶于水的白色物质。
①M为____ (填化学式),其作用是____ 。
②能说明X元素的非金属性比硅元素强的实验现象是____ 。
(5)元素Z与W相比,金属性较弱的是____ (填元素名称),请写出能证明这一结论的实验事实_____ (列举一条)。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是内层电子数的2倍 |
| Y | 其单质与氢气在暗处能剧烈化合并发生爆炸 |
| Z | 短周期元素中原子半径最大 |
| W | 其氧化物是两性氧化物 |
| Q | 同周期元素中,最高价氧化物对应水化物的酸性最强 |
(2)Z在氧气中完全燃烧所得产物的电子式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

已知:H2SiO3是一种难溶于水的白色物质。
①M为
②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近一年使用:0次
2022-09-02更新
|
650次组卷
|
3卷引用:第四章 物质结构 元素周期律(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第四章 物质结构 元素周期律(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)山东省临沂市2021-2022学年高一上学期期末统考化学试题新疆乌鲁木齐市第101中学2022-2023学年高一上学期12月月考化学试题
解题方法
2 . 下表列出了10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的是_______ ,电负性最小的金属元素是_______ 。
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是_______ 。
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是_______ 。
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为_______ 、_______ 。
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:_______ 。
(7)⑨元素原子的价电子的轨道表示式为_______ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑤ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑥ | ⑧ | ⑩ | |||
| 第4周期 | ② | ④ | ⑨ |
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素原子的价电子的轨道表示式为
您最近一年使用:0次
名校
3 . 如图为元素周期表的一部分,列出了前四周期10种主族元素在周期表中的位置。
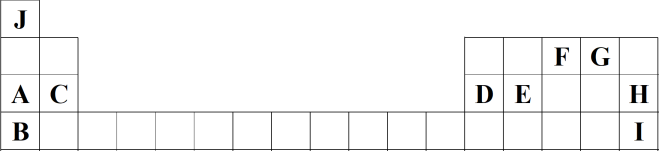
请回答下列问题:
(1)元素E的原子结构示意图为___________ ,I在元素周期表中的位置为___________ ,C与I形成的化合物的电子式为___________ 。
(2)G与J形成原子数之比为 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为___________ ,空间构型为___________ ;元素K与G同主族且位于G的下一周期,P的沸点比元素K的氢化物的沸点高,原因是___________ 。
(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:___________ 。
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为___________ 。
(5)J、F、G、K可以形成原子个数之比为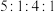 的化合物M,M的化学式为
的化合物M,M的化学式为___________ ;M中含有的化学键类型为___________ 。
(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。

请回答下列问题:
(1)元素E的原子结构示意图为
(2)G与J形成原子数之比为
 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为
(5)J、F、G、K可以形成原子个数之比为
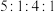 的化合物M,M的化学式为
的化合物M,M的化学式为(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。
A.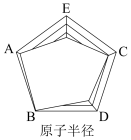 | B.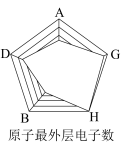 | C.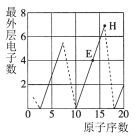 | D.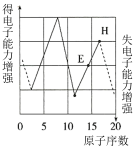 |
您最近一年使用:0次
21-22高二上·河北沧州·期末
4 . 元素周期表中前四周期几种主族元素的位置关系如图所示(过渡元素已忽略)。
请回答下列问题。
(1)①和②能形成简单化合物,该物质的化学式为_______ ,已知该物质为离子化合物,两种离子半径①_______ ②(填“>”“<”或“=”)。
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为_______ (用元素符号表示,下同),电负性由大到小的顺序为_______ 。
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为_______ (用化学式表示)。
(4)元素⑦的基态原子的电子排布式为_______ ,其电子占据的最高能级的轨道形状为_______ 。
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||
| ⑩ | ⑾ |
(1)①和②能形成简单化合物,该物质的化学式为
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为
(4)元素⑦的基态原子的电子排布式为
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因
您最近一年使用:0次
21-22高二·全国·单元测试
解题方法
5 . 如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
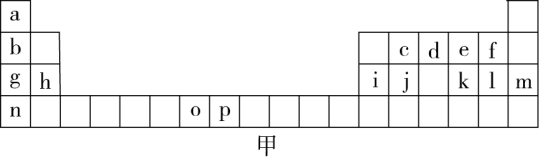
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:___________ 。
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:____________ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的I2、I3可知,气态基态o2+再失去一个电子比基态气态p2+再失去一个电子难。对此,你的解释是___________ 。
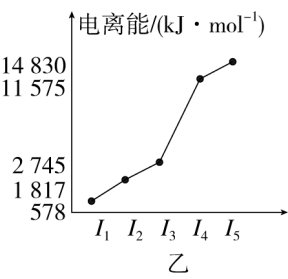
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是___________ (填元素符号)。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是

您最近一年使用:0次
名校
6 . 表为周期表的一部分,其中的编号代表对应的元素,请用元素符号 回答下列问题
(1)上述元素中,属于ds区的是_______ (填元素符号)。
(2)不能 说明⑨的金属性比⑩强的是_______ 。
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 分子的空间构型为_______ 。
(4)元素⑫与 可形成
可形成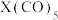 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ⑪ | ⑫ | ⑬ | ⑭ |
(2)
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是
(4)元素⑫与
 可形成
可形成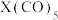 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
2021-04-28更新
|
647次组卷
|
4卷引用:专题4 综合检测(基础卷)
专题4 综合检测(基础卷)(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测天津市耀华中学2020-2021学年高二下学期期中检测化学试题天津北京师范大学静海附属学校2021-2022学年高二下学期期中考试化学试题
20-21高二·全国·单元测试
解题方法
7 . I.元素在周期表中的位置反映了元素的原子结构和性质。请回答下列有关硼(B)元素的问题:
(1)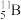 原子核内的中子数为
原子核内的中子数为________ 。
(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为___________ 。
(3)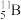 的原子半径比
的原子半径比 的原子半径
的原子半径__________ (填“大”或“小”)。
(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性_______ (填“强”或“弱”)。
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
请回答下列问题:
(1)元素②的原子结构示意图是_______________ 。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为_________ (填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为___________________ 。
(4)⑧与⑩两种元素非金属较强的是_______ (填元素符号)。
(1)
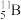 原子核内的中子数为
原子核内的中子数为(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为
(3)
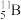 的原子半径比
的原子半径比 的原子半径
的原子半径(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)元素②的原子结构示意图是
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为
(4)⑧与⑩两种元素非金属较强的是
您最近一年使用:0次
8 . 如图是元素周期表的一部分,图中所列的字母分别代表某一化学元素。
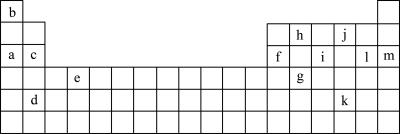
(1)下列______ (填序号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/( )
)
①X可能为图中13种元素中的______ (填字母)。用元素符号表示X和j形成的化合物的化学式:______ 。
②Y是周期表中第______ 族的元素。
③图中13种元素中,______ (填字母)元素原子失去核外第1个电子需要的能量最多。

(1)下列
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/(
 )
)| 元素 | 锂 | X | Y |
| 失去第1个电子 | 519 | 502 | 580 |
| 失去第2个电子 | 7296 | 4570 | 1820 |
| 失去第3个电子 | 11799 | 6920 | 2750 |
| 失去第4个电子 | — | 9550 | 11600 |
②Y是周期表中第
③图中13种元素中,
您最近一年使用:0次
2021-02-06更新
|
682次组卷
|
2卷引用:第一章 原子结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)
20-21高一上·全国·单元测试
9 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
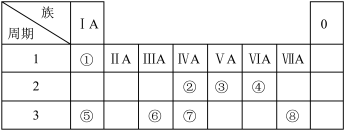
(1)地壳中含量居于第二位的元素在周期表中的位置是______ 。
(2)②的最高价氧化物的分子式为______ ;⑦的最高价氧化物对应水化物的分子式为______ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:______ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是______ (填字母)。
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为_________ 。
②铯单质与H2O反应的化学反应方程式为________ 。
③预测铯单质的还原性比钠单质的还原性________ (填“弱”或“强”)。
④下列推断正确的是________ (填字母)。
A.与铯处于同一主族的元素都是金属元素 B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱 D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素 B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱 D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
19-20高一上·辽宁丹东·期末
名校
解题方法
10 . 为了庆祝元素周期表诞生 150 周年,联合国将 2019 年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(1)⑧所对应的元素名称为______ ,其在周期表中的位置为_____ 。
(2)在①~⑨元素中,原子半径最大的是_____ (填元素符号),这些元素中的某种元素的氧化物可用于呼吸面具中氧气来源,请写出该反应的化学方程式_________ 。
(3)⑤、⑥、⑦三种元素分别形成的最高价氧化物对应的水化物中碱性最强的是____ (填化学式)。
(4)④与⑨两种元素分别形成的气态氢化物的稳定性由强到弱的顺序是_____ (用化学式表示)。
(5)由下列元素形成的化合物中含有离子键的是_____ 。
A.①和③ B.②和③ C.①和④ D.⑥和⑨

(1)⑧所对应的元素名称为
(2)在①~⑨元素中,原子半径最大的是
(3)⑤、⑥、⑦三种元素分别形成的最高价氧化物对应的水化物中碱性最强的是
(4)④与⑨两种元素分别形成的气态氢化物的稳定性由强到弱的顺序是
(5)由下列元素形成的化合物中含有离子键的是
A.①和③ B.②和③ C.①和④ D.⑥和⑨
您最近一年使用:0次
2020-10-13更新
|
276次组卷
|
6卷引用:第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)辽宁省丹东市2019-2020学年高一上学期期末质量监测化学试题山西省晋中市和诚中学2019-2020学年高一3月月考化学试题甘肃省静宁县第一中学2019-2020学年高一下学期第一次月考化学试题青海省海东市第二中学2019-2020学年高一下学期期中考试化学试题湖北省武汉市五校联合体2019-2020学年高一下学期期中考试化学试题



