如图为元素周期表的一部分,列出了前四周期10种主族元素在周期表中的位置。
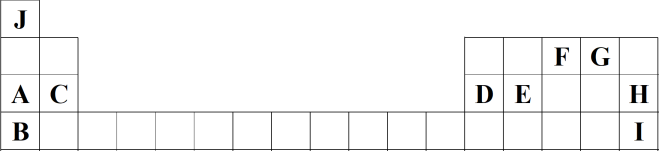
请回答下列问题:
(1)元素E的原子结构示意图为___________ ,I在元素周期表中的位置为___________ ,C与I形成的化合物的电子式为___________ 。
(2)G与J形成原子数之比为 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为___________ ,空间构型为___________ ;元素K与G同主族且位于G的下一周期,P的沸点比元素K的氢化物的沸点高,原因是___________ 。
(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:___________ 。
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为___________ 。
(5)J、F、G、K可以形成原子个数之比为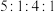 的化合物M,M的化学式为
的化合物M,M的化学式为___________ ;M中含有的化学键类型为___________ 。
(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。

请回答下列问题:
(1)元素E的原子结构示意图为
(2)G与J形成原子数之比为
 的化合物P,P是日常生活中最常见的物质,P分子的结构式为
的化合物P,P是日常生活中最常见的物质,P分子的结构式为(3)已知木炭可在G的单质中完全燃烧形成化合物Q,用电子式表示Q的形成过程:
(4)元素D的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式为
(5)J、F、G、K可以形成原子个数之比为
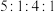 的化合物M,M的化学式为
的化合物M,M的化学式为(6)下图是依据各种元素(原子或离子)的性质对比关系而绘制出来的,其中描述正确的是___________。
A.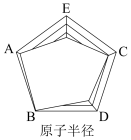 | B.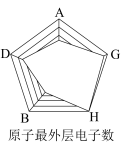 | C.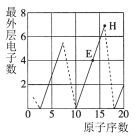 | D.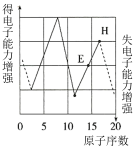 |
更新时间:2022-08-17 22:06:09
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A是一种气态烃。完全燃烧时产生的水和二氧化碳的物质的量之比为1:1。A的相对分子质量小于30。在下图变化中,中间产物C跟葡萄糖一样也能和新制的氢氧化铜反应生成砖红色沉淀。(反应条件未写出)

又知2CH3CHO+O2 2CH3COOH。请回答下列问题:
2CH3COOH。请回答下列问题:
(1)写出A的电子式_______________________ 。
(2)B、D分子内含有的官能团分别是_______ 、_______ (填名称)。
(3)写出下列反应的反应类型:①_____________ ,④_____________ 。
(4)写出下列反应的化学方程式:
①__________________________ ;④___________________________ 。

又知2CH3CHO+O2
 2CH3COOH。请回答下列问题:
2CH3COOH。请回答下列问题:(1)写出A的电子式
(2)B、D分子内含有的官能团分别是
(3)写出下列反应的反应类型:①
(4)写出下列反应的化学方程式:
①
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铅蓄电池的拆解、回收和利用可以减少其对环境的污染,具有重要的可持续发展意义。利用废铅蓄电池的铅膏(主要成分为 、
、 ),还有少量
),还有少量 、
、 、
、 )制备PbO的流程如下:
)制备PbO的流程如下:

回答下列问题:
(1)步骤①将废铅膏研磨过筛的目的是___________ 。
(2)向废铅膏粉中加入NaOH溶液可将 转化为PbO,反应的离子方程式是
转化为PbO,反应的离子方程式是___________ 。
(3)溶液I中主要含有的阴离子有 、
、___________ 。
(4)加入 溶液和
溶液和 溶液可将脱硫铅膏中的含铅物质转化为
溶液可将脱硫铅膏中的含铅物质转化为 。
。 的电子式为
的电子式为___________ , 转化为
转化为 的化学方程式是
的化学方程式是___________ 。
(5)若废铅膏中铅元素的质量分数为69%,用上述流程对1kg废铅膏进行处理,得到669gPbO,则铅的回收率为___________ %。[M(Pb)=207、M(O)=16]
 、
、 ),还有少量
),还有少量 、
、 、
、 )制备PbO的流程如下:
)制备PbO的流程如下:
回答下列问题:
(1)步骤①将废铅膏研磨过筛的目的是
(2)向废铅膏粉中加入NaOH溶液可将
 转化为PbO,反应的离子方程式是
转化为PbO,反应的离子方程式是(3)溶液I中主要含有的阴离子有
 、
、(4)加入
 溶液和
溶液和 溶液可将脱硫铅膏中的含铅物质转化为
溶液可将脱硫铅膏中的含铅物质转化为 。
。 的电子式为
的电子式为 转化为
转化为 的化学方程式是
的化学方程式是(5)若废铅膏中铅元素的质量分数为69%,用上述流程对1kg废铅膏进行处理,得到669gPbO,则铅的回收率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D是短周期元素组成的中学常见的四种物质,它们之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体。
请回答下列问题:
(1)写出B和C的化学式:B________ ,C________ ;
(2)写出A的电子式:____________ ;
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是____________________ ;
(4)写出上图D→C的化学方程式:________________________________________________________________________ 。

请回答下列问题:
(1)写出B和C的化学式:B
(2)写出A的电子式:
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是
(4)写出上图D→C的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表短周期的一部分:

请按要求用化学式回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为:_______ (用化学式回答,下同)
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:_______ ;
(3)写出由①④⑤三种元素组成的一种离子化合物的电子式_______ ,若将其溶于水,破坏了其中的_______ (填“离子键”、“共价键”或“离子键和共价键”):
(4)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物反应的离子方程式_______ 。

请按要求用化学式回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为:
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:
(3)写出由①④⑤三种元素组成的一种离子化合物的电子式
(4)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下列是元素周期表的一部分,表中所列字母分别代表某一化学元素。
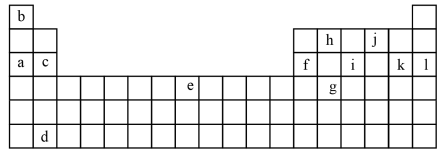
(1)e元素在周期表中的位置是___ ;表中所列元素的单质能用作半导体材料的是___ (填名称)。
(2)写出h与b元素组成的最简单分子的电子式:___ ;i、k元素的最高价氧化物对应水化物的酸性强弱为:____>___(用化学式表示)___ 。
(3)将表中短周期字母元素挑出四种,另用W、X、Y、Z表示,其原子序数X>W>Z>Y,X原子最外层电子数与最内层电子数相等,Y原子最外层电子数是内层电子数的2倍,W原子和Z原子可形成2∶1和1∶1两种化合物,Z原子最外层电子数是核外电子层数的3倍。
①写出Y、Z的元素符号:Y___ ,Z___ 。
②W、X元素的最高价氧化物对应水化物的碱性强弱为:____<____(用化学式表示)___ 。
③这四种元素原子半径的大小为___>____>____>____(填元素符号)___ 。

(1)e元素在周期表中的位置是
(2)写出h与b元素组成的最简单分子的电子式:
(3)将表中短周期字母元素挑出四种,另用W、X、Y、Z表示,其原子序数X>W>Z>Y,X原子最外层电子数与最内层电子数相等,Y原子最外层电子数是内层电子数的2倍,W原子和Z原子可形成2∶1和1∶1两种化合物,Z原子最外层电子数是核外电子层数的3倍。
①写出Y、Z的元素符号:Y
②W、X元素的最高价氧化物对应水化物的碱性强弱为:____<____(用化学式表示)
③这四种元素原子半径的大小为___>____>____>____(填元素符号)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题。
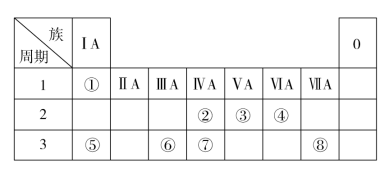
(1)地壳中含量居于第二位的元素在周期表中的位置是____ 。
(2)④和⑤可形成既含离子键又含共价键的离子化合物,写出该化合物的电子式:____ ;用电子式表示①和⑧组成的化合物的形成过程:____ 。
(3)③④⑧的简单气态氢化物的稳定性中大到小是____ (用化学式表示);③④⑤⑥的简单离子的半径由大到小是____ (用化学符号表示)。
(4)⑤⑥的最高价氧化物的水化物可发生反应,其反应的化学方程式为____ 。
(5)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是____ (填字母序号)。
(6)已知X为第四周期第IIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为____ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)④和⑤可形成既含离子键又含共价键的离子化合物,写出该化合物的电子式:
(3)③④⑧的简单气态氢化物的稳定性中大到小是
(4)⑤⑥的最高价氧化物的水化物可发生反应,其反应的化学方程式为
(5)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
| A.最高正化合价为+6 |
| B.气态氢化物比H2S稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
(6)已知X为第四周期第IIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Fe、HCN与K2CO3在一定条件下发生如下反应:
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为___________________ 。
(2)配合物K4Fe(CN)6的中心离子是____________ ,该离子价电子的基态电子排布图为____________ 。
(3)lmol HCN分子中含有σ键的数目为____________ ,HCN分子中碳原子轨道杂化类型是____________ ,与CN-互为等电子体的阴离子是____________ 。
(4)K2CO3中阴离子的空间构型为____________ ,其中碳原子的价层电子对数为____________ 。
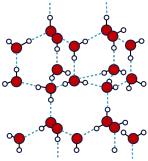
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有__________ 个氢键,若氢键键长为d nm,则晶体密度(g/cm3)计算式为____________ (用NA表示阿伏加德罗常数的值)。
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为
(2)配合物K4Fe(CN)6的中心离子是
(3)lmol HCN分子中含有σ键的数目为
(4)K2CO3中阴离子的空间构型为
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4、6。A和C分子中的原子个数比均为1∶1,B和D分子中原子个数比均为1∶2。D可作为火箭推进剂的燃料。请回答下列问题:
(1)A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小为_______ (填元素符号)。
(2)A与HF相比,其熔、沸点较低,原因是_______ 。
(3)B分子的空间构型为_______ 形,C分子属于_______ (填“极性”或“非极性”)分子。
(4)A、B两分子中心原子的氧化物对应的水化物酸性最强的是_______ (填该含氧酸的化学式)。
(5)D分子中心原子的杂化方式是_______ ,由该中心原子组成的常见单质分子中包含_______ 个 键,与该单质分子互为等电子体的常见分子的结构式为
键,与该单质分子互为等电子体的常见分子的结构式为_______ 。
(1)A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小为
(2)A与HF相比,其熔、沸点较低,原因是
(3)B分子的空间构型为
(4)A、B两分子中心原子的氧化物对应的水化物酸性最强的是
(5)D分子中心原子的杂化方式是
 键,与该单质分子互为等电子体的常见分子的结构式为
键,与该单质分子互为等电子体的常见分子的结构式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ、由CO2、甲醇为原料合成绿色化学品碳酸二甲酯(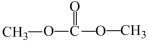 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
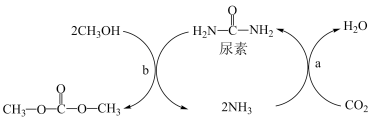
(1)下列说法不正确的是___________ (填字母)。
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是___________ 。
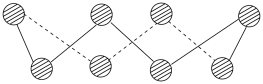
(3) 的电子式是
的电子式是___________ ,依据 理论推测
理论推测 的空间构型为
的空间构型为___________ ,常温下 是气体而
是气体而 是液体的原因是
是液体的原因是___________ 。
(4) 的键角
的键角___________  的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是___________ 。
(5) 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
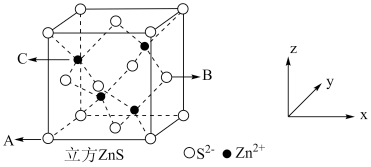
①已知A、B点的原子坐标分别为 和
和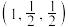 ,则C点的原子坐标为
,则C点的原子坐标为___________ ;
②若晶胞棱长为 ,密度为
,密度为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
(1)下列说法不正确的是
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.NH3极易溶解在水中,只因氨分子与水分子间形成了氢键
C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅱ、硫元素在化合物中常表现出多种化合价,它的许多化合物在研究和生产中有许多重要用途。回答下列问题:
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是

(3)
 的电子式是
的电子式是 理论推测
理论推测 的空间构型为
的空间构型为 是气体而
是气体而 是液体的原因是
是液体的原因是(4)
 的键角
的键角 的键角(填“大于”或“小于”),理由是
的键角(填“大于”或“小于”),理由是(5)
 在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方
在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方 晶体结构如图所示。
晶体结构如图所示。
①已知A、B点的原子坐标分别为
 和
和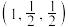 ,则C点的原子坐标为
,则C点的原子坐标为②若晶胞棱长为
 ,密度为
,密度为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素的符号是_____ ;
(2)Y元素原子的价层电子的轨道表示式为_______________ ,该元素的名称是_____ ;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为_____ ;
(4)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由________________________________________________________________________ .
(1)X元素的符号是
(2)Y元素原子的价层电子的轨道表示式为
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】四氟化硅、二氟甲烷(CH2F2)等含氟化合物在生产、生活中有重要的应用。回答下列问题:
(1)基态氟原子核外电子的空间运动状态有___________ 种,核外电子的最高能级符号为___________ ,最高能级电子的电子云形状为___________ 。
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为___________ 。
②N2F2结构式为___________ ,其分子中。σ键与π键的数目之比为___________ 。
(3)氢氟酸能腐蚀玻璃生成SiF4,SiF4中Si的杂化方式为___________ ,SiF4的空间构型为___________ 。
(4) CH2F2难溶于水,而三氟甲烷(CHF3)可溶于水,其可能的原因是___________ 。
(1)基态氟原子核外电子的空间运动状态有
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为
②N2F2结构式为
(3)氢氟酸能腐蚀玻璃生成SiF4,SiF4中Si的杂化方式为
(4) CH2F2难溶于水,而三氟甲烷(CHF3)可溶于水,其可能的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】结构决定性质,研究物质的组成、结构对于学习物质的性质至关重要。
(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是___________ 、___________ (写化学式),a比b的沸点高的原因是__________________________________ 。
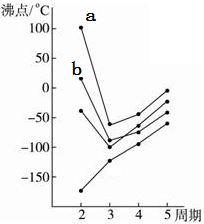
(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为__________ ,与石英相比该晶体的熔点、沸点________ (“更高”或“更低”),理由是_________________________________ 。
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:

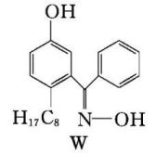
①M所含元素的电负性由大到小顺序为____ ,其中氮原子以__ 轨道与氧原子形成σ键。
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是___________________________________ 。
(4)常用 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为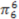 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为________ ,吡咯分子中N原子的杂化类型为 ________ ,1mol吡咯分子中所含的σ键数目为________ 。

(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是

(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:


①M所含元素的电负性由大到小顺序为
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是
(4)常用
 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为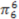 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
您最近一年使用:0次



