如图甲是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
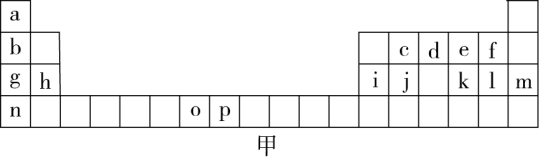
试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:___________ 。
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:____________ 。
(4)o、p两元素的部分电离能数据如表:
比较两元素的I2、I3可知,气态基态o2+再失去一个电子比基态气态p2+再失去一个电子难。对此,你的解释是___________ 。
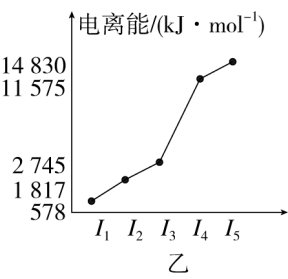
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是___________ (填元素符号)。

试回答下列问题。
(1)元素p为26号元素,请写出其基态原子的电子排布式:
(2)c、d、e、f四种元素的第一电离能由大到小的顺序为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据如表:
| 元素 | o | p | |
 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(5)图甲中的某主族元素的电离能情况如图乙所示,则该元素是

21-22高二·全国·单元测试 查看更多[1]
(已下线)第1章 章末综合测评A-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)
更新时间:2021-12-25 23:00:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W均为短周期元素且原子序数依次增大,元素Y和W同族。盐ZWX与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到含ZWX的溶液。根据以上信息,试判断下列问题:
(1)写出这四种元素的元素符号:X_____ 、Y_____ 、Z____ 、W____ ,并将这四种元素的原子按照半径由大到小的顺序排列______ (用具体的元素符号作答)
(2)Y的氢化物稳定性_________ W的氢化物稳定性(填“大于”或“小于”),Y的氢化物水溶液酸性_________ W的氢化物水溶液的酸性(填“大于”或“小于”)。
(3)写出Z2X2的电子式_____ ,该物质所含化学键的类型有_________ 。0.1 mol该物质与水反应转移电子数为______ 。
(1)写出这四种元素的元素符号:X
(2)Y的氢化物稳定性
(3)写出Z2X2的电子式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)这九种元素中,位于第三周期且原子半径最小元素的原子结构示意图_____________ 。
(2)④、⑤、⑧三种元素中,离子半径由大到小的顺序为__________ (填离子符号)。
(3)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是__________ (填化学式)。
⑧和⑨元素的气态氢化物稳定性顺序为_____________________ (填化学式)。
(4)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为____________________________ 。
(5)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式____________ 。
(6)元素⑤与元素④能形成原子个数比为1:1的化合物Y,Y在常温下为固态,焰色反应为黄色,Y与②的最高价氧化物反应的化学方程式为_____________ ,②的最高价氧化物的电子式___________ 。
(7)能说明⑧的非金属性比⑨的非金属性__________ (填“强”或“弱”)的事实是________ (用离子方程式说明)。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)④、⑤、⑧三种元素中,离子半径由大到小的顺序为
(3)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
⑧和⑨元素的气态氢化物稳定性顺序为
(4)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为
(5)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式
(6)元素⑤与元素④能形成原子个数比为1:1的化合物Y,Y在常温下为固态,焰色反应为黄色,Y与②的最高价氧化物反应的化学方程式为
(7)能说明⑧的非金属性比⑨的非金属性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分(短周期),其中每个数字序号代表一种元素。
请按要求回答下列问题:
(1)④⑤元素相比较,金属性最强的是___________ (填元素符号)。
(2)⑥元素的氢化物的稳定性___________ (填“>”或“<”)同一主族短周期元素的氢化物。
(3)②③的原子半径大小关系是:②___________ ③(填“>”“<”或“=”)。
(4)③④的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。
| 族 周期 | ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ |  | |||||||
| 3 | ④ | ⑤ | ⑥ |
(1)④⑤元素相比较,金属性最强的是
(2)⑥元素的氢化物的稳定性
(3)②③的原子半径大小关系是:②
(4)③④的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其所在周期序数相同;D原子的L层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L层中未成对电子数与D相同,但有空轨道;D与E同族。请回答下列问题:
(1)A与B、C、D、E元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为_______ ,其中心原子的杂化方式为_______ ;A分别与B、C、D形成的共价化合物中既含有极性键,又含有非极性键的是_______ (填化学式,任意写出三种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的是_______ (写两种即可);酸根离子呈三角锥形的是_______ 。
(3) 分子的空间结构为
分子的空间结构为_______ ;根据原子轨道重叠方式的不同,该分子中共价键的类型为_______ 。
(4)B的一种氢化物的相对分子质量是26,其分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
(1)A与B、C、D、E元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的是
(3)
 分子的空间结构为
分子的空间结构为(4)B的一种氢化物的相对分子质量是26,其分子中
 键与
键与 键的数目之比为
键的数目之比为
您最近一年使用:0次
【推荐2】R、W、X、Y、Z是原子序数依次增大的前四周期元素,其中R与W位于同一周期,且R元素的第一电离能大于氧,W的单质在暗处与 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
(1)基态Z原子的价层电子排布式为__________ ,该元素位于元素周期表中的__________ 区。
(2)基态R原子中有__________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为__________ 形。
(3)R、W、X三种元素中第一电离能由大到小的顺序为____ (用元素符号表示),原因是________ 。
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是__________ (填化学式)。
(5)X、Y两种元素组成的化合物 的电子式为
的电子式为__________ ,其中含有的化学键类型为__________ 。
 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:(1)基态Z原子的价层电子排布式为
(2)基态R原子中有
(3)R、W、X三种元素中第一电离能由大到小的顺序为
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是
(5)X、Y两种元素组成的化合物
 的电子式为
的电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,电子占据最高能层的符号为______ ,该能层上具有的原子轨道数为________ ,电子数为________ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?________ (填“是”或“否”),原因是_____________________________________________ (如果前一问填“是”,此问可以不答)。
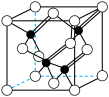
(3)镓与第ⅤA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子)。在GaAs晶体中,每个Ga原子与________ 个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为________ 。
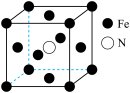
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________ ;设晶胞边长为a cm,阿伏加 德罗常数为NA,该晶体的密度为________ g·cm-3(用含a和NA的式子表示)。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,电子占据最高能层的符号为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?
(3)镓与第ⅤA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子)。在GaAs晶体中,每个Ga原子与

(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为

您最近一年使用:0次
【推荐1】回答下列问题
(1)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有___________ 种空间运动状态的电子,属于___________ 区(填“s”或“p”或“d”或“f”)
②LiBH4由Li+和 构成,与
构成,与 互为等电子体的分子为
互为等电子体的分子为___________ ,Li、Be、B元素的第一电离能由大到小排列顺序为___________ 。
③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是___________ (填元素符号)。
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(3)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电子数与Al相同的有___________ 。
(4)元素铋主要用于制造易熔金属合金,元素Bi位于第6周期VA族,其基态原子的价电子排布式为___________ 。Bi(NO3)3∙5H2O中各元素电负性从大到小的顺序为___________ 。
(1)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有
②LiBH4由Li+和
 构成,与
构成,与 互为等电子体的分子为
互为等电子体的分子为③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 |
| 580 | 1820 | 2750 | 11600 |
M是
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.[Ne]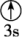 | B.[Ne]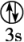 | C.[Ne] | D.[Ne]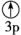 |
(4)元素铋主要用于制造易熔金属合金,元素Bi位于第6周期VA族,其基态原子的价电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】回答下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ 。
(2)①O2-、②Al3+、③Cl-、④Ca2+的半径由大到小排列为:___________ (用序号表示)。
(3)下列属于氧原子激发态的轨道表示式的有___________ (填字母)。
a.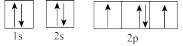 b.
b.
c.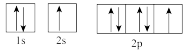 d.
d.
(4)Cu的价层电子排布式为___________ ,位于在周期表___________ 区(填s、p、d或ds)。
(5)基态Si原子中,电子占据的最高能层符号为___________ 。
(6)基态S原子的原子核外电子有___________ 种空间运动状态,其能量最高的电子电子云轮廓图为___________ 形。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①O2-、②Al3+、③Cl-、④Ca2+的半径由大到小排列为:
(3)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(4)Cu的价层电子排布式为
(5)基态Si原子中,电子占据的最高能层符号为
(6)基态S原子的原子核外电子有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表所示:
(1)X元素位于元素周期表的位置______ 。
(2)X、Y、Z三种元素的原子半径由小到大的排列顺序______ 。
(3)含Z元素的化合物在灼烧时火焰呈黄色。许多金属盐在灼烧时都会使火焰呈特征颜色,其原因是______ 。
(4)M的原子结构示意图为______ ,基态M原子的核外电子填充时最高能级符号为______ 。
(5)写出Q元素基态原子的价层电子排布图(即轨道表示式)______ 。
(6)写出基态 简化的电子排布式
简化的电子排布式______ ,基态 价层电子排布图(即轨道表示式)
价层电子排布图(即轨道表示式)______ 。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 位于第三周期,且原子半径是同周期主族元素中最大的 |
| M | 基态原子核外最外层所有p轨道为半充满状态 |
| Q | 基态原子核外最外层p轨道上有两个电子的自旋方向与最外层p轨道上其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级且d轨道上有6个电子 |
(2)X、Y、Z三种元素的原子半径由小到大的排列顺序
(3)含Z元素的化合物在灼烧时火焰呈黄色。许多金属盐在灼烧时都会使火焰呈特征颜色,其原因是
(4)M的原子结构示意图为
(5)写出Q元素基态原子的价层电子排布图(即轨道表示式)
(6)写出基态
 简化的电子排布式
简化的电子排布式 价层电子排布图(即轨道表示式)
价层电子排布图(即轨道表示式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】C、N化合物对人类生存环境有重要影响。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为_________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序为_________ 。
(3)键角:NH3__________ (填“>“<”或“=”)H2O;NH3的VSEPR模型为_________ 。
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为_________ 。
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为_________ (填元素符号),原因是_________ 。
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。_________ 。
②2号原子的坐标为_________ 。
③该晶体的密度为__________ g/cm3。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为
(2)C、N、O三种元素的第一电离能由小到大的顺序为
(3)键角:NH3
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。
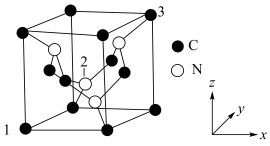
②2号原子的坐标为
③该晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、c、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氧化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24, ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)B、C、D的第一电离能由小到大的顺序为__________________ 。
(2)B的氢化物的分子空间构型是____________ ,其中心原子采取的杂化方式是________________ 。
(3)写出化合物AC2的电子式______________ ,一种由B、C组成的化合物与AC2互为等电子体,其化学式为_________ 。
(4)ECl3形成的配合物的化学式为______________________ 。
(1)B、C、D的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
(4)ECl3形成的配合物的化学式为
您最近一年使用:0次
【推荐3】第VIII族元素Fe、Co、Ni性质相似,称为铁系元素,主要用于制造合金。试回答下列问题:
(1)按照电子排布,可把元素周期表中的元素划分成五个区,VIII族元素位于周期表中_______ 区;写出基态Co原子的价层电子排布式_______ ;Co3+的半径_______ Fe2+的半径(填“大 于”或“小于”),第四电离能I4(Co)<I4(Fe)的原因是_______ 。
(2)写出与Ni同周期元素中,基态原子未成对电子数与Ni相同的主族元素名称_______ 。Ni与CO在60~80℃时反应生成Ni(CO)4气体,在Ni(CO)4中与Ni形成配位键的原子是_______ ,Ni(CO)4晶体类型是_______ 。确定Ni(CO)4固体为晶体的最可靠方法是_______ 。某同学画出基态碳原子的核外电子排布图: ,该电子排布图违背了
,该电子排布图违背了_______ 。
(3)Fe3+与酚类物质的显色反应常用于其离子检验,已知Fe3+遇邻苯二酚( )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是
)均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是_______ ;已知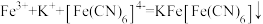 ,利用该离子方程式可以检验溶液中的Fe3+。
,利用该离子方程式可以检验溶液中的Fe3+。 中σ键、π键数目之比为
中σ键、π键数目之比为_______ 。
(4)某立方晶系的(Sb-Ni)合金用途广泛,下图为该合金的晶胞结构图:

①Ni和Sb原子数之比为_______ ;
②与Sb最邻近的Sb原子数为_______ 个。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,VIII族元素位于周期表中
(2)写出与Ni同周期元素中,基态原子未成对电子数与Ni相同的主族元素名称
 ,该电子排布图违背了
,该电子排布图违背了(3)Fe3+与酚类物质的显色反应常用于其离子检验,已知Fe3+遇邻苯二酚(
 )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是
)均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是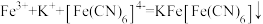 ,利用该离子方程式可以检验溶液中的Fe3+。
,利用该离子方程式可以检验溶液中的Fe3+。 中σ键、π键数目之比为
中σ键、π键数目之比为(4)某立方晶系的(Sb-Ni)合金用途广泛,下图为该合金的晶胞结构图:

①Ni和Sb原子数之比为
②与Sb最邻近的Sb原子数为
您最近一年使用:0次



