名校
1 . 科学家为社会发展做出了巨大贡献,下列研究成果与科学家对应关系不符的是
| A.门捷列夫发现了元素周期律,使化学的研究变得有规律可循 |
| B.屠呦呦为提取抗疟药青蒿素做出卓越贡献而获得诺贝尔奖 |
| C.侯德榜发明的侯氏制碱法推动了我国烧碱工业的发展 |
| D.道尔顿提出分子学说,使人们对物质结构的认识发展到一个新的阶段 |
您最近一年使用:0次
2021-11-01更新
|
152次组卷
|
2卷引用:山西省朔州市第一中学2021-2022学年高一上学期10月月考化学试题
名校
解题方法
2 . 碲在生产中用途广泛,常用作石油裂化的催化剂,电镀液的光亮剂、玻璃的着色材料等。元素周期表中碲元素的数据如图所示。下列说法正确的是
52 Te 碲 5s25p4 127.6 |
| A.碲元素在元素周期表中位于第五周期ⅣA族 |
| B.碲元素位于元素周期表d区 |
| C.碲原子5p能级有2个未成对电子 |
| D.碲原子核外电子的空间运动状态有52种 |
您最近一年使用:0次
2023-03-20更新
|
317次组卷
|
4卷引用:安徽省灵璧县第一中学2022-2023学年高二下学期3月月考化学试题
3 . C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
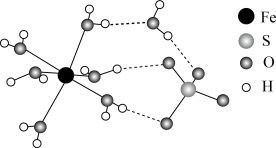
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
2023-04-20更新
|
187次组卷
|
2卷引用:山西省大同市2022-2023学年高二下学期期中考试化学试题
名校
4 . 运用元素周期律和元素周期表,可以系统研究元素的性质。回答下列问题:
(1)碱金属元素中,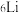 和
和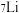 之间的关系是互为
之间的关系是互为_______ 。金属钾的氧化物有多种,其中过氧化钾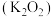 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是_______ ,根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
②硅和锗单质分别与 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是_______ (填“硅”或“锗”)。
(1)碱金属元素中,
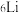 和
和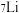 之间的关系是互为
之间的关系是互为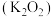 常作供氧剂,写出
常作供氧剂,写出 与
与 反应的化学方程式:
反应的化学方程式:(2)门捷列夫预言的“类硅”,后被发现,并命名为锗(Ge),周期表中排在硅的下一行。加上之前发现的碳(C)、铅(Pb)、锡(Sn),这一主族的元素趋于完善。
①锗在元素周期表中的位置是
②硅和锗单质分别与
 反应生成的氢化物更稳定的是
反应生成的氢化物更稳定的是
您最近一年使用:0次
5 . 摩擦剂是牙膏的主体成分,SiO2是一种常见的摩擦剂。
(1)Si在元素周期表中的位置是_____ 。
(2)根据用途推测SiO2在水中的溶解性:_____ (填“易溶”或“难溶”)。
(3)制备SiO2的方法如下:
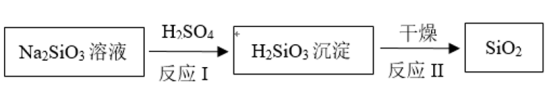
①写出反应I的离子方程式_____ 。
②比较酸性强弱:H2SO4_____ H2SiO3(填“>”或“<”)。
③结合原子结构解释②中酸性关系:Si和S电子层数相同,_____ 。
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。
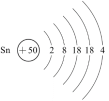
下列说法正确的是_____ (填序号)。
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
(1)Si在元素周期表中的位置是
(2)根据用途推测SiO2在水中的溶解性:
(3)制备SiO2的方法如下:

①写出反应I的离子方程式
②比较酸性强弱:H2SO4
③结合原子结构解释②中酸性关系:Si和S电子层数相同,
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF2)。锡的原子结构示意图如图。

下列说法正确的是
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
您最近一年使用:0次



