解题方法
1 . 某水性钠离子电池电极材料由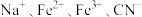 组成,其立方晶胞嵌入和嵌出
组成,其立方晶胞嵌入和嵌出 过程中,
过程中, 与
与 含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法正确的是
含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法正确的是
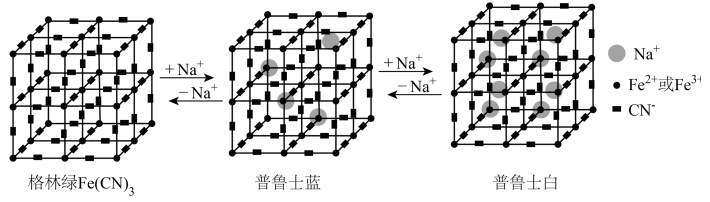
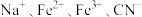 组成,其立方晶胞嵌入和嵌出
组成,其立方晶胞嵌入和嵌出 过程中,
过程中, 与
与 含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法正确的是
含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法正确的是
| A.铁在元素周期表中位于第4周期ⅧB族 |
| B.普鲁士蓝的导电能力大于普鲁士白 |
C.普鲁士蓝中 与 与 个数比为1∶2 个数比为1∶2 |
D.普鲁士白的化学式为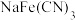 |
您最近一年使用:0次
解题方法
2 . 铁是一种重要的元素,在成人体中的含量达44~5g,铁的配合物在有机合成、催化等领域中发挥重要作用。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),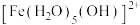 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。
(1)铁元素位于元素周期表的第___________ 周期第___________ 族。
(2) 中,中心离子为
中,中心离子为___________ ,配位原子是___________ ,配位数为___________ 。
(3)加入NaCl溶液后,溶液又变为黄色的原因:___________ (用离子方程式表示)。
Ⅱ. 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。
(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有___________ ;推测维生素C在水中的溶解性:___________ (填“难溶于水”或“易溶于水”)。
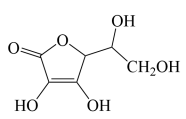
(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
②___________ 、___________ ;
③___________ 、___________ 、___________ 。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如
 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),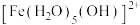 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。(1)铁元素位于元素周期表的第
(2)
 中,中心离子为
中,中心离子为(3)加入NaCl溶液后,溶液又变为黄色的原因:
Ⅱ.
 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有

(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
| 序号 | 结构特征 | 可反应的试剂 | 反应类型 |
| ① | 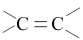 |  | 加成反应 |
| ② | 氧化反应 | ||
| ③ |
③
您最近一年使用:0次
解题方法
3 . A、B、C、D、E是原子序数依次增大的五种常见的短周期主族元素,E是地壳中含量最高的金属元素,B和E同主族。A、B、C、D四种元素形成的化合物[CA4]+[ BD4]-其结构如下图所示。下列说法正确的是


| A.元素A、D的原子最外层均有7个电子 |
| B.一个[CA4]+含有10个电子 |
| C.化合物BD3各原子最外层均达到8电子稳定结构 |
| D.E元素最高价氧化物对应的水化物是强碱 |
您最近一年使用:0次
4 . Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为______ ,基态Co原子的价层电子排布式为______ ,与Ni同周期且与Ni具有相同未成对电子数的元素有_______ 种。
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为____ 。Co(OH)3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:_____ 。
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。
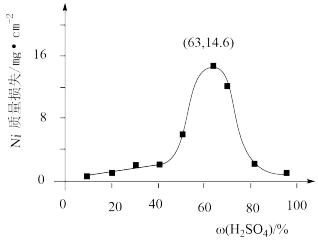
当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____ 。由于Ni与硫酸反应很慢,而与稀HNO3反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4,为了提高产物的纯度,在硫酸中添加HNO3的方式为_____ (填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为_____ 。
(1)Fe、Co、Ni在周期表中的位置为
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。

当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
您最近一年使用:0次
名校
5 . 下列关于元素周期表的说法正确的是
| A.地壳中含量最多的金属元素位于第四周期 |
| B.主族元素都是短周期元素 |
| C.最外层电子数相同的元素一定在同一族 |
| D.元素周期表有7个周期 |
您最近一年使用:0次
2022-07-28更新
|
110次组卷
|
2卷引用:陕西省西安市蓝田县2021~2022学年高一下学期期末质量检测化学试题
解题方法
6 . 已知a、b、c、d是元素周期表中前20号主族元素,其中a是地壳中含量最多的元素,b是元素周期表中非金属性最强的元素,c是短周期中原子半径最大的元素,d原子的N层电子数与K层电子数相等。下列说法正确的是
| A.a、b、c、d形成的简单离子都是10电子微粒 |
B.一定条件下,1molc单质与足量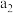 充分反应,转移电子数不一定是 充分反应,转移电子数不一定是 |
| C.与d元素同主族且位于下一周的元素原子序数为38 |
| D.b元素和d元素形成的化合物既含离子键又含共价键 |
您最近一年使用:0次
解题方法
7 . 化学和生活、社会发展息息相关。下列说法错误的是
| A.“嫦娥五号”返回舱携带的月壤中含有3He,He可以表示一种单质 |
| B.“奋斗者”号全海深载人潜水器的耐压壳使用了钛合金材料,钛合金属于金属材料 |
| C.由袁隆平团队研发的海水稻制成的大米中蛋白质的含量高于淀粉的含量 |
| D.我国“硅—石墨烯—锗晶体管”技术获得重大突破,C和Si都是短周期元素 |
您最近一年使用:0次
2021-10-12更新
|
194次组卷
|
4卷引用:湖北省京山市、安陆市等百校联考2022届高三月考化学试题
湖北省京山市、安陆市等百校联考2022届高三月考化学试题河北省邢台市“五岳联盟”2021-2022学年高三上学期10月联考化学试题重庆市缙云教育联盟2021-2022学年高一上学期期末考试化学试题(已下线)卷01 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
8 . 元素周期表在指导科学研究和生产实践方面具有十分重要的意义,请将下表中A、B两栏描述的内容对应起来。
| A | B | A | B |
| ①制半导体的元素 | (a)ⅣB至ⅥB的过渡元素 | ① | |
| ②制催化剂的元素 | (b)F、Cl、Br、N、S“三角地带” | ② | |
| ③制耐高温材料的元素 | (c)金属与非金属元素分界线附近 | ③ | |
| ④制制冷剂的元素 | (d)相对原子质量较小的元素 | ④ | |
| ⑤地壳中含量较多的元素 | (e)过渡元素 | ⑤ |
您最近一年使用:0次
9 . 2009年3月1日16时13分10秒,“嫦娥一号”卫星在北京航天飞机控制中心科技人员的精确控制下,准确落于月球东经52.36°、南纬1.50°的预定撞击点。“嫦娥一号”担负的四大科学目标之一是探测下列14种元素的含量和分布情况:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其中属于主族元素的有( )
| A.4种 | B.5种 |
| C.6种 | D.7种 |
您最近一年使用:0次
名校
10 . 已知X为地壳中含量最高的元素,则X在元素周期表中的位置是
| A.第一周期ⅠA族 | B.第二周期ⅣA族 |
| C.第二周期ⅥA族 | D.第三周期ⅣA族 |
您最近一年使用:0次



