名校
1 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_____ 与盐酸反应最剧烈,____ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl____ S(填“>”或“<”),反应的离子方程式为_______ 。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。
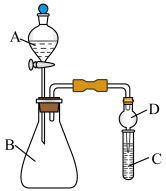
(3)仪器A的名称为___________ ,干燥管D的作用为___________________ 。
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为___________ ,观察到C中溶液____________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_________ 溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液________ (填现象),即可证明。但有的同学认为盐酸具有挥发性,HCl可进入C中干扰实验,应在两装置间添加装有 _________ 溶液的洗气瓶除去。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液
您最近一年使用:0次
2019-03-29更新
|
322次组卷
|
8卷引用:山西省长治二中2018-2019学年高一下学期第一次月考化学试题
2 . 为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将外观相近的钠、钾、镁、铝各1克分别投入到足量的同浓度的盐酸中,试预测实验结果:__ 与盐酸反应最剧烈,___ 与盐酸反应的速度最慢;__ 与盐酸反应产生的气体最多。
(2)向H2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______
Ⅱ.利用下图装置可验证同主族元素非金属性的变化规律________
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液_____ (填现象),即可证明
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中_______ (填现象),即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有_______ 溶液的洗气瓶除去
Ⅰ.(1)将外观相近的钠、钾、镁、铝各1克分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向H2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
Ⅱ.利用下图装置可验证同主族元素非金属性的变化规律
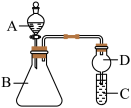
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中
您最近一年使用:0次
2019-05-07更新
|
131次组卷
|
2卷引用:【校级联考】河南省开封市、商丘市九校2018-2019学年高一下学期期中联考化学试题
3 . 某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
通过实验验证三种元素金属性由强到弱是_____ ,则下列判断正确的是( )
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是_______ (填选项),化学反应方程式是_________ 。
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为______ (填选项)。
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液_______ 的现象,即可证明。用原子结构理论解释非金属性Cl>I的原因:同主族元素从上到下,________________ 。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
| 实验内容 | 实验现象 |
| 1、各取1.0g金属X和金属Z,分别加入到5mL水中 | 金属X与水反应比金属Z剧烈 |
| 2、各取1.0g的金属Z和金属Y(形状相同),分别加入到5mL1.0mol/L盐酸中。 | 金属Z与盐酸反应比金属Y剧烈 |
A.原子序数:Y>Z>X B.原子的最外层电子数X>Y>Z
C.原子半径:Y>Z>X D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:

(1)装置A中盛放的试剂是
A.Na2SO3溶液 B.Na2S溶液 C.Na2SO4溶液
(2)下列不能用于验证氯元素比硫元素非金属性强的依据为
A.HCl比H2S稳定
B.HClO氧化性比H2SO4强
C.HClO4酸性比H2SO4强
D.铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(3)若要验证非金属性:Cl>I,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液
您最近一年使用:0次
2019-06-10更新
|
1163次组卷
|
5卷引用:第1章原子结构与元素周期律 拓展区 综合拓展
名校
4 . 某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,________ 与盐酸反应的速度最慢;________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________ 。
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是________________ 。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________ 。
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:___________________ 。
(2)验证氯气的氧化性强于碘的实验现象是________________________ 。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是__________________________ 。
(4)为验证溴的氧化性强于碘,过程④的操作和现象是___________ ,___________ 。
(5)过程③实验的目的是____________________ 。
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:_______________ 。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:
(2)验证氯气的氧化性强于碘的实验现象是
(3)B、C管口“浸有NaOH溶液的棉花”的作用是
(4)为验证溴的氧化性强于碘,过程④的操作和现象是
(5)过程③实验的目的是
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:
您最近一年使用:0次
2017-05-18更新
|
287次组卷
|
6卷引用:广东省广州市第二中学2016-2017学年高二下学期期中考试化学试题
广东省广州市第二中学2016-2017学年高二下学期期中考试化学试题河北省衡水中学滁州分校2017-2018学年高一下学期第一次月考化学试题河北省衡水市阜城中学2020-2021学年高二上学期开学考试化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)练习14 元素周期律和元素周期表-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)湖南省衡阳市第八中学2016-2017学年高一理科实验班下学期结业(期末)理综化学试题



