1 . 如下图所示是氯气的制备以及氯、溴、碘的非金属性比较实验,充分反应一段时间后,打开装置D的活塞,将装置D中少量溶液加入装置E中,振荡,观察实验现象,下列说法正确的是
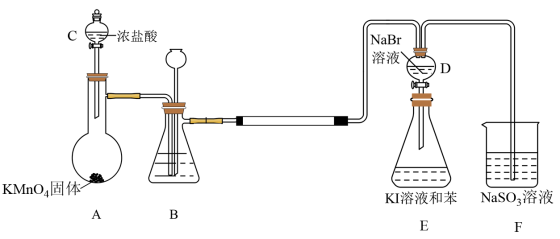

| A.F装置中的Na2SO3溶液能吸收Cl2,进行尾气处理 |
| B.装置B中可盛放水吸收氯气中的HCl气体 |
| C.装置E下层呈现紫红色 |
| D.装置E中有机试剂层呈现紫红色,能说明非金属性:Br>I |
您最近一年使用:0次
2 . 两个化学兴趣小组拟通过实验探究同主族元素性质的递变规律。
Ⅰ.第一小组同学探究元素Cl、Br、I的非金属性强弱,设计的实验方案如下:
(1)补充下列实验报告中的实验现象和离子方程式
(2)【评价】该小组设计的实验方案是____________ (填“合理”或“不合理”)
(3)【补充和完善】上一题(2)中若选合理,则此项不用再作答,若选不合理,则合理完成实验还需要的试剂是______
Ⅱ.第二小组同学探究元素C、Si的非金属性强弱,设计的实验方案如下:

(4)干燥管D的作用为_______
(5)该小组同学用盐酸、CaCO3和Na2SiO3溶液,按图装置进行试验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性C>Si。但乙同学认为此方案不合理,理由___ ,
改进措施:在B、C两装置之间接一个盛有______ 溶液的洗气瓶。
Ⅰ.第一小组同学探究元素Cl、Br、I的非金属性强弱,设计的实验方案如下:
(1)补充下列实验报告中的实验现象和离子方程式
| 实验步骤 | 实验现象 | 实验结论及离子方程式 |
 | 甲溶液由无色变成橙色 乙 | 离子方程式 甲 乙Cl2+2I-=2Cl-+I2 结论:卤素单质的氧化性由强到弱的顺序为Cl2>Br2>I2 |
(3)【补充和完善】上一题(2)中若选合理,则此项不用再作答,若选不合理,则合理完成实验还需要的试剂是
Ⅱ.第二小组同学探究元素C、Si的非金属性强弱,设计的实验方案如下:

(4)干燥管D的作用为
(5)该小组同学用盐酸、CaCO3和Na2SiO3溶液,按图装置进行试验,观察到试管C中溶液有白色沉淀生成,甲同学认为非金属性C>Si。但乙同学认为此方案不合理,理由
改进措施:在B、C两装置之间接一个盛有
您最近一年使用:0次
解题方法
3 . 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。

(1)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理,请说明理由?___________ 。
(2)根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。利用装置图1一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究。
①实验中A选用的物质名称为___________ ,B中为碳酸钙固体,C选用的物质名称为___________ ;
②装置B中出现的现象为___________ 。
③但有同学认为该装置有缺陷,如何改进?___________ 。
(3)继续利用装置图1证明非金属性氯大于硫,选择合适药品设计实验验证。实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,选择合适药品设计实验验证氯的非金属性大于硫:装置B中所装药品为KMnO4,装置B中发生反应的化学方程式为___________ , 装置C中的实验现象为有淡黄色沉淀生成,离子方程式为___________ 。

(1)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理,请说明理由?
(2)根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。利用装置图1一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究。
①实验中A选用的物质名称为
②装置B中出现的现象为
③但有同学认为该装置有缺陷,如何改进?
(3)继续利用装置图1证明非金属性氯大于硫,选择合适药品设计实验验证。实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,选择合适药品设计实验验证氯的非金属性大于硫:装置B中所装药品为KMnO4,装置B中发生反应的化学方程式为
您最近一年使用:0次
2021-05-11更新
|
140次组卷
|
2卷引用:江西省南昌市新建一中2020-2021学年高一下学期第一次月考化学试题
4 . 某校化学兴趣小组同学为探究元素周期律,设计了如下一系列实验。
Ⅰ.(1)将物质的量均为1 mol的钠、钾、镁、铝分别投入足量的0.1 mol/L的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,________ 与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合,反应生成NH3·H2O,从而验证NaOH的碱性强于NH3·H2O的碱性,继而可以验证Na的金属性强于N的金属性,你认为此设计是否合理,并说明理由_______ 。
Ⅱ.利用如所示装置可以验证元素的非金属性的变化规律。______ ,D的作用是__________ 。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为_________ 、_________ 、_________ ,装置C中的实验现象为有淡黄色沉淀生成,则反应的离子方程式为___________ 。
(5)若要证明非金属性C>Si,则A中应加入________ 溶液,B中应加入Na2CO3,C中应加入______ 溶液,装置C中的现象为________ 。
Ⅰ.(1)将物质的量均为1 mol的钠、钾、镁、铝分别投入足量的0.1 mol/L的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合,反应生成NH3·H2O,从而验证NaOH的碱性强于NH3·H2O的碱性,继而可以验证Na的金属性强于N的金属性,你认为此设计是否合理,并说明理由
Ⅱ.利用如所示装置可以验证元素的非金属性的变化规律。
已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
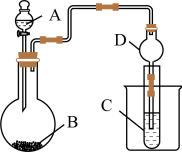
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为
(5)若要证明非金属性C>Si,则A中应加入
您最近一年使用:0次
2020-09-24更新
|
685次组卷
|
3卷引用:鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律章末综合检测卷
5 . 某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。甲同学取钠、镁、锡各1 mol分别投入到足量的盐酸中,预测实验结果。
(1)甲同学设计实验的目的是______ 。
(2)与盐酸反应最剧烈的是______ 。
(3)利用如图所示装置可以验证非金属性的变化规律。

①仪器A的名称为______ ,干燥管D的作用是______ 。
②实验室中现有药品: 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为______ 、______ 、______ ,装置C中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______ 。
③若要证明非金属性: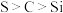 ,则A中加
,则A中加______ ,B中加 ,C中加
,C中加______ ,观察到C中的现象为______ 。
(1)甲同学设计实验的目的是
(2)与盐酸反应最剧烈的是
(3)利用如图所示装置可以验证非金属性的变化规律。

①仪器A的名称为
②实验室中现有药品:
 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为③若要证明非金属性:
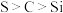 ,则A中加
,则A中加 ,C中加
,C中加
您最近一年使用:0次
解题方法
6 . 用如图所示装置进行下列实验,a、b和c中所装试剂如下表所示,其中实验现象与结论对应关系不正确的是一组是


| 选项 | a | b | c | 现象 | 结论 |
| A | 饱和食盐水 | 碳化钙 | 酸性 溶液 溶液 | c中溶液紫色褪去 | 乙炔具有还原性 |
| B | 浓盐酸 |  固体 固体 | NaBr溶液 | c中溶液由无色变橙色 |  的氧化性比 的氧化性比 强 强 |
| C | 稀盐酸 | 大理石 |  溶液 溶液 | c中有白色胶状沉淀生成 | 碳酸的酸性比硅酸强 |
| D | 硫酸 |  固体 固体 | 品红溶液 | c中溶液红色褪去 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后 层溶液变为紫红色。
层溶液变为紫红色。
请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______ 。
(2)验证氯气的氧化性强于碘的实验现象是______ 。
(3)B和C仪器口放置浸有 溶液的棉花的作用是
溶液的棉花的作用是______ 。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______ (填“减弱”或“增强”)。

实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后
 层溶液变为紫红色。
层溶液变为紫红色。请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为
(2)验证氯气的氧化性强于碘的实验现象是
(3)B和C仪器口放置浸有
 溶液的棉花的作用是
溶液的棉花的作用是(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐
您最近一年使用:0次
2020-03-02更新
|
744次组卷
|
5卷引用:第一节 元素周期表 课时2 元素的性质与原子结构
名校
解题方法
8 . 某化学兴趣小组为探究元素性质的递变规律,设计以下实验。
Ⅰ.(1)将钠、钾、镁、铝各1 分别投入足量的0.1
分别投入足量的0.1 的盐酸中,试预测实验结果:
的盐酸中,试预测实验结果:______ 与盐酸反应最剧烈,______ 与盐酸反应最慢。
(2)将 溶液与
溶液与 溶液混合生成
溶液混合生成 ,从而验证
,从而验证 的碱性强于
的碱性强于 ,继而可以验证
,继而可以验证 的金属性强于
的金属性强于 。此设计
。此设计______ (填“合理”或“不合理”),理由是________________________ 。
Ⅱ.利用如图所示装置可以验证非金属性的变化规律。

(3)仪器 的名称为
的名称为____________ ,干燥管 的作用是
的作用是__________________ 。
(4)实验室中现有药品: 溶液、
溶液、 浓盐酸、
浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置 、
、 、
、 中所装药品分别为
中所装药品分别为____________ 、____________ 、____________ ,装置 中的实验现象为有黄色沉淀生成,相关反应的离子方程式为
中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______________________________________ 。
(5)若要证明非金属性: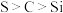 ,则
,则 中加
中加__________ , 中加
中加 ,
, 中加
中加__________ ,观察到 中的现象为
中的现象为______________________________ 。
Ⅰ.(1)将钠、钾、镁、铝各1
 分别投入足量的0.1
分别投入足量的0.1 的盐酸中,试预测实验结果:
的盐酸中,试预测实验结果:(2)将
 溶液与
溶液与 溶液混合生成
溶液混合生成 ,从而验证
,从而验证 的碱性强于
的碱性强于 ,继而可以验证
,继而可以验证 的金属性强于
的金属性强于 。此设计
。此设计Ⅱ.利用如图所示装置可以验证非金属性的变化规律。

(3)仪器
 的名称为
的名称为 的作用是
的作用是(4)实验室中现有药品:
 溶液、
溶液、 浓盐酸、
浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置 、
、 、
、 中所装药品分别为
中所装药品分别为 中的实验现象为有黄色沉淀生成,相关反应的离子方程式为
中的实验现象为有黄色沉淀生成,相关反应的离子方程式为(5)若要证明非金属性:
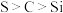 ,则
,则 中加
中加 中加
中加 ,
, 中加
中加 中的现象为
中的现象为
您最近一年使用:0次
2020-03-02更新
|
164次组卷
|
14卷引用:2015-2016学年安徽省合肥中科大附中高一下期中化学试卷
2015-2016学年安徽省合肥中科大附中高一下期中化学试卷山西省朔州市怀仁县第一中学2018-2019学年高一下学期第三次月考化学试题2019-2020学年人教版高中化学高考基础复习专题5《物质结构 元素周期律》测试卷2020届人教版高中化学高三专题基础复习专题5《物质结构 元素周期律》测试卷第1章原子结构与元素周期律第3节课时2 预测同主族元素的性质山西省晋中市和诚中学2019-2020学年高一4月月考化学试题(已下线)4.2.1 元素性质的周期性变化规律(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)四川省成都市蒲江县蒲江中学2019-2020学年高一4月月考化学试题2014-2015浙江省余姚中学高一4月月考化学试卷2014-2015浙江省严州中学高一4月阶段性测试化学试卷山西省应县第一中学校2018-2019学年高一下学期期中考试化学试题云南省弥勒市第二中学2019-2020学年高二上学期开学考试化学试题安徽省庐巢七校联盟2020届高三第五次联考化学试题福建省仙游县郊尾中学2020届高三上学期期中考试化学试题
9 . 利用如图装置来验证同主族元素非金属性的变化规律。

要证明非金属性:Cl>I,在A中加入浓盐酸,B中加入KMnO4(KMnO4与浓盐酸在常温下反应生成氯气),C中加入___ 溶液,观察到C中___ (填实验现象),即可证明。干燥管D的作用是___ 。从环境保护的角度考虑,此装置尚缺少尾气处理装置,可用___ 溶液吸收尾气。

要证明非金属性:Cl>I,在A中加入浓盐酸,B中加入KMnO4(KMnO4与浓盐酸在常温下反应生成氯气),C中加入
您最近一年使用:0次
解题方法
10 . 利用如图装置可验证同主族元素非金属性的变化规律。

(1)仪器A的名称为______ ,干燥管D的作用为______ 。
(2)若要证明非金属性: ,C中为淀粉
,C中为淀粉 碘化钾混合溶液,B中装有
碘化钾混合溶液,B中装有 固体,则A中试剂为
固体,则A中试剂为______ ,观察到C中溶液______  填现象
填现象 ,即可证明。从环境保护的观点考虑,此装置缺点
,即可证明。从环境保护的观点考虑,此装置缺点______ 。
(3)若要证明非金属性: ,则在A中
,则在A中______ B中加______ 、C中加______ ,写出C中反应的化学方程式______

(1)仪器A的名称为
(2)若要证明非金属性:
 ,C中为淀粉
,C中为淀粉 碘化钾混合溶液,B中装有
碘化钾混合溶液,B中装有 固体,则A中试剂为
固体,则A中试剂为 填现象
填现象 ,即可证明。从环境保护的观点考虑,此装置缺点
,即可证明。从环境保护的观点考虑,此装置缺点(3)若要证明非金属性:
 ,则在A中
,则在A中
您最近一年使用:0次



