1 . 某研究性学习小组设计了一组实验验证元素周期律。
I.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的:验证同一主族,从上到下金属元素原子失电子能力逐渐增强;同一周期主族元素从左到右金属元素原子失电子能力逐渐_______ 。
(2)烧杯中反应最剧烈的金属是_______(填字母)。
(3)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_______(填字母)。
II.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题。
(4)实验装置:
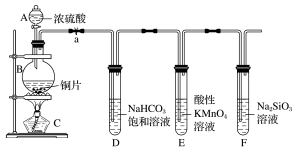
仪器B的名称为_______ 。
(5)实验步骤:连接仪器、_______ 、加药品,打开a,然后滴入浓硫酸,加热。
(6)问题探究:(已知酸性亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是_______ ;装置E中酸性KMnO4溶液的作用是_______ 。
②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是_______ ;试管F中发生反应的离子方程式为_______ 。
③依据试管D中的反应,能否证明S的非金属性强于C的非金属性?_______ (填“能”或“否”)。说明理由_______ 。
I.甲同学在a、b、c、d四只烧杯中分别加入50 mL冷水,再各滴加几滴酚酞试液,依次加入大小相同的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的:验证同一主族,从上到下金属元素原子失电子能力逐渐增强;同一周期主族元素从左到右金属元素原子失电子能力逐渐
(2)烧杯中反应最剧烈的金属是_______(填字母)。
| A.钠 | B.镁 | C.铝 | D.钾 |
| A.把镁、铝的金属块换成金属粉末 | B.把烧杯中的冷水换成热水 |
| C.把烧杯中的冷水换成等量的同浓度的盐酸 | D.把烧杯中的冷水换成氢氧化钠溶液 |
II.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题。
(4)实验装置:

仪器B的名称为
(5)实验步骤:连接仪器、
(6)问题探究:(已知酸性亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是
②能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
③依据试管D中的反应,能否证明S的非金属性强于C的非金属性?
您最近半年使用:0次
解题方法
2 . 某化学研究性学习小组为学习了元素性质后,分别设计了如下实验:
(1)甲同学想探究“铝热反应”中熔融物的成分,他查阅《化学手册》得到Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
①由此甲同学推测,教材中铝热反应所得到的熔融物应是铁铝合金。其理由是:_______________ 。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝,该实验所用试剂是___ ,反应的离子方程式为_____ 。
③甲同学为确定熔融物中是否还会有残留的Fe2O3,将熔融物用酸完全溶解后加入KSCN试剂。请你分析该设计是否正确___ (填“正确”或“不正确”),理由是(用离子方程式表示)______________________ 。
(2) 乙同学设计了如下图装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。乙同学可能观察到的现象有_______ 。 从环保角度考虑,该装置有明显不足,请提出改进建议_____________________ 。
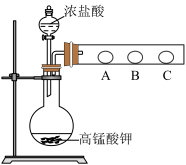
(3) 丙同学欲比较N、C、Si的非金属性强弱,设计了下图所示的实验装置,其设计能否达到实验目的______ (填“能”或“不能”),理由是______________ 。

(1)甲同学想探究“铝热反应”中熔融物的成分,他查阅《化学手册》得到Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | …… |
①由此甲同学推测,教材中铝热反应所得到的熔融物应是铁铝合金。其理由是:
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝,该实验所用试剂是
③甲同学为确定熔融物中是否还会有残留的Fe2O3,将熔融物用酸完全溶解后加入KSCN试剂。请你分析该设计是否正确
(2) 乙同学设计了如下图装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。乙同学可能观察到的现象有

(3) 丙同学欲比较N、C、Si的非金属性强弱,设计了下图所示的实验装置,其设计能否达到实验目的

您最近半年使用:0次
名校
解题方法
3 . 根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
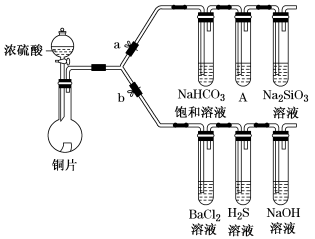
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、________ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______ 。装置A中试剂是_______ 。
③ 能说明碳的非金属性比硅强的实验现象是_________ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____ 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_________ 。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、
② 铜与浓硫酸反应的化学方程式是
③ 能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近半年使用:0次
4 . 如图是实验室制备氯气并进行一系列性质探究的实验装置(夹持及加热仪器已省略)。
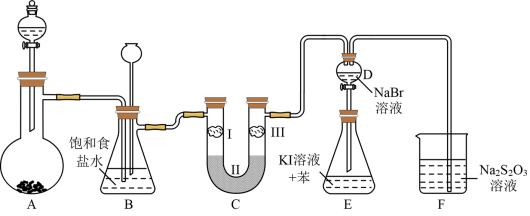
(1)用二氧化锰和浓盐酸制备氯气,则反应的离子方程式为:_____ 。
(2)实验装置B的作用之一是除去氯气中的杂质氯化氢,作用之二是起安全瓶的作用,当长颈漏斗中液面上升时,说明_____ ,此时应停止实验。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中II可放入_____ (填编号)。
(4)写出装置F中相应的离子反应方程式:_____ 。
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性,有人认为该设计不能达到实验目的,其理由是_____ ,某兴趣小组的同学思考后将上述D、E、F装置改为如图装置替代。
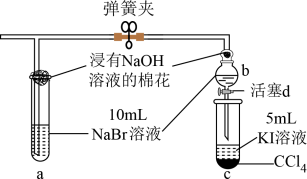
已知当溴水浓度较小时,溶液颜色与氯水相似也呈黄色。
实验操作步骤如下:
I.打开弹簧夹,缓缓通入氯气;
II.当a和b中的溶液都变为黄色时,夹紧弹簧夹;
III.当a中溶液由黄色变为棕色时,停止通氯气;
IV._____。
①设计步骤III的实验思想是_____ 。
②步骤IV的操作是_____ 。

(1)用二氧化锰和浓盐酸制备氯气,则反应的离子方程式为:
(2)实验装置B的作用之一是除去氯气中的杂质氯化氢,作用之二是起安全瓶的作用,当长颈漏斗中液面上升时,说明
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中II可放入
| A.碱石灰 | B.硅胶 | C.浓硫酸 | D.无水氯化钙 |
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性,有人认为该设计不能达到实验目的,其理由是

已知当溴水浓度较小时,溶液颜色与氯水相似也呈黄色。
实验操作步骤如下:
I.打开弹簧夹,缓缓通入氯气;
II.当a和b中的溶液都变为黄色时,夹紧弹簧夹;
III.当a中溶液由黄色变为棕色时,停止通氯气;
IV._____。
①设计步骤III的实验思想是
②步骤IV的操作是
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
5 . 下列装置能达到相应实验目的的是


| A.装置Ⅰ可用于除去苯中的溴 | B.装置Ⅱ可用于配制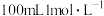 的稀硫酸 的稀硫酸 |
| C.装置Ⅲ可用于实验室制备少量氧气 | D.装置Ⅳ可用于滴定盐酸 |
您最近半年使用:0次
名校
解题方法
6 . 某兴趣小组拟制备氯气及验证其性质并比较氯、溴、碘的非金属性强弱。
Ⅰ[查阅资料]①当溴水浓度较小时,溶液颜色与氯水相似,也呈黄色。
②硫代硫酸钠溶液在工业上可作脱氯剂。
Ⅱ[性质验证]实验装置如图所示(夹持装置省略)
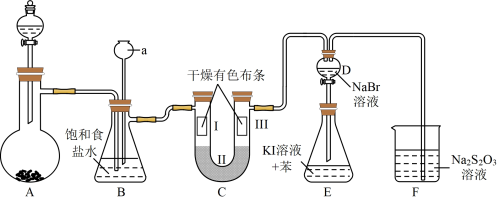
实验步骤;
(1)检查装置的气密性,按图示加入试剂。仪器a的名称是__________ ;
装置C中Ⅱ处加入的试剂可以是_____ (填字母)。
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
(2)装置B的作用为___________________________________ 。
(3)KI的电子式为_____ ;硫代硫酸钠中所含的化学键类型为_______________ ;写出装置F中反应的离子方程式____________________ ( 中的S元素被氧化成最高价)。
中的S元素被氧化成最高价)。
Ⅲ[探究与反思]
(4)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性强弱,有同学认为该设计不能达到实验目的,其理由是________________________________________ 。该组同学思考后将上述D、E、F装置改为下图装置,实验操作步骤如下:
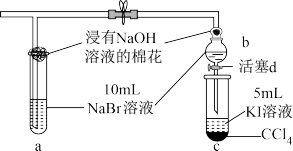
①打开弹簧夹,缓缓通入氯气。
②当a和b中的溶液都变为黄色时,夹紧弹簧夹。
③当a中溶液由黄色变为棕色时,停止通氯气。
④……
(5)步骤④的操作是________________________________________________ 。
Ⅰ[查阅资料]①当溴水浓度较小时,溶液颜色与氯水相似,也呈黄色。
②硫代硫酸钠溶液在工业上可作脱氯剂。
Ⅱ[性质验证]实验装置如图所示(夹持装置省略)

实验步骤;
(1)检查装置的气密性,按图示加入试剂。仪器a的名称是
装置C中Ⅱ处加入的试剂可以是
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
(2)装置B的作用为
(3)KI的电子式为
 中的S元素被氧化成最高价)。
中的S元素被氧化成最高价)。Ⅲ[探究与反思]
(4)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性强弱,有同学认为该设计不能达到实验目的,其理由是

①打开弹簧夹,缓缓通入氯气。
②当a和b中的溶液都变为黄色时,夹紧弹簧夹。
③当a中溶液由黄色变为棕色时,停止通氯气。
④……
(5)步骤④的操作是
您最近半年使用:0次
解题方法
7 . 用下列装置进行实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 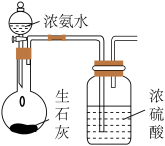 | 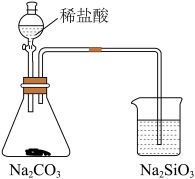 | 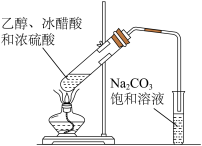 | 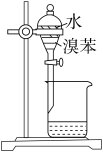 |
| 目的 | 制备干燥的氨气 | 证明非金属性 Cl>C>Si | 制备乙酸乙酯 | 分离出溴苯 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
14-15高三上·浙江杭州·阶段练习
解题方法
8 . 根据要求完成下列各小题实验目的。(a、b 为弹簧夹,加热及固定装置已略去)
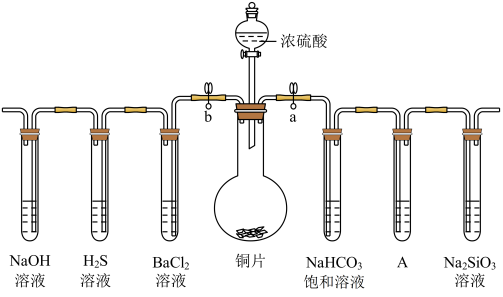
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸 >碳酸)
①连接仪器、___________ 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是__________________ ,装置A中的试剂是___________ 。
③能说明碳的非金属性比硅强的实验现象是:_______________________ 。
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性。
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是:___________ 。
②若大量的SO2通入NaOH溶液中,其化学方程式是:__________________ 。
③BaCl2溶液中无沉淀现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性并生成沉淀的离子方程式___________________ 。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸 >碳酸)
①连接仪器、
②铜与浓硫酸反应的化学方程式是
③能说明碳的非金属性比硅强的实验现象是:
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性。
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是:
②若大量的SO2通入NaOH溶液中,其化学方程式是:
③BaCl2溶液中无沉淀现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯 水 | 氨 水 |
| 沉淀的化学式 |
您最近半年使用:0次
名校
解题方法
9 . 某研究小组利用下图所示装置制备氯气并进行卤素性质的探究。
Ⅰ.制备 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略) 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为________ 。
(2)B中发生反应的离子方程式为________ 。
(3)反应一段时间后,取一支试管,加入2mLC中的橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论: 的氧化性强于
的氧化性强于 。理由
。理由________ 。
Ⅱ.研究小组为了进一步验证 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:
(4)同学甲认为实验i的现象说明溴水能将 氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将
氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将 氧化”的结论不严谨,原因为
氧化”的结论不严谨,原因为________ ,同学乙补充了实验方案,证明了“溴水能将 氧化”。同学乙补充的实验方案是
氧化”。同学乙补充的实验方案是________ 。
(5)分析实验ii及上述实验,判断 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为________ 。
(6)从“位置—结构—性质”的角度解释 、
、 、
、 氧化性逐渐减弱的原因
氧化性逐渐减弱的原因________ 。
Ⅰ.制备
 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略)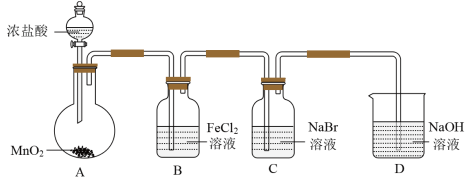
 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为(2)B中发生反应的离子方程式为
(3)反应一段时间后,取一支试管,加入2mLC中的橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论:
 的氧化性强于
的氧化性强于 。理由
。理由Ⅱ.研究小组为了进一步验证
 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:实验 | 操作 | 现象 |
i | 先向试管中加入2mL新制 溶液,滴加少量溴水,振荡 溶液,滴加少量溴水,振荡 | 溶液为黄色 |
ii | 先向试管中加入2mL新制 溶液和0.5mL苯(有机溶剂,不溶于水,浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 溶液和0.5mL苯(有机溶剂,不溶于水,浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 | 下层溶液为黄色 |
| 再滴加0.5mLKSCN溶液于下层溶液中 | 无红色出现 |
(4)同学甲认为实验i的现象说明溴水能将
 氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将
氧化:同学乙认为仅从“溶液为黄色”得出“溴水能将 氧化”的结论不严谨,原因为
氧化”的结论不严谨,原因为 氧化”。同学乙补充的实验方案是
氧化”。同学乙补充的实验方案是(5)分析实验ii及上述实验,判断
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(6)从“位置—结构—性质”的角度解释
 、
、 、
、 氧化性逐渐减弱的原因
氧化性逐渐减弱的原因
您最近半年使用:0次
名校
10 . 摩擦剂是牙膏的主体成分, 是一种常见的摩擦剂.
是一种常见的摩擦剂.
(1) 在元素周期表中的位置是
在元素周期表中的位置是_____________ .
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_____________ (填“易溶”或“难溶”).
(3)制备 的方法如下:
的方法如下:

①写出反应Ⅰ的离子方程式________________________ .
②比较酸性强弱:
_____________  (填“>”或“<”).
(填“>”或“<”).
③结合原子结构解释②中酸性关系: 和S电子层数相同,
和S电子层数相同,__________________________ .
(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡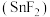 .
.
已知锡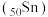 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是_____________ (填序号).
a. 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大
c. 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸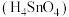 的酸性强于硅酸
的酸性强于硅酸
(5)工业上可以用木炭还原 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:_____________ ;该反应能否验证 和C的非金属性强弱?
和C的非金属性强弱?_____________ (填“能”、“不能”)
(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?_____________ (填“同意”、“不同意”);
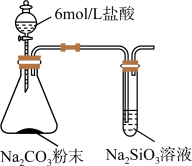
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案._____________
 是一种常见的摩擦剂.
是一种常见的摩擦剂.(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)根据用途推测
 在水中的溶解性:
在水中的溶解性:(3)制备
 的方法如下:
的方法如下:
①写出反应Ⅰ的离子方程式
②比较酸性强弱:

 (填“>”或“<”).
(填“>”或“<”).③结合原子结构解释②中酸性关系:
 和S电子层数相同,
和S电子层数相同,(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡
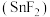 .
.已知锡
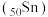 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是a.
 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大c.
 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸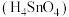 的酸性强于硅酸
的酸性强于硅酸(5)工业上可以用木炭还原
 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为: 和C的非金属性强弱?
和C的非金属性强弱?(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与
 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案.
您最近半年使用:0次



