解题方法
1 . 某元素的原子结构示意图为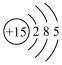 。下列关于该元素的说法中,
。下列关于该元素的说法中,
| A.元素符号是P | B.属于短周期元素 | C.非金属性比硫的强 | D.最高正化合价是 价 价 |
您最近一年使用:0次
解题方法
2 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了6种元素在周期表中的位置,其中①~③代表3种元素。
(1)①的元素符号是_______ 。
(2)下列能说明 比
比 失电子能力强的事实是
失电子能力强的事实是_______ (填字母)。
 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢
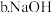 是强碱,
是强碱, 是中强碱
是中强碱
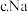 的密度比
的密度比 的小
的小
(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,_______ ,原子半径②小于③,得电子能力②强于③。
(4)依据元素周期律,预测气态氢化物的热稳定性: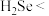
_______ (填写化学式,一种即可)。
| \ | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ||||||||
| 3 |  |  | ① | ② | ||||
| 4 |  | ③ |
(2)下列能说明
 比
比 失电子能力强的事实是
失电子能力强的事实是 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢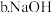 是强碱,
是强碱, 是中强碱
是中强碱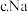 的密度比
的密度比 的小
的小(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,
(4)依据元素周期律,预测气态氢化物的热稳定性:
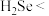
您最近一年使用:0次
名校
解题方法
3 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_______ 。
(3)非金属性e强于g,用原子结构解释原因:_______ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_______ (填序号)。
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | |||||||
| 3 | b | c | d | e | ||||
| 4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因:
(4)下列对f及其化合物的推断中,正确的是
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
您最近一年使用:0次
名校
解题方法
4 .  分别代表原子序数依次增大的短周期元素,在周期表的短周期主族元素中,
分别代表原子序数依次增大的短周期元素,在周期表的短周期主族元素中, 的原子半径最小,
的原子半径最小, 与
与 的最外层电子数相等;
的最外层电子数相等; 的内层电子数是最外层电子数的一半,
的内层电子数是最外层电子数的一半, 的最高化合价和最低化合价的代数和为
的最高化合价和最低化合价的代数和为 和
和 形成原子个数之比为1:2的气态化合物的颜色是红棕色;
形成原子个数之比为1:2的气态化合物的颜色是红棕色; 和
和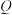 可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
(1)T元素在周期表中的位置是___________ 。
(2)X、Y、Q三种元素的原子半径由小到大的顺序为___________ (填元素符号)。
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)下列可以判断R和T的金属性强弱的是___________。
(5)Z元素对应的最高价氧化物对应的水化物的化合物类型是___________ 。(填“离子化合物”或“共价化合物”)
 分别代表原子序数依次增大的短周期元素,在周期表的短周期主族元素中,
分别代表原子序数依次增大的短周期元素,在周期表的短周期主族元素中, 的原子半径最小,
的原子半径最小, 与
与 的最外层电子数相等;
的最外层电子数相等; 的内层电子数是最外层电子数的一半,
的内层电子数是最外层电子数的一半, 的最高化合价和最低化合价的代数和为
的最高化合价和最低化合价的代数和为 和
和 形成原子个数之比为1:2的气态化合物的颜色是红棕色;
形成原子个数之比为1:2的气态化合物的颜色是红棕色; 和
和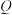 可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:(1)T元素在周期表中的位置是
(2)X、Y、Q三种元素的原子半径由小到大的顺序为
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为
(4)下列可以判断R和T的金属性强弱的是___________。
| A.单质的熔点:R比T低 |
B.单质与酸反应时,失电子数: 比 比 少 少 |
C.单质与水反应: 比 比 更易 更易 |
D.最高价氧化物对应水化物的碱性: 比T强 比T强 |
您最近一年使用:0次
名校
解题方法
5 . 根据元素周期律判断,不正确的是
| A.Mg原子失电子能力比Ca弱 | B.K与水反应比Mg与水反应剧烈 |
| C.HCl的稳定性强于HBr | D. 酸性强于 酸性强于 |
您最近一年使用:0次
6 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图所示,下列有关含量前六位元素的说法正确的是


| A.原子半径Al<Si |
| B.六种元素均为主族元素 |
| C.六种元素中,非金属性最强的是氧元素 |
| D.月壤元素含量排在第2位的硅的氧化物可用于做半导体材料 |
您最近一年使用:0次
名校
解题方法
7 . 镓(31Ga)与K位于元素周期表中同一周期,下列关于Ga的说法不正确的是
| A.位于元素周期表第ⅢA族 | B.原子半径比K小 |
| C.单质的还原性比K弱 | D.Ga(OH)3的碱性比Al(OH)3弱 |
您最近一年使用:0次
2023-04-10更新
|
276次组卷
|
4卷引用:北京师范大学附属实验中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
8 . 下列顺序正确的是
| A.酸性HNO3>H3PO4>HClO4 | B.还原性F->Cl->S2- |
| C.稳定性:H2O>HF>H2S | D.原子半径:Na>Mg>O |
您最近一年使用:0次
名校
9 . 下列有关性质的比较,不能用元素周期律解释的是
| A.酸性:H2SO4>H3PO4 | B.非金属性:N>P |
| C.氧化性:O2>S | D.高温时的还原性:C>Si |
您最近一年使用:0次
名校
10 . 下表是元素周期表的一部分,请按要求回答下列问题:
(1)元素①形成的温室气体(氧化物)的结构式为___________ 。
(2)元素④⑤⑥的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)用电子式表示元素③和元素⑥组成的化合物的形成过程___________ 。
(4)用离子方程式表示元素④的最高价氧化物与元素②的最高价氧化物的水化物的反应___________ 。
(5)下列对元素⑦的说法正确的是___________ (填序号)
a.原子的核电荷数为34
b.气态氢化物的稳定性⑤>⑦
c.能形成 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性
(6)从原子结构角度解释元素⑥的非金属性强于元素⑧的原因___________ 。元素⑥和⑧化合形成的 属于卤素互化物,性质与
属于卤素互化物,性质与 相似。写出
相似。写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式___________ 。
族 族 | IA | 0 | ||||||
1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | |||||||
3 | ② | ④ | ⑤ | ⑥ | ||||
4 | ③ | ⑦ | ⑧ | |||||
(1)元素①形成的温室气体(氧化物)的结构式为
(2)元素④⑤⑥的简单离子半径由大到小的顺序是
(3)用电子式表示元素③和元素⑥组成的化合物的形成过程
(4)用离子方程式表示元素④的最高价氧化物与元素②的最高价氧化物的水化物的反应
(5)下列对元素⑦的说法正确的是
a.原子的核电荷数为34
b.气态氢化物的稳定性⑤>⑦
c.能形成
 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性(6)从原子结构角度解释元素⑥的非金属性强于元素⑧的原因
 属于卤素互化物,性质与
属于卤素互化物,性质与 相似。写出
相似。写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次



