名校
1 . 元素周期表是研究化学的重要工具。下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题。

(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ;元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键” 或“离子键和共价键”);将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式);该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含10e-和18e-的分子的电子式分别是_______ 、_______ 。
(6)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
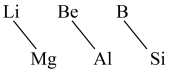
(7)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含10e-和18e-的分子的电子式分别是
(6)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第ⅠA、ⅡA族元素中寻找制造耐高温、耐腐蚀合金的元素 |

| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.BeCl2是离子化合物 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次
解题方法
2 . 锂的用途很广泛,涉及电池、核工业等领域。下列说法错误的是
| A.钠与水的反应比锂更剧烈 |
| B.锂是最轻的金属,具有银白色光泽 |
| C.锂在氧气中燃烧的产物主要是氧化锂 |
| D.等质量的锂和钾相比,钾与水反应生成的H2较多 |
您最近一年使用:0次
3 . X、Y、Z、M、Q为前四周期元素,原子序数依次增大。X的族序数等于其周期数,Y和M同族,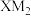 分子和
分子和 分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
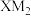 分子和
分子和 分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是A.一个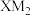 分子含1个 分子含1个 和2个 和2个 | B.X的氢氧化物能与NaOH溶液反应 |
| C.Y的气态氢化物沸点比M的气态氢化物低 | D.基态Q原子的价电子排布式为 |
您最近一年使用:0次
名校
解题方法
4 . 四种短周期元素X、Y、Z、W在周期表中的位置如表所示,其中Z元素的最外层电子数是内层电子总数的 。试回答下列问题。
。试回答下列问题。
(1)Y元素在元素周期表中的位置___________ 。四种元素中原子半径最大的是___________ (填元素符号)。
(2)写出Y的氧化物的一种用途___________ 。
(3)能证明W的非金属性强于Y的事实是___________ 。
a.W的氢化物水溶液显酸性,Y的氢化物不显酸性
b.Y的氢化物不如W的氢化物稳定
c.简单阴离子的还原性:Y>W
(4)+2价X的氧化物可将W的+4价氧化物还原为W单质,恢复至室温时,生成1 mol W放热269.0 kJ,则该反应的热化学方程式为___________ 。
(5)W的最高价氧化物对应的水化物可以氧化Z的氢化物,并将Z氧化为最高价氧化物,写出反应的化学方程式___________ 。氧化1 mol Z的氢化物转移电子的物质的量为___________ 。
 。试回答下列问题。
。试回答下列问题。X | ||
Y | Z | W |
(1)Y元素在元素周期表中的位置
(2)写出Y的氧化物的一种用途
(3)能证明W的非金属性强于Y的事实是
a.W的氢化物水溶液显酸性,Y的氢化物不显酸性
b.Y的氢化物不如W的氢化物稳定
c.简单阴离子的还原性:Y>W
(4)+2价X的氧化物可将W的+4价氧化物还原为W单质,恢复至室温时,生成1 mol W放热269.0 kJ,则该反应的热化学方程式为
(5)W的最高价氧化物对应的水化物可以氧化Z的氢化物,并将Z氧化为最高价氧化物,写出反应的化学方程式
您最近一年使用:0次
2021-11-07更新
|
211次组卷
|
2卷引用:河南省周口恒大中学2022-2023学年高二下学期开学考试化学试题



