名校
解题方法
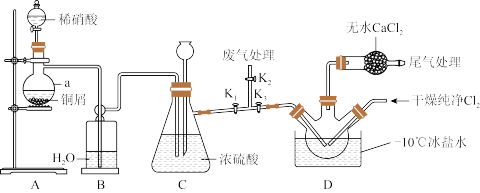
1 . 亚硝酰氯NOCl常用于合成洗涤剂、触媒及用作中间体,其熔点为-64.5℃,沸点-5.5℃,遇水易水解为两种酸。某学习小组在实验室用 与NO制备NOCl并测定其纯度,进行如下实验(部分夹持装置已略去)。
与NO制备NOCl并测定其纯度,进行如下实验(部分夹持装置已略去)。
(1)实验室用 制取
制取 的离子方程式为
的离子方程式为_______ 。
(2)装置A中仪器a的名称为_______ ,装置C中长颈漏斗的作用是_______ 。
(3)若不用装置D中的干燥管,对实验有何影响_______ (用化学方程式表示)。
(4)N、O、Cl的简单离子中半径最小的是_______ (填离子符号),简单氢化物的熔沸点由高到低的顺序是_______ (用化学式表示)。
(5)通过以下实验测定NOCl样品的纯度。取D中所得液体10g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL于锥形瓶中,用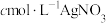 。标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCL)样品的纯度为
。标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCL)样品的纯度为_______ 。
 与NO制备NOCl并测定其纯度,进行如下实验(部分夹持装置已略去)。
与NO制备NOCl并测定其纯度,进行如下实验(部分夹持装置已略去)。
(1)实验室用
 制取
制取 的离子方程式为
的离子方程式为(2)装置A中仪器a的名称为
(3)若不用装置D中的干燥管,对实验有何影响
(4)N、O、Cl的简单离子中半径最小的是
(5)通过以下实验测定NOCl样品的纯度。取D中所得液体10g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL于锥形瓶中,用
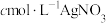 。标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCL)样品的纯度为
。标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCL)样品的纯度为
您最近一年使用:0次
2022-05-29更新
|
305次组卷
|
3卷引用:新疆生产建设兵团第六师五家渠高级中学2022-2023学年高三2月月考化学试题
名校
解题方法
2 . 短周期元素A、B、C、D、E、F的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,A和D同主族,B和C相邻,F的最高价氧化物对应的水化物为无机含氧酸中的最强酸。E与B可构成化合物E3B2,且该物质遇水发生水解反应。已知利用如下装置以制备E3B2,装置①用于制备B单质。下列说法错误的是


| A.E与B的简单离子的电子层结构相同,且离子半径B>E |
| B.③、④、⑥中依次盛装的试剂可以是NaOH 溶液浓H2SO4、碱石灰 |
| C.A、B、C三种元素组成的化合物可能与F的最高价氧化物对应的水化物反应 |
| D.实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝 |
您最近一年使用:0次



