名校
解题方法
1 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X、Y位于同周期,它们的原子最外层电子数均为偶数,W、Z同主族。下列说法正确的是
| A.简单离子半径:Z>Y>W | B. 中的原子最外层均满足 中的原子最外层均满足 稳定结构 稳定结构 |
| C.最简单氢化物的热稳定性:X>Y | D.WY不能与氢氧化钠溶液反应 |
您最近一年使用:0次
2024-04-07更新
|
337次组卷
|
4卷引用:江西省部分地区2023-2024学年高三下学期3月月考化学试题
2 . 下列物质性质中,不能用“对角线规则”解释的是
A. 和 和 都能与 都能与 反应生成盐和水 反应生成盐和水 |
B.硼单质、硅单质都是共价晶体且都能与 溶液反应生成盐和 溶液反应生成盐和 |
| C.溴单质、碘单质都能与氢气在一定条件下生成氢化物 |
D.常温下, 、 、 都难溶于水 都难溶于水 |
您最近一年使用:0次
解题方法
3 . 依据元素周期表与元素周期律回答以下问题:
(1)根据元素周期表对角线规则,金属Be与Al单质及其化合物性质相似。写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:___ 。
(2)硒(34Se)和S位于同一主族。H2Se的稳定性比H2S的___ (填“强”或“弱”,断开1molH—Se键吸收的能量比断开1molH—S键吸收的能量____ (填“多”或“少”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下___ 。
(3)氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
①砷在元素周期表中的位置___ 。
②沸点:N2H4___ P2H4(填“>”或“<”),判断依据是___ 。
③PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应所得产物的推断正确的是___ (填序号)。
a.只含共价键 b.难于水
c.受热易分解 d.能与NaOH溶液反应
(1)根据元素周期表对角线规则,金属Be与Al单质及其化合物性质相似。写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:
(2)硒(34Se)和S位于同一主族。H2Se的稳定性比H2S的
(3)氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
①砷在元素周期表中的位置
②沸点:N2H4
③PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应所得产物的推断正确的是
a.只含共价键 b.难于水
c.受热易分解 d.能与NaOH溶液反应
您最近一年使用:0次
4 . 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应: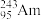 +
+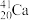 =
=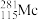 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是___________ 。
(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式___________ ;该分子内存在的共价键类型有___________ 。
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式___________ 。
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应:
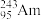 +
+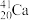 =
=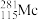 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
| A.硼的电负性和硅相近 |
| B.π键是由两个p轨道“肩并肩”重叠形成的,呈轴对称。 |
| C.Cl2是双原子分子,H2S是三原子分子,这是由共价键的方向性决定的 |
| D.原子和其它原子形成共价键时,其共价键数一定等于原子的价电子数 |
您最近一年使用:0次
6 . 已知铍(Be)原子与镁原子最外层电子数都为2,而铍元素与铝元素的单质及其化合物的性质相似。下列关于铍的化合物的推断中不正确的是
| A.氯化铍的化学式为BeCl2 |
| B.BeO、Be(OH)2均难溶于水 |
| C.氢氧化铍与与强碱反应的离子方程式:Be(OH)2+OH-= BeO2-+ H2O |
| D.氧化铍与稀硫酸反应的化学方程式为:BeO+H2SO4 = BeSO4+H2O |
您最近一年使用:0次
名校
7 . 下列实验事实及理论解释都正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 酸性: H3BO3、 H2SiO3 相近 | B、Si电负性相近,符合“对角线规则” |
| B | 熔点: SiO2> SiCl4 | 键能:Si-O>Si-Cl |
| C | 密度:干冰>冰 | 相对分子质量:CO2>H2O |
| D | 沸点: Cl2> N2>CO | CO为极性分子:且相对分子质量:Cl2>CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-05-18更新
|
196次组卷
|
2卷引用:江西省安福中学2022-2023学年高二下学期5月期中考试化学试题
9-10高一下·江西·期中
8 . 运用元素周期律分析下面的推断,其中错误的是( )
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为有色固体;HAt不稳定;AgAt感光性很强,且不溶于水也不溶于稀酸 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
您最近一年使用:0次



