1 . 下列化学反应表示错误的是
A.氢氧化铍溶于强碱: |
B.可溶性铝盐净水原理: |
C.硅与氢氧化钠溶液反应: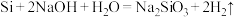 |
D.焦炭与石英砂反应: |
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、M、R、Q为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示,下列说法正确的是
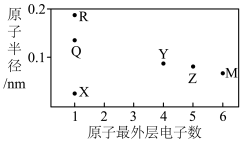
| A.M存在最高化合价为+6价 |
| B.Q单质与Y的氧化物之间一定无法发生置换反应 |
C.Y、M形成的化合物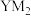 为大气污染物 为大气污染物 |
| D.X、Z、M可形成一种含共价键、配位键的离子化合物 |
您最近一年使用:0次
7日内更新
|
417次组卷
|
2卷引用:广东省汕头市2024届高三二模考试化学试
名校
3 . 以下类比结论中正确的是
A. 的沸点高于 的沸点高于 ,则 ,则 的沸点高于 的沸点高于 |
B. 分子结构为直线形,则 分子结构为直线形,则 分子结构也是直线形 分子结构也是直线形 |
C. 能与 能与 溶液发生反应,则 溶液发生反应,则 也能与 也能与 溶液发生反应 溶液发生反应 |
D. 用作耐火材料,则 用作耐火材料,则 也可用作耐火材料 也可用作耐火材料 |
您最近一年使用:0次
2024-05-11更新
|
254次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
4 . Be与 类似,
类似, 也能与
也能与 溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出
溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出 和
和 反应的离子方程式
反应的离子方程式___________ 。
 类似,
类似, 也能与
也能与 溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出
溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出 和
和 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
解题方法
5 . 下列说法不正确的是
A. 的熔点低于 的熔点低于 ,可推知 ,可推知 的熔点低于 的熔点低于 |
B. 与Na反应的剧烈程度弱于 与Na反应的剧烈程度弱于 与Na反应的剧烈程度,可知烃基为推电子基团,减小了 与Na反应的剧烈程度,可知烃基为推电子基团,减小了 的极性 的极性 |
C. 的分子空间构型为V形,可推知 的分子空间构型为V形,可推知 的分子空间构型也为V形 的分子空间构型也为V形 |
D. 为两性氧化物,可推知BeO也为两性氧化物 为两性氧化物,可推知BeO也为两性氧化物 |
您最近一年使用:0次
名校
解题方法
6 . 元素周期律反映了元素性质的周期性变化规律。
(1)氮氧化铝(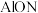 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是___________ 。
(2)在元素周期表中, ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:___________ 。
(3)锡为主族元素,其原子结构示意图: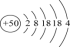 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是___________ , 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:___________ 。
(4)硒 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式:___________ 。理论上该反应每转移 电子,可得到的
电子,可得到的 的质量为
的质量为___________ g。
(1)氮氧化铝(
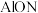 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是(2)在元素周期表中,
 ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:(3)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:(4)硒
 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式: 电子,可得到的
电子,可得到的 的质量为
的质量为
您最近一年使用:0次
名校
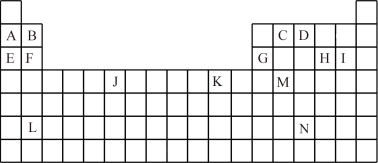
7 . 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
(1)写出基态时J的价层电子排布式_____ ,L的原子序数为____ ,K的+2离子的价层电子的轨道表示式_____ 。
(2)下列关于元素在元素周期表中的位置的叙述正确的是_____。
(3)G元素最高价氧化物的水化物与E元素最高价氧化物的水化物的溶液反应的离子方程式是______ 。
(4)根据对角线规则及已知元素性质,推测A元素的单质与氧气在点燃时反应生成的物质为_______ (填化学式)。
(5)D的简单气态氢化物的 构型为
构型为______ ,它极易溶于水,原因是_______ 。
(1)写出基态时J的价层电子排布式
(2)下列关于元素在元素周期表中的位置的叙述正确的是_____。
| A.M位于元素周期表中第四周期ⅥA族,属于p区元素 |
| B.J位于元素周期表中第四周期ⅣB族,属于d区元素 |
| C.F位于元素周期表中第三周期ⅡA族,属于s区元素 |
| D.I位于元素周期表中第三周期ⅦA族,属于ds区元素 |
(3)G元素最高价氧化物的水化物与E元素最高价氧化物的水化物的溶液反应的离子方程式是
(4)根据对角线规则及已知元素性质,推测A元素的单质与氧气在点燃时反应生成的物质为
(5)D的简单气态氢化物的
 构型为
构型为
您最近一年使用:0次
8 . 中国科学院化学研究所有机固体院重点实验室合成了适用于非卤溶剂加工的“巨分子受体”,对于推动聚合物太阳电池受体光伏材料的发展具有重要意义。目前可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1) 在元素周期表中的位置为
在元素周期表中的位置为_______ ,其基态原子有_______ 种不同运动状态的电子。
(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为_______ ,其核外电子占据的最高能级的电子云轮廓图为_______ 。
(3)第一电子亲和能 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
_______ (填“ ”或“
”或“ ”)
”)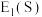 。
。
(4) 和
和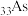 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是_______ (填元素符号),试解释其原因:_______ 。
(5)根据对角线规则可知, 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
(1)
 在元素周期表中的位置为
在元素周期表中的位置为(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为
(3)第一电子亲和能
 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
 ”或“
”或“ ”)
”)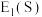 。
。(4)
 和
和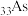 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是(5)根据对角线规则可知,
 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题:
(1)②元素原子的电子式是:_______ 。
(2)硅元素在周期表中的位置是:第_______ 周期_______ 族。
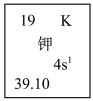
(3)如图所示钾元素的部分信息,“30.97”数值表示_______ 。______ (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的是_______ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式_______ 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因_______ 。能证明这一事实的化学反应为_______ (写一个化学方程式)。
(6)能证明O元素的非金属性强于S元素的依据是_______ 。
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是_______ 。
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是_______ 。
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是_______ 。
族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②元素原子的电子式是:
(2)硅元素在周期表中的位置是:第
(3)如图所示钾元素的部分信息,“30.97”数值表示
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因
(6)能证明O元素的非金属性强于S元素的依据是
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是
| A.质子数相同 | B.质量相同 |
| C.化学性质相同 | D.位置相同(周期表中) |
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第IA、IIA族元素中寻找制造耐高温、耐腐蚀合金的元素 |
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
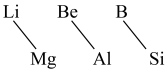
| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.Be不与水反应 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次
名校
解题方法
10 . 类推的思维方法在化学学习中应用广泛,但类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论错误的是
| A.Al(OH)3能与NaOH溶液反应,则Be(OH)2也能与NaOH溶液反应 |
| B.SO2是“V形”分子,则O3是“V形”分子 |
| C.NH3中N原子采用sp3杂化则PH3中P也采用sp3杂化 |
| D.工业制Mg采用电解熔融MgCl2的方法,则工业制Al也可采用电解熔融AlCl3的方法 |
您最近一年使用:0次
2024-04-11更新
|
114次组卷
|
2卷引用:宁夏六盘山高级中学2023-2024学年高二下学期第一次月考化学试题



