1 . 联合国大会宣布2019年是“国际化学元素周期表年”(I YPT 2019)·下列运用元素周期律分析的推断中,错误的是
| A.铍(Be)的氧化物的水化物具有两性 |
| B.砹(At)为有色固体,AgAt感光性很强,不溶于水 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体 |
您最近一年使用:0次
2019-12-26更新
|
206次组卷
|
6卷引用:苏教版高一化学必修2专题一第一单元第三课时《元素周期表》课时训练(夯实基础)
名校
解题方法
2 . Ⅰ.下列8种化学符号: O2、
O2、 O3、
O3、 H、
H、 C、
C、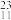 Na、
Na、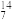 N、
N、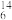 C、
C、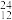 Mg。
Mg。
(1)表示核素的符号共_____ 种。
(2)互为同位素的是______ ,质量数相等的是_______ ,中子数相等的是____ 。
(3)质量相同的H216O和D216O所含中子数之比为________ 。
Ⅱ.根据周期表对角线规则,金属Be与Al的单质及其化合物的性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式____________
(5)Be(OH)2与Mg(OH)2可用_________ 鉴别。
Ⅲ.铜有两种天然同位素 Cu和
Cu和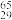 Cu,参考铜的相对原子质量(63.5)。
Cu,参考铜的相对原子质量(63.5)。
(6)计算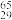 Cu的质量百分含量约是
Cu的质量百分含量约是_________ 。(保留3位有效数字)
 O2、
O2、 O3、
O3、 H、
H、 C、
C、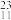 Na、
Na、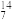 N、
N、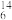 C、
C、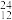 Mg。
Mg。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
Ⅱ.根据周期表对角线规则,金属Be与Al的单质及其化合物的性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式
(5)Be(OH)2与Mg(OH)2可用
Ⅲ.铜有两种天然同位素
 Cu和
Cu和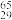 Cu,参考铜的相对原子质量(63.5)。
Cu,参考铜的相对原子质量(63.5)。(6)计算
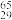 Cu的质量百分含量约是
Cu的质量百分含量约是
您最近一年使用:0次
3 . 铝和铍的性质十分相似, 下列关于铍性质推断不正确的是( )
| A.氧化铍能与强酸或强碱起反应 | B.氢氧化铍可溶于水 |
| C.氢氧化铍是两性氢氧化物 | D.氯化铍溶液显酸性 |
您最近一年使用:0次
2019-10-24更新
|
160次组卷
|
2卷引用:河南省周口市中英文学校2019-2020学年高一下学期期中考试(6月)化学试题
名校
4 . 根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(1)写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:______________________________________ 。
(2)Be(OH)2与Mg(OH)2可用__________ 试剂鉴别,其离子方程式为:______________________________ 。
(3)Li与Mg根据对角线规则,性质也相似,Li2CO3受热也易分解,请写出分解产物中金属氧化物的电子式_____________ ,它属于____________ 晶体。
(1)写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:
(2)Be(OH)2与Mg(OH)2可用
(3)Li与Mg根据对角线规则,性质也相似,Li2CO3受热也易分解,请写出分解产物中金属氧化物的电子式
您最近一年使用:0次
5 . 铍原子比铝原子少1个电子层,最外层电子数也比铝原子少1,在周期表中铍和铝处于对角线位置,具有“对角线”关系的元素性质存在相似性。下列关于铍的判断不正确的是( )
| A.Be能在空气中燃烧 |
| B.BeO熔点较低 |
| C.BeCl2易溶于水 |
| D.Be(OH)2具有两性 |
您最近一年使用:0次
名校
6 . 几种短周期元素的原子半径及主要化合价见下表:下列叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A.L、M的单质在相同条件下与相同浓度稀盐酸反应的反应速率为L>M |
| B.M与T形成的化合物有两性 |
| C.Q是硫元素 |
| D.L、Q形成的简单离子核外电子数相等 |
您最近一年使用:0次
9-10高一下·江西·期中
7 . 运用元素周期律分析下面的推断,其中错误的是( )
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为有色固体;HAt不稳定;AgAt感光性很强,且不溶于水也不溶于稀酸 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
您最近一年使用:0次
11-12高一下·江苏·期中
8 . 锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性。下列关于锂的判断可能正确的是
| A.Li能在空气中燃烧 | B.Li2O熔点较低 |
| C.Li2CO3能溶于水 | D.LiOH受热时不易分解 |
您最近一年使用:0次
9 . 如图所示,在元素周期表中处于A、B位置的某些元素性质相似,这称为“对角线规则”。A为铍(Be),原子序数为4,B为铝(Al),下列有关其性质的推断正确的是


| A.铍能与冷水发生剧烈反应 |
| B.氢氧化铍既能与强酸溶液反应,又能与强碱溶液反应 |
| C.氢氧化铍的化学式为Be(OH)3 |
| D.氢氧化铍易溶于水 |
您最近一年使用:0次
10 . 元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在周期表的位置______________________ 。
(2)比较Be2+、Li+、H+微粒半径的大小_______________________ 。
(3)下列有关Be性质的推断正确的是_______________________ 。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点
c.常温时,BeCl2溶液的pH<7
(4)已知:Al4C3+ 12H2O === 4Al(OH)3 + 3CH4↑,写出Be2C与NaOH溶液反应的方程式(铍酸根离子:BeO22-)_________________________ 。
(1)Be元素在周期表的位置
(2)比较Be2+、Li+、H+微粒半径的大小
(3)下列有关Be性质的推断正确的是
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点
c.常温时,BeCl2溶液的pH<7
(4)已知:Al4C3+ 12H2O === 4Al(OH)3 + 3CH4↑,写出Be2C与NaOH溶液反应的方程式(铍酸根离子:BeO22-)
您最近一年使用:0次



