1 . 下列化学反应表示错误的是
A.氢氧化铍溶于强碱: |
B.可溶性铝盐净水原理: |
C.硅与氢氧化钠溶液反应: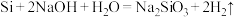 |
D.焦炭与石英砂反应: |
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、M、R、Q为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示,下列说法正确的是
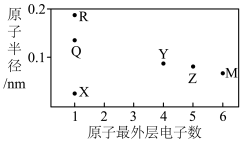
| A.M存在最高化合价为+6价 |
| B.Q单质与Y的氧化物之间一定无法发生置换反应 |
C.Y、M形成的化合物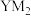 为大气污染物 为大气污染物 |
| D.X、Z、M可形成一种含共价键、配位键的离子化合物 |
您最近一年使用:0次
7日内更新
|
414次组卷
|
2卷引用:广东省汕头市2024届高三二模考试化学试
名校
3 . 以下类比结论中正确的是
A. 的沸点高于 的沸点高于 ,则 ,则 的沸点高于 的沸点高于 |
B. 分子结构为直线形,则 分子结构为直线形,则 分子结构也是直线形 分子结构也是直线形 |
C. 能与 能与 溶液发生反应,则 溶液发生反应,则 也能与 也能与 溶液发生反应 溶液发生反应 |
D. 用作耐火材料,则 用作耐火材料,则 也可用作耐火材料 也可用作耐火材料 |
您最近一年使用:0次
2024-05-11更新
|
253次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
解题方法
4 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X、Y位于同周期,它们的原子最外层电子数均为偶数,W、Z同主族。下列说法正确的是
| A.简单离子半径:Z>Y>W | B. 中的原子最外层均满足 中的原子最外层均满足 稳定结构 稳定结构 |
| C.最简单氢化物的热稳定性:X>Y | D.WY不能与氢氧化钠溶液反应 |
您最近一年使用:0次
2024-04-07更新
|
327次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
5 . 类比推理是化学中常用的思维方法,下列说法正确的是
A. 是非极性分子,则 是非极性分子,则 是非极性分子 是非极性分子 |
B. 有还原性,则 有还原性,则 也有还原性 也有还原性 |
C. 易溶于水,则 易溶于水,则 也易溶于水 也易溶于水 |
D. 被足量酸性 被足量酸性 溶液氧化为 溶液氧化为 ,则 ,则 被足量酸性 被足量酸性 溶液氧化为 溶液氧化为 |
您最近一年使用:0次
名校
6 . 依据物质结构与反应原理分析,下列演绎或推论不正确的是


A.通常状况下,氯化铝为分子晶体,可推知 也为分子晶体 也为分子晶体 |
| B.常温下,浓硫酸或浓硝酸能使铁钝化,可推知钴、镍也可能会钝化 |
C. 不能使酸性高锰酸钾溶液褪色,可推知 不能使酸性高锰酸钾溶液褪色,可推知 也不能使之褪色 也不能使之褪色 |
D.如图装置可以制备无水氯化镁,也可由 制备 制备 |
您最近一年使用:0次
7 . 下列有关元素周期表及元素周期律的说法错误的是
| A.N能层的能级数最多为4个 |
| B.Na元素在元素周期表的ds区 |
| C.F元素在同周期中电负性最大 |
| D.根据对角线规则,铍和铝的化学性质具有相似性 |
您最近一年使用:0次
8 . 下列物质性质相似与“对角线”规则无关的是
A. 能与 能与 反应, 反应, 也能与 也能与 反应 反应 |
B. 微溶于水, 微溶于水, 也微溶于水 也微溶于水 |
| C.单质硼的熔点高,晶体硅的熔点也高 |
| D.Fe能与HCl反应,Al也能与HCl反应 |
您最近一年使用:0次
解题方法
9 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
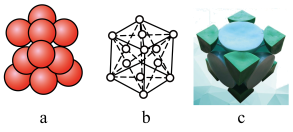
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2023-10-28更新
|
92次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期10月月考化学试题
名校
10 . 类比法是一种学习化学的重要方法,下列类比结论正确的是
| A.AlCl3是共价化合物,则 BeCl2也是共价化合物 |
| B.N2分子中存在N≡N键,化学性质稳定,则CH≡CH化学性质稳定 |
| C.NaCl固体与浓硫酸共热可制 HCl,则NaI固体与浓硫酸共热可制 HI |
| D.卤素单质中 F₂熔点最低,则碱金属元素单质中 Li 的熔点最低 |
您最近一年使用:0次



