1 . 下列物质性质相似与“对角线”规则无关的是
A. 能与 能与 反应, 反应, 也能与 也能与 反应 反应 |
B. 微溶于水, 微溶于水, 也微溶于水 也微溶于水 |
| C.单质硼的熔点高,晶体硅的熔点也高 |
| D.Fe能与HCl反应,Al也能与HCl反应 |
您最近一年使用:0次
解题方法
2 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子中,占据最高能级电子的电子云轮廓图形状为___________ 。
(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是___________ 。
(ii)离子半径:Li+___________ H-(填“>”“=”或“<”)。
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:
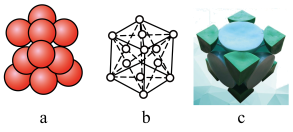
(i)晶胞中锂的配位数为___________ 。
(ii)若锂原子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为___________  (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
(1)在元素周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是(2)LiH是一种储氢材料。
(i)Li与H中第一电离能较小的元素是
(ii)离子半径:Li+
(3)已知金属锂晶体为FCC(面心立方晶格),面心立方紧密堆积结构示意图如下:

(i)晶胞中锂的配位数为
(ii)若锂原子的半径为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则锂晶体密度为
,则锂晶体密度为 (列出含有
(列出含有 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2023-10-28更新
|
93次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期10月月考化学试题
名校
3 . 类比法是一种学习化学的重要方法,下列类比结论正确的是
| A.AlCl3是共价化合物,则 BeCl2也是共价化合物 |
| B.N2分子中存在N≡N键,化学性质稳定,则CH≡CH化学性质稳定 |
| C.NaCl固体与浓硫酸共热可制 HCl,则NaI固体与浓硫酸共热可制 HI |
| D.卤素单质中 F₂熔点最低,则碱金属元素单质中 Li 的熔点最低 |
您最近一年使用:0次
4 . 下列说法正确的是
| A.Fe分别与Cl2、S反应,产物中Fe的化合价相同 |
| B.Cu分别与浓硝酸、稀硝酸反应,生成的产物完全相同 |
| C.CO2分别与Na2O2、CaO反应,反应类型相同 |
| D.Be分别与盐酸、氢氧化钠溶液反应,生成的气体相同 |
您最近一年使用:0次
2023-10-10更新
|
120次组卷
|
3卷引用:重庆市拔尖强基联盟(西南大学附中、育才中学)2023-2024学年高三10月联合考试化学试题
名校
5 . 应用元素周期律可预测我们不知道的一些元素及其化合物的性质,下列预测正确的是
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液反应均产生氢气
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是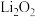 ,其溶液是一种强碱
,其溶液是一种强碱
⑤ 可能是难溶于水的白色固体
可能是难溶于水的白色固体
⑥ 无色,有毒,比
无色,有毒,比 稳定
稳定
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液反应均产生氢气
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是
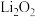 ,其溶液是一种强碱
,其溶液是一种强碱⑤
 可能是难溶于水的白色固体
可能是难溶于水的白色固体⑥
 无色,有毒,比
无色,有毒,比 稳定
稳定| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
2023-09-15更新
|
240次组卷
|
2卷引用:河南省郑州外国语学校2022-2023学年高三上学期12月月考化学试题
解题方法
6 . 镁、锂的性质相似,下列有关锂的说法不正确的是
| A.Li2SO4易溶于水 | B.LiOH是受热不易分解的强碱 |
| C.Li遇浓硫酸不产生“钝化”现象 | D.Li2CO3受热分解,生成Li2O和CO2 |
您最近一年使用:0次
名校
解题方法
7 . 类比法是一种学习化学的重要方法,下列类比法结论正确的是
| A.AlCl3是共价化合物,则BeCl2也是共价化合物 |
| B.C2H5OH分子间可以形成氢键,则CH3CHO分子间也可以形成氢键 |
| C.NaCl固体与浓硫酸共热可制HCl,则NaI固体与浓硫酸共热可制HI |
| D.卤素单质中F2熔点最低,则碱金属元素单质中Li的熔点最低 |
您最近一年使用:0次
2023-06-02更新
|
302次组卷
|
2卷引用:辽宁省东北育才学校科学高中部2023届高三最后一次模拟考试化学试题
名校
8 . 根据周期表中的对角线规则,下列有关推断错误的是
| A.BeO是两性氧化物 | B.Li在空气中燃烧可生成 和 和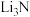 |
C. 是弱酸 是弱酸 | D.碱性: |
您最近一年使用:0次
2023-04-22更新
|
252次组卷
|
3卷引用:原子结构与性质
9 . 如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

(1)请写出 区铜原子基态电子排布式
区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______
(3)图中第一电离能最小的元素在周期表中的位置是_______
(4)根据对角线规则,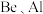 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明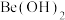 该性质的实验结论是
该性质的实验结论是_______
(5) 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示:
①由此判断该元素是_______ (填元素符号);
②分析图中同周期元素第一电离能的变化规律,推断: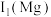
_______  。
。

(1)请写出
 区铜原子基态电子排布式
区铜原子基态电子排布式(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,
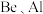 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有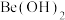 该性质的实验结论是
该性质的实验结论是(5)
 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示: | 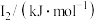 | 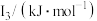 | 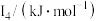 | 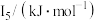 |
| 578 | 1817 | 2745 | 11575 | 14830 |
②分析图中同周期元素第一电离能的变化规律,推断:
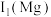
 。
。
您最近一年使用:0次
名校
10 . 元素周期表是重要的化学学习工具。随着原子序数变化,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
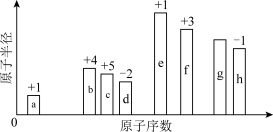
(1)b在元素周期表中的位置是_______ 周期_______ 族。
(2)8种元素中金属性最强的是_______ (用元素符号表示),b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示)。
(3)c、h两种元素电负性相近,在不同的电负性标度下其大小关系不同,写出由两者组成的化合物按照c:h=1:3形成的化合物的电子式:_______ 。
(4)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,Be及其化合物与f单质及其化合物的性质相似,写出Be的最高价氧化物对应的水化物与e的最高价氧化物对应的水化物反应的离子方程式:_______ 。

(1)b在元素周期表中的位置是
(2)8种元素中金属性最强的是
(3)c、h两种元素电负性相近,在不同的电负性标度下其大小关系不同,写出由两者组成的化合物按照c:h=1:3形成的化合物的电子式:
(4)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,Be及其化合物与f单质及其化合物的性质相似,写出Be的最高价氧化物对应的水化物与e的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
2022-11-11更新
|
137次组卷
|
2卷引用:安徽省安庆市第二中学2022-2023学年高三上学期11月月考化学试题



