1 . A、B、C、D、E、F六种元素,均位于周期表的前四周期,它们的核电荷数依次增加,A原子的L层p轨道中有2个电子,B元素在同周期元素中电负性最大,C与A原子的价电子数相同,D的最高价含氧酸酸性最强,E原子核外不成对电子数最多,F元素能形成的双原子分子,其单质在常温下呈液态。
(1)A的最高价含氧酸酸根离子的价层电子对数为_____ ,其 模型是
模型是_____ 。
(2)B、D、F简单氢化物沸点由高到低的顺序为_____ (填化学式),原因是_____ 。
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为_____ 。
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键_____ 。
(1)A的最高价含氧酸酸根离子的价层电子对数为
 模型是
模型是(2)B、D、F简单氢化物沸点由高到低的顺序为
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键
您最近一年使用:0次
名校
解题方法
2 . W、X、Y、Z是原子序数递增的短周期主族元素,Z原子的核外电子总数是次外层电子数的4倍,现代石油化工采用银作催化剂,可以一步完成化合物乙的制备,化合物乙常用于一次性医用口罩的消毒,下列说法正确的是


| A.原子半径:Z>Y>X |
| B.X、Y的氢化物的沸点:Y>X |
| C.Y的氧化物对应水化物均为强酸 |
| D.以上四种元素能形成不止1种既能与强酸又能与强碱反应的离子化合物 |
您最近一年使用:0次
2023-06-27更新
|
228次组卷
|
2卷引用:广东省揭阳市普宁市第二中学2020-2021学年高三下学期适应性考试(二)化学试题
名校
解题方法
3 . 现有原子序数依次增大的短周期主族元素W、P、Q,气体X、Y、Z分别为W、P、Q的单质,X、Y、Z之间能发生如图转换关系。已知化合物乙的水溶液常用于蚀刻玻璃,化合物乙与化合物甲反应可生成白烟。下列说法正确的是
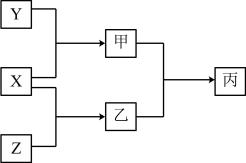

| A.W元素的氧化物中只存在极性共价键 |
| B.P元素的氧化物都是酸性氧化物 |
| C.化合物甲能使湿润的紫色石蕊试纸变红 |
| D.化合物甲和乙分子中所含电子总数相同 |
您最近一年使用:0次
名校
4 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W最外层电子数是内层电子数的3倍,Y在短周期元素中原子半径最大,Z的最高正价与最低负价代数之和为4,下列说法不正确的是
| A.阴离子的还原性:X > W > Z |
| B.Z与W形成的某种物质能使品红溶液褪色 |
| C.X与Y形成离子化合物 |
| D.W与Y组成的Y2W2可作为供氧剂 |
您最近一年使用:0次
2023-03-27更新
|
262次组卷
|
4卷引用:四川省达州市大竹中学2020-2021学年高一下学期第一次月考化学试题
名校
5 . a、b、c、d、e均为短周期主族元素,其最高正化合价或最低负化合价与原子序数的关系如图所示。下列说法正确的是
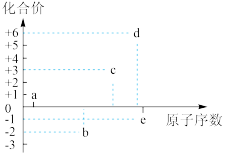

| A.d的原子半径比e的小 |
| B.常温下,c单质不与b单质反应 |
| C.与d元素同主族的下一周期元素的单质可作为半导体材料 |
| D.a与b元素形成的化合物仅含有极性键 |
您最近一年使用:0次
2023-02-02更新
|
237次组卷
|
2卷引用:湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷
6 . 原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y;A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是_______ 。
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式_______ 。
(3)B元素的单质与浓硫酸反应的化学方程式_______ 。
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式_______ 。
(1)B在周期表中的位置是
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式
(3)B元素的单质与浓硫酸反应的化学方程式
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式
您最近一年使用:0次
解题方法
7 . W、X、Y、Z为原子序数依次增大的四种短周期元素,W的简单氢化物可用作制冷剂,Y所在周期数与族序数相同,X与Y为同周期元素,Z原子的最外层电子数与W的电子总数相等。下列说法不正确的是
| A.简单离子半径:Z>W>X>Y |
| B.W、X的氢化物在常温下均为气体 |
| C.Y的最高价氧化物的水化物为两性氢氧化物 |
| D.W与Z形成的化合物中只有共价键 |
您最近一年使用:0次
解题方法
8 . 如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是


A.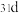 和 和 属于同种核素 属于同种核素 |
B.气态氢化物的稳定性: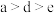 |
C.a与b可以形成 、 、 两种化合物 两种化合物 |
| D.五种元素原子形成的简单离子中,c离子的半径最小 |
您最近一年使用:0次
9 . 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z组合成一种超分子,分子结构示意图如下。W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。(注:实线代表共价键,其他重复单元的W、X未标注)下列说法不正确的是


| A.Y单质的氧化性在同主族中最强 |
| B.离子半径:Z>Y |
| C.Z与Y组成的两种常见离子化合物的阴阳离子个数比相同 |
| D.氢化物的热稳定性:Y>X |
您最近一年使用:0次
解题方法
10 . 甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:
①取mg甲的晶体溶于蒸馏水,配成500mL溶液;
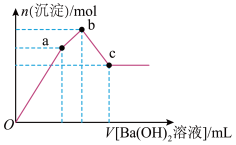
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224mL。
回答下列问题:
(1)D在元素周期表中的位置为_______ 。
(2)经测定晶体甲的摩尔质量为453g∙mol﹣1,其中阳离子和阴离子物质的量之比为1:1,且1mol甲晶体中含有12mol结晶水。则晶体甲的化学式为_______ 。
(3)图象中V(Oa):V(ab):V(bc)=_______
(4)写出ab段发生反应的离子方程式:_______ 。
(5)配成的甲溶液物质的量浓度是_______ 。
①取mg甲的晶体溶于蒸馏水,配成500mL溶液;
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224mL。

回答下列问题:
(1)D在元素周期表中的位置为
(2)经测定晶体甲的摩尔质量为453g∙mol﹣1,其中阳离子和阴离子物质的量之比为1:1,且1mol甲晶体中含有12mol结晶水。则晶体甲的化学式为
(3)图象中V(Oa):V(ab):V(bc)=
(4)写出ab段发生反应的离子方程式:
(5)配成的甲溶液物质的量浓度是
您最近一年使用:0次



