名校
1 . 随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。

请回答下列问题:
(1)f在周期表中的位置为______________ ;x形成的阴离子的结构示意图为_____________________ 。
(2)比较d、e常见离子的半径大小:__________________ (填化学式,下同);比较g、h的最高价氧化物对应水化物的酸性强弱:_______________________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为__________________________ 。
②能形成共价化合物,写出其中一种的结构简式____________________________ 。

请回答下列问题:
(1)f在周期表中的位置为
(2)比较d、e常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近一年使用:0次
2017-10-15更新
|
1327次组卷
|
6卷引用:湖南三湘名校教育联盟2018届高三第一次大联考化学试题
湖南三湘名校教育联盟2018届高三第一次大联考化学试题湖北省鄂州市2018-2019学年高二高中质量监测化学试题苏教版高一化学必修2专题一第一单元《原子核外电子排布与元素周期律》单元检测(夯基提能)山西省长治市2019-2020学年高一下学期第一次在线月考化学试题吉林省白城市第四中学2019-2020学年高一下学期网上阶段检测化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
2 . 我国科学家在金刚石压腔实验中创造出了前所未见的化合物X,在超过113 GPa的压力下能够保持稳定。X在一定条件下完全分解为A(气体)和B,A的密度约为0.18 g·L−1;B是短周期中最活泼的金属;Y为含有C元素的气态氧化物,能使品红溶液褪色,E为常见无机物,Y与E以1∶1发生化合反应生成F,F仅含三种元素,是常用的食品抗氧化剂之一(假设反应过程无损耗,题中均为短周期元素,A、B、C为单质,气体数据均为标准状况下测定)。根据如下转化,回答下列问题:
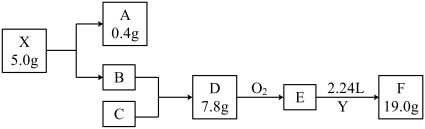
(1) 图中C在元素周期表中的位置是________ 。
(2) D的电子式为________ 。
(3) X的化学式为________ 。
(4) E→F的化学方程式为________ 。

(1) 图中C在元素周期表中的位置是
(2) D的电子式为
(3) X的化学式为
(4) E→F的化学方程式为
您最近一年使用:0次
2019-11-18更新
|
540次组卷
|
3卷引用:浙江省宁波市2020年新高考选考适应性考试化学试题
3 . 短周期元素W、X、Y、Z、M的原子序数依次增大,元素W的一种核素的中子数为0,X原子的最外层电子数是次外层的2倍,Z与M同主族,Z2﹣的电子层结构与氖原子相同。请回答下列问题:
(1)M在元素周期表中的位置_____ 。
(2)化合物p由W、X、Y、M四种元素组成。已知:向p溶液中加入FeCl3溶液,溶液变为血红色;向p溶液中加入NaOH溶液并加热,放出使湿润的红色石蕊试纸变蓝的气体。则p的化学式为_____ 。
(3)由X、Z、M三种元素可组成物质q,q的分子结构类似于CO2,则q的结构式为_____ 。
(4)(XY)2的化学性质与Cl2相似。常温下,(XY)2与NaOH溶液反应的离子方程式为_____ 。
(5)常温下,1mol Z3能与Y的最简单氢化物反应,生成一种常见的盐和1mol Z2,该反应的化学方程式为_____ 。
(1)M在元素周期表中的位置
(2)化合物p由W、X、Y、M四种元素组成。已知:向p溶液中加入FeCl3溶液,溶液变为血红色;向p溶液中加入NaOH溶液并加热,放出使湿润的红色石蕊试纸变蓝的气体。则p的化学式为
(3)由X、Z、M三种元素可组成物质q,q的分子结构类似于CO2,则q的结构式为
(4)(XY)2的化学性质与Cl2相似。常温下,(XY)2与NaOH溶液反应的离子方程式为
(5)常温下,1mol Z3能与Y的最简单氢化物反应,生成一种常见的盐和1mol Z2,该反应的化学方程式为
您最近一年使用:0次
名校
4 . X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的名称为__________________________ ;五种元素的原子半径从大到小的顺序为______________________________ (用元素符号表示)。
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,工业合成A的化学方程式为______________________________ ,B的结构式为_____________________ 。在标准状况下,将A充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面上升,(假设溶质不扩散)最后烧瓶内溶液中溶质的物质的量浓度为________ (精确到0.001)。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则其最高价氧化物对应水化物的化学式为__________________ 。
回答下列问题:
(1)L的名称为
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,工业合成A的化学方程式为
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则其最高价氧化物对应水化物的化学式为
您最近一年使用:0次
名校
5 . 离子化合物A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的最外层结构。请回答:
(1)试写出A的阳离子及阴离子的化学式________ 、________
(2)适当加热,A就分解为两种气体,其中一种气体是化合物,该反应的化学方程式为________ 。
(3)A溶于水后生成一种化合物和一种单质,则A的水溶液呈________ 性(酸/碱/中),原因:________
(1)试写出A的阳离子及阴离子的化学式
(2)适当加热,A就分解为两种气体,其中一种气体是化合物,该反应的化学方程式为
(3)A溶于水后生成一种化合物和一种单质,则A的水溶液呈
您最近一年使用:0次
名校
6 . 随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
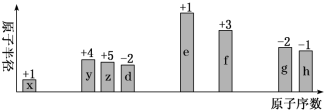
根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
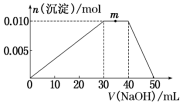
(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________ 。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是
(2)写出m点反应的离子方程式:
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
2018-09-24更新
|
250次组卷
|
4卷引用:安徽省阜阳市临泉县第一中学2019届高三上学期第三次模拟(12月)化学试题
2008·重庆·高考真题
真题
名校
7 . 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 molXY2含有54 mol电子。
(1)该融雪剂的化学式是_______ ;X与氢元素形成的化合物的电子式是_______ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_______ ;D与E能形成一种非极性分子,该分子的结构式为_______ ;D所在族元素的氢化物中,沸点最低的是_______ 。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是_______ 。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为_______ 。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为
您最近一年使用:0次
2016-12-09更新
|
903次组卷
|
4卷引用:2011届嘉禾一中高三第一次摸底考试化学卷
(已下线)2011届嘉禾一中高三第一次摸底考试化学卷2008年普通高等学校招生统一考试理综试题化学部分(重庆卷)(已下线)2012届陕西省师大附中高三10月份月考化学试卷安徽省郎溪中学、泾县中学2020-2021学年高一下学期3月联考化学试题
2010·上海普陀·二模
8 . 下面是元素周期表的前三周期。请用相应的化学用语回答下列问题:
(1)写出由e形成的两种阴离子的符号,它们带有相同的电荷数:______ 、_____ ;
(2)h的单质能与g元素的最高价氧化物对应水化物的溶液反应,请写出该反应的化学方程式________

(注:序列与b、c、d、e、f 并不一一对应)
(3)上左图表示的是b、c、d、e、f的氢化物的沸点(℃)。序列 “5”的氢化物是由______ 键构成的______ 分子(均填写“极性”或“非极性”)。由c和 e 组成的可灭火的物质的电子式是_______ 。
(4)上图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则柱形“8”熔点最高的原因是__________ 。
| a | |||||||
| b | c | d | e | f | |||
| g | h |
(1)写出由e形成的两种阴离子的符号,它们带有相同的电荷数:
(2)h的单质能与g元素的最高价氧化物对应水化物的溶液反应,请写出该反应的化学方程式

(注:序列与b、c、d、e、f 并不一一对应)
(3)上左图表示的是b、c、d、e、f的氢化物的沸点(℃)。序列 “5”的氢化物是由
(4)上图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则柱形“8”熔点最高的原因是
您最近一年使用:0次
名校
9 . A、B、C、D、E、F是六种短周期的主族元素,原子序数依次增大,A是IA族的非金属元素,B元素的最高价氧化物的水化物与其简单气态氢化物可反应生成盐,C是短周期中原子半径最大的元素,D元素原子L层电子数和M层电子数之差等于B元素最外层电子数,E元素最高正价和最低负价代数和等于4,据此回答下列问题:
(1)F元素在周期表中的位置__________ ,C原子结构示意图______________ 。
(2)A、B两元素可形成18电子的分子,该分子的电子式为_______________ 。
(3)A和氧元素形成的简单化合物,其熔沸点高于A和E形成的简单化合物,原因是____________ 。
(4)C、D、F可形成复杂化合物C[DF4],该化合物含有的化学键类型为________________ 。
(5)仅有上述元素形成的化合物或单质间的某些反应,可用以说明E和F两元素非金属性的强弱,写出其中一个离子反应方程式__________________________________ 。
(6)写出C、D两元素最高价氧化物的水化物反应的离子方程式____________________ 。
(1)F元素在周期表中的位置
(2)A、B两元素可形成18电子的分子,该分子的电子式为
(3)A和氧元素形成的简单化合物,其熔沸点高于A和E形成的简单化合物,原因是
(4)C、D、F可形成复杂化合物C[DF4],该化合物含有的化学键类型为
(5)仅有上述元素形成的化合物或单质间的某些反应,可用以说明E和F两元素非金属性的强弱,写出其中一个离子反应方程式
(6)写出C、D两元素最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
2011·浙江嘉兴·一模
10 . 中学常见反应的化学方程式是A+B→X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1∶4.请回答:
(1)若Y是黄绿色气体,则Y的电子式是__________ ,该反应的化学方程式是__________ 。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是__________ 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在周期表中的位置是_________ (填所在周期和族);Y的化学式是__________________ 。
②含a mol x的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是_________ mol。
(4)若A、B、X、Y均为化合物,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色,则A与B按物质的量之比1∶4恰好反应后,溶液中离子浓度从大到小的顺序是__________________
(1)若Y是黄绿色气体,则Y的电子式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在周期表中的位置是
②含a mol x的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是
(4)若A、B、X、Y均为化合物,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色,则A与B按物质的量之比1∶4恰好反应后,溶液中离子浓度从大到小的顺序是
您最近一年使用:0次
2016-12-09更新
|
477次组卷
|
3卷引用:2011届浙江省海盐元济高级中学高三高考全真压轴考试(理综)化学试题
(已下线)2011届浙江省海盐元济高级中学高三高考全真压轴考试(理综)化学试题2016届河北省衡水中学高三上学期四调考试化学试卷湖北省鄂东南省级示范高中教育教学改革联盟学校2018届高三上学期期中联考化学试题



