1 . 随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以CO2和NH3为原料合成尿素2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
(1)有利于提高CO2平衡转化率的措施是_______(填序号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图甲所示:
第一步: 2NH3(g)+CO2(g) NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1
第二步:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ∆H2
CO(NH2)2(s)+H2O(g) ∆H2
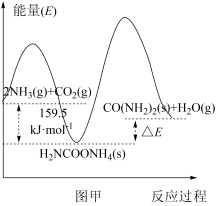
①图中ΔE=_______ kJ/mol。
②反应速率较快的是_______ 反应(填“第一步”或“第二步”),理由是_______ 。
II.以CO2和CH4催化重整制备合成气: CO2(g)+CH4(g) 2CO(g)+ 2H2(g)。
(3)在密闭容器中通入物质的量均为0.2 mol的CH4和CO2,在一定条件下发生反应CH4(g) +CO2 (g) 2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
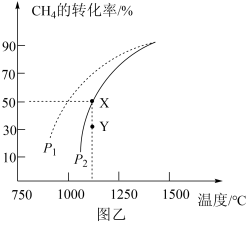
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是_______ (填序号)。
A容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C.反应速率: 2v正(CO2)=v正 (H2) D.同时断裂2molC- H键和1 molH-H键
②由图乙可知,压强P1_______ P2 (填“>”“<”或“=”,下同); Y点速率v正_______ v逆。
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,则X点对应温度下的Kp=_______ (用含P2的代数式表示)。
III. 电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:
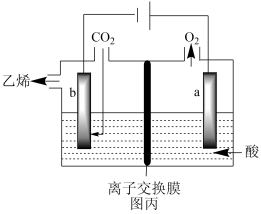
(4)阴极电极反应式为_______ ,该装置中使用的是_______ (填“阴”或“阳”)离子交换膜。
I.以CO2和NH3为原料合成尿素2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。(1)有利于提高CO2平衡转化率的措施是_______(填序号)。
| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
第一步: 2NH3(g)+CO2(g)
 NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1第二步:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ∆H2
CO(NH2)2(s)+H2O(g) ∆H2
①图中ΔE=
②反应速率较快的是
II.以CO2和CH4催化重整制备合成气: CO2(g)+CH4(g) 2CO(g)+ 2H2(g)。
(3)在密闭容器中通入物质的量均为0.2 mol的CH4和CO2,在一定条件下发生反应CH4(g) +CO2 (g)
 2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
A容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C.反应速率: 2v正(CO2)=v正 (H2) D.同时断裂2molC- H键和1 molH-H键
②由图乙可知,压强P1
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,则X点对应温度下的Kp=
III. 电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应式为
您最近一年使用:0次
2022-05-12更新
|
3102次组卷
|
3卷引用:四川省南充市2022届高三适应性考试(三诊)理综化学试题
名校
解题方法
2 . 根据所学知识,回答下列问题。
(1)向 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为_______ 。
(2)已知:①
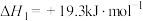
②
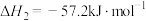
③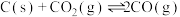
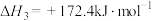
碳与水制氢气总反应的热化学方程式是_______ 。
(3)已知CO与 合成甲醇反应过程中的能量变化如图所示:
合成甲醇反应过程中的能量变化如图所示:

下表为断裂1mol化学键所需的能量数据:
则甲醇中C—H键的键能为_______  。
。
(4)一定条件下,在水溶液中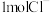 、
、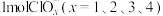 的相对能量(kJ)大小如图所示:
的相对能量(kJ)大小如图所示:

①D是_______ (填离子符号)。
②反应B→A+C的热化学方程式为_______ (用离子符号表示)。
(5)汽车发动机工作时会引发 和
和 反应,其能量变化示意图如下:
反应,其能量变化示意图如下:
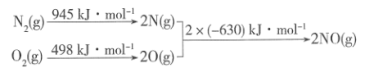
写出该反应的热化学方程式:_______ 。
(1)向
 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为(2)已知:①

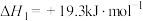
②

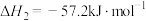
③
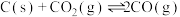
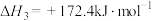
碳与水制氢气总反应的热化学方程式是
(3)已知CO与
 合成甲醇反应过程中的能量变化如图所示:
合成甲醇反应过程中的能量变化如图所示:
下表为断裂1mol化学键所需的能量数据:
| 化学键 | H—H |  | H—O | C—O |
| 断裂1mol化学键所需的能量/kJ | 436 | 1084 | 465 | 343 |
 。
。(4)一定条件下,在水溶液中
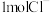 、
、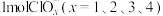 的相对能量(kJ)大小如图所示:
的相对能量(kJ)大小如图所示:
①D是
②反应B→A+C的热化学方程式为
(5)汽车发动机工作时会引发
 和
和 反应,其能量变化示意图如下:
反应,其能量变化示意图如下: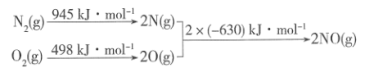
写出该反应的热化学方程式:
您最近一年使用:0次
2022-09-04更新
|
1936次组卷
|
4卷引用:河北省衡水中学2023届高三上学期三调考试化学试题
河北省衡水中学2023届高三上学期三调考试化学试题第一章化学反应的热效应(已下线)【知识图鉴】单元讲练测选择性必修1第1单元03巩固练江苏省连云港市东海县石榴高级中学2022-2023学年高二上学期第一次学情测试化学试题
真题
解题方法
3 . (1)用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰,原因是______ 。
(2)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF3熔点比GaCl3熔点高很多的原因是______ 。
(2)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
| GaF3 | GaCl3 | GaBr3 | |
| 熔点/℃ | > 1000 | 77. 75 | 122. 3 |
您最近一年使用:0次
2021-01-09更新
|
3985次组卷
|
12卷引用:2021年1月浙江高考化学试题变式题26-31
(已下线)2021年1月浙江高考化学试题变式题26-31浙江省金华市曙光学校2021-2022学年高三下学期5月模拟考试化学试题2021年1月新高考浙江化学高考真题(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题08.微粒间相互作用力-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
真题
名校
4 . 吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
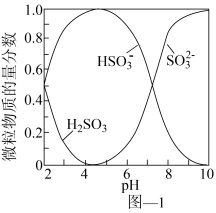
(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为___________ ;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是_____________ (填化学式)。
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是____________ (填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为_______________ 。

(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO 生成速率越大,其主要原因是
生成速率越大,其主要原因是__________ ;随着氧化的进行,溶液的pH将__________ (填“增大”、“减小”或“不变”)。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。

(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是

(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO
 生成速率越大,其主要原因是
生成速率越大,其主要原因是
您最近一年使用:0次
2020-07-11更新
|
5738次组卷
|
11卷引用:2020年江苏卷化学高考真题变式题16-21
(已下线)2020年江苏卷化学高考真题变式题16-212020年江苏卷化学高考试题(已下线)专题14 化学反应原理综合-2020年高考真题和模拟题化学分项汇编河南省郑州市巩义市第四高级中学2021届高三上学期期中考试化学试题江苏省苏州中学2020-2021学年高一下学期期初化学试卷陕西省汉中中学2021-2022学年高二上学期第三次月考化学试题黑龙江省密山市第四中学2021-2022学年高三上学期第二次月考化学试题湖南省临湘市第五中学2021-2022学年高二上学期第三次月考化学试题湖北省武汉外国语学校2022-2023学年高二上学期期末考试化学试题 (已下线)热点题型训练 化学与STSE(已下线)溶液中的离子平衡
名校
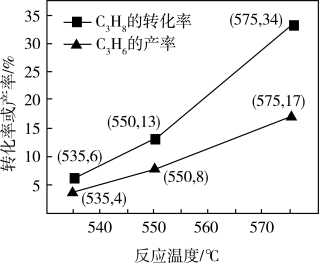
5 . 丙烯是重要的化工原料,可用于生产丙醇、卤代烃和塑料。
(1)工业上用丙烯加成法制各1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理为:
Ⅰ.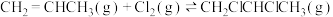
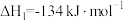
Ⅱ.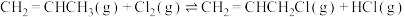
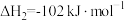
则

_______  。
。
(2)某研究小组向密闭容器中充入一定量的 和
和 ,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得
,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。
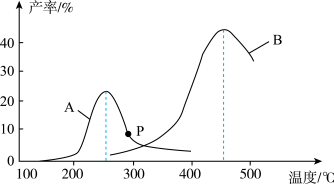
①下列说法错误的是_______ (填代号)
A.使用催化剂A的最佳温度约为250℃
B.相同条件下,改变压强不影响 的产率
的产率
C.两种催化剂均能降低反应的活化能,但△H不变
D.P点可能为对应温度下 的平衡产率
的平衡产率
②在催化剂A作用下,温度低于200℃时, 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是_______ 。
(3) 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。
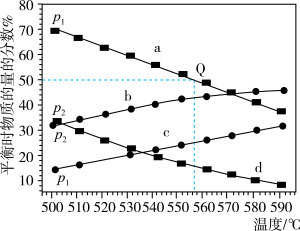
①a、d代表_______ (填“丙烷”或“丙烯”),
_______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
②起始时充入一定量丙烷,在恒压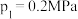 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为_______ (保留1位小数),该反应的平衡常数
_______ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)丙烷氧化脱氢法制备丙烯的反应: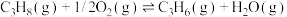
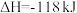
 ,过程中还生成CO、
,过程中还生成CO、 等副产物。
等副产物。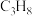 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。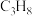 的转化率如图变化的原因是
的转化率如图变化的原因是_______ 。
(1)工业上用丙烯加成法制各1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理为:
Ⅰ.
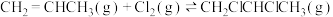
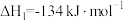
Ⅱ.
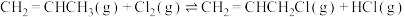
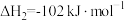
则


 。
。(2)某研究小组向密闭容器中充入一定量的
 和
和 ,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得
,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。
①下列说法错误的是
A.使用催化剂A的最佳温度约为250℃
B.相同条件下,改变压强不影响
 的产率
的产率C.两种催化剂均能降低反应的活化能,但△H不变
D.P点可能为对应温度下
 的平衡产率
的平衡产率②在催化剂A作用下,温度低于200℃时,
 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是(3)
 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。
①a、d代表

 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。②起始时充入一定量丙烷,在恒压
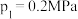 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为
(4)丙烷氧化脱氢法制备丙烯的反应:
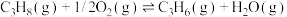
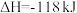
 ,过程中还生成CO、
,过程中还生成CO、 等副产物。
等副产物。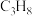 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。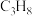 的转化率如图变化的原因是
的转化率如图变化的原因是
您最近一年使用:0次
2022-11-15更新
|
2084次组卷
|
5卷引用:模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
(已下线)模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)广东省广州市广雅中学2022-2023学年高二上学期期中考试化学试题广东省佛山市南海区狮山石门高级中学2022-2023学年高二下学期3月月考化学试题广东省广州天省实验学校2022-2023学年高二上学期期末考试化学试题(已下线)题型01 化学反应速率与化学平衡的图像分析-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
真题
解题方法
6 . (1)已知3种原子晶体的熔点数据如下表:
金刚石熔点比晶体硅熔点高的原因是_______ 。
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是_______ 。
| 金刚石 | 碳化硅 | 晶体硅 | |
| 熔点/℃ | >3550 | 2600 | 1415 |
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是
您最近一年使用:0次
2021-06-15更新
|
3688次组卷
|
9卷引用:2021年6月浙江高考化学试题变式题26-31
(已下线)2021年6月浙江高考化学试题变式题26-312021年6月新高考浙江化学高考真题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题08.微粒间相互作用力-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
7 . 铁元素存在多种价态,且不同价态的铁元素在一定条件下可以相互转化。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式___________ 。
(2) 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。
① 中铁元素的化合价为
中铁元素的化合价为___________ ,当有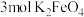 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为___________  。
。
②发生相应反应的离子方程式为___________ 。
(3)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。

①X不能是硝酸,原因是___________ ,装置4的作用是___________ 。
②实验开始时,开关 应
应___________ (填“打开”成“关闭”);这样操作的目的是___________ 。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式
(2)
 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。①
 中铁元素的化合价为
中铁元素的化合价为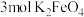 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为 。
。②发生相应反应的离子方程式为
(3)某同学设计如图装置制备一定量的
 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
①X不能是硝酸,原因是
②实验开始时,开关
 应
应
您最近一年使用:0次
8 . 次氯酸钠溶液和二氯异氰尿酸钠(C3N3O3Cl2Na)都是常用的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是__________________ 。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为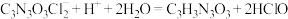


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品_______ 。(写出计算过程,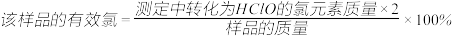 )
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________ (填“偏高”或“偏低”)。
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为
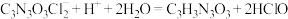


准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用
 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。①通过计算判断该样品是否为优质品
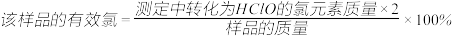 )
)②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
您最近一年使用:0次
2020-07-11更新
|
5083次组卷
|
16卷引用:2020年江苏卷化学高考真题变式题16-21
(已下线)2020年江苏卷化学高考真题变式题16-212020年江苏卷化学高考试题(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编江苏省苏州中学2020-2021学年高一下学期期初化学试卷(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记(已下线)小题25 定量实验 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)甘肃省天水市一中2022届高三上学期8月第一次考试化学试题江苏省徐州市王杰中学2021-2022学年高三10月学情调研化学试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点52 定量分析-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)实验综合题
9 . 燃煤烟气中SO2和NOx是大气污染物的主要来源,脱硫脱硝技术是烟气治理技术的研究热点。
(1)尿素/H2O2溶液脱硫脱硝。尿素[CO(NH2)2]是一种强还原剂。60℃时在一定浓度的尿素/H2O2溶液中通入含有SO2和NO的烟气,烟气中有毒气体被一定程度吸收。尿素/H2O2溶液对SO2具有很高的去除效率,写出尿素和H2O2溶液吸收SO2,生成硫酸铵和CO2的化学方程式为____ 。
(2)除去烟气中的NOx,利用氢气选择性催化还原(H2—SCR)是目前消除NO的理想方法。H2—SCR法的主反应:2NO(g)+2H2(g)=N2(g)+2H2O(g) △H1
副反应:2NO(g)+H2(g)=N2O(g)+H2O(g) △H2<0
①已知H2(g)+ O2(g)=H2O(g) △H3=-241.5kJ·mol-1
O2(g)=H2O(g) △H3=-241.5kJ·mol-1
N2(g)+O2(g)=2NO(g) △H4=+180.5kJ·mol-1
则△H1=____ kJ·mol-1。
②H2—SCR在Pt—HY催化剂表面的反应机理如图所示:
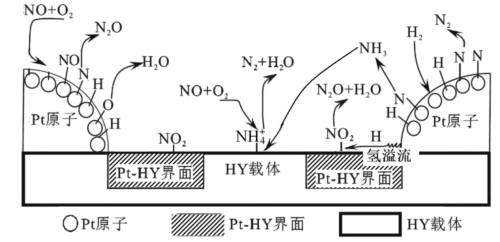
已知在HY载体表面发生反应的NO、O2物质的量之比为4∶1,反应中每生成1molN2,转移的电子的物质的量为___ mol。
(3)V2O5/炭基材料(活性炭、活性焦、活炭纤维)也可以脱硫脱硝。V2O5/炭基材料脱硫原理是:SO2在炭表面被吸附,吸附态SO2在炭表面被催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫时,通过红外光谱发现,脱硫开始后催化剂表面出现了VOSO4的吸收峰,再通入O2后VOSO4吸收峰消失,该脱硫反应过程可描述为____ 。
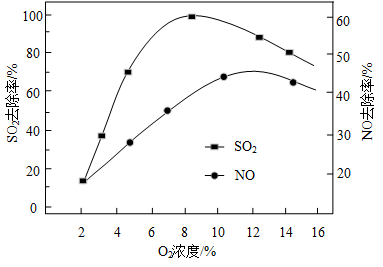
②V2O5/炭基材料脱硫时,控制一定气体流速和温度,考察了烟气中O2的存在对V2O5/炭基材料催化剂脱硫脱硝活性的影响,结果如图所示,当O2浓度过高时,去除率下降,其可能原因是_____ 。
(1)尿素/H2O2溶液脱硫脱硝。尿素[CO(NH2)2]是一种强还原剂。60℃时在一定浓度的尿素/H2O2溶液中通入含有SO2和NO的烟气,烟气中有毒气体被一定程度吸收。尿素/H2O2溶液对SO2具有很高的去除效率,写出尿素和H2O2溶液吸收SO2,生成硫酸铵和CO2的化学方程式为
(2)除去烟气中的NOx,利用氢气选择性催化还原(H2—SCR)是目前消除NO的理想方法。H2—SCR法的主反应:2NO(g)+2H2(g)=N2(g)+2H2O(g) △H1
副反应:2NO(g)+H2(g)=N2O(g)+H2O(g) △H2<0
①已知H2(g)+
 O2(g)=H2O(g) △H3=-241.5kJ·mol-1
O2(g)=H2O(g) △H3=-241.5kJ·mol-1N2(g)+O2(g)=2NO(g) △H4=+180.5kJ·mol-1
则△H1=
②H2—SCR在Pt—HY催化剂表面的反应机理如图所示:

已知在HY载体表面发生反应的NO、O2物质的量之比为4∶1,反应中每生成1molN2,转移的电子的物质的量为
(3)V2O5/炭基材料(活性炭、活性焦、活炭纤维)也可以脱硫脱硝。V2O5/炭基材料脱硫原理是:SO2在炭表面被吸附,吸附态SO2在炭表面被催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫时,通过红外光谱发现,脱硫开始后催化剂表面出现了VOSO4的吸收峰,再通入O2后VOSO4吸收峰消失,该脱硫反应过程可描述为
②V2O5/炭基材料脱硫时,控制一定气体流速和温度,考察了烟气中O2的存在对V2O5/炭基材料催化剂脱硫脱硝活性的影响,结果如图所示,当O2浓度过高时,去除率下降,其可能原因是

您最近一年使用:0次
2022-03-05更新
|
1533次组卷
|
7卷引用:黄金卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)
(已下线)黄金卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)必刷卷02-2022年高考化学考前信息必刷卷(江苏专用)江苏南京师范大学附属中学2022-2023学年高三一模适应性考试化学试题(已下线)化学-2023年高考押题预测卷03(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省六校2021-2022学年高三下学期期初联合调研考试化学试题(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)专题17 原理综合题
名校
解题方法
10 . 黄金是一种非常重要的金属。不仅是用于储备和投资的特殊通货,同时又是首饰业、电子业、现代通讯。航天航空业等部门的重要材料。
(1)金能溶解于王水中: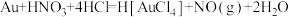 ,请分析
,请分析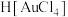 中
中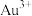 的配体是
的配体是___________ ,配位数是___________ 。
(2)开采的金矿可用氰化法提取:先以氰化钠(NaCN)溶液处理粉碎的金矿石得到 ,再用锌还原:
,再用锌还原: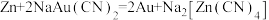 。Zn与
。Zn与 形成的配离子为正四面体形,Au(+1价)与
形成的配离子为正四面体形,Au(+1价)与 形成的配离子为直线形。
形成的配离子为直线形。
① 中配合离子
中配合离子 中σ键和π键个数之比是
中σ键和π键个数之比是___________ ,配体 杂化方式是
杂化方式是___________ 。
②写出Zn的电子排布式___________ ,C、N、Na的第一电离能由大到小顺序为___________ 。
(3)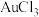 是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,它都是以二聚体
是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,它都是以二聚体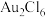 的形式存在。依据以上信息判断
的形式存在。依据以上信息判断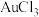 晶体的结构属于
晶体的结构属于___________ 晶体,写出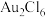 的结构式
的结构式___________ 。
(4)①Au单质的晶体为面心立方最密堆积,Au的配位数为___________ 。以下金属和金具有相同的堆积模型的是___________ 。
a.Po b.Na c.Zn d.Cu
②若Au的原子半径为a nm,Au单质的摩尔质量为M g/mol,阿伏加德罗常数为NA,求Au单质的密度为
___________  。(用含a、NA、M的代数式表示)
。(用含a、NA、M的代数式表示)
(1)金能溶解于王水中:
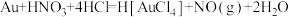 ,请分析
,请分析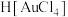 中
中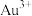 的配体是
的配体是(2)开采的金矿可用氰化法提取:先以氰化钠(NaCN)溶液处理粉碎的金矿石得到
 ,再用锌还原:
,再用锌还原: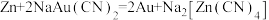 。Zn与
。Zn与 形成的配离子为正四面体形,Au(+1价)与
形成的配离子为正四面体形,Au(+1价)与 形成的配离子为直线形。
形成的配离子为直线形。①
 中配合离子
中配合离子 中σ键和π键个数之比是
中σ键和π键个数之比是 杂化方式是
杂化方式是②写出Zn的电子排布式
(3)
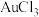 是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,它都是以二聚体
是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,它都是以二聚体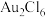 的形式存在。依据以上信息判断
的形式存在。依据以上信息判断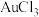 晶体的结构属于
晶体的结构属于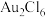 的结构式
的结构式(4)①Au单质的晶体为面心立方最密堆积,Au的配位数为
a.Po b.Na c.Zn d.Cu
②若Au的原子半径为a nm,Au单质的摩尔质量为M g/mol,阿伏加德罗常数为NA,求Au单质的密度为

 。(用含a、NA、M的代数式表示)
。(用含a、NA、M的代数式表示)
您最近一年使用:0次
2022-01-30更新
|
1541次组卷
|
3卷引用:广西柳州市2022届高三第二次模拟考试理科综合化学试题
广西柳州市2022届高三第二次模拟考试理科综合化学试题湖南省怀化市沅陵县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)第十二章 物质结构与性质(测)-2023年高考化学一轮复习讲练测(全国通用)



