真题
1 . 学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______ ,装置B的作用为_______ 。 反应的探究如下:
反应的探究如下:_______ ;产生的气体为_______ 。比较实验①和②,从氧化还原角度说明 的作用是
的作用是_______ 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,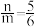 。X的化学式为
。X的化学式为_______ 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
标准溶液15.00mL。(已知: ,
, )标志滴定终点的现象是
)标志滴定终点的现象是_______ ,粗品中X的相对含量为_______ 。
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为

 反应的探究如下:
反应的探究如下:
 的作用是
的作用是(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,
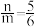 。X的化学式为
。X的化学式为(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用
 标准溶液滴定,滴定终点时消耗
标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
标准溶液15.00mL。(已知: ,
, )标志滴定终点的现象是
)标志滴定终点的现象是
您最近一年使用:0次
2023-06-14更新
|
8264次组卷
|
18卷引用:四川省眉山市仁寿第一中学校(北校区)2023-2024学年高三上学期11月期中考试理综化学试题
四川省眉山市仁寿第一中学校(北校区)2023-2024学年高三上学期11月期中考试理综化学试题2023年高考湖北卷化学真题(已下线)专题19 实验综合题(已下线)T18-实验题(已下线)考点08 物质的量在化学方程式计算中的应用(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)第13讲氮及其化合物(已下线)考点16 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型二 实验中常考滴定计算-备战2024年高考化学答题技巧与模板构建(已下线)第03讲 物质的量在化学方程式计算中的应用(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)(已下线)专题12 化学实验综合题-【好题汇编】3年(2022-2024)高考1年模拟化学真题分类汇编(湖北专用)(已下线)暑假作业18 化学实验综合题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)(已下线)第04讲 金属材料及金属矿物的开发利用(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)(已下线)专题16 化学实验综合题-备战2025年高考化学真题题源解密(新高考通用)
真题
2 . 回答下列问题:
(1)两种有机物的相关数据如表:
HCON(CH3)2的相对分子质量比HCONH2的大,但其沸点反而比HCONH2的低,主要原因是______ 。
(2)四种晶体的熔点数据如表:
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是______ 。
(1)两种有机物的相关数据如表:
| 物质 | HCON(CH3)2 | HCONH2 |
| 相对分子质量 | 73 | 45 |
| 沸点/℃ | 153 | 220 |
(2)四种晶体的熔点数据如表:
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 熔点/℃ | -183 | -90 | -127 | >1000 |
您最近一年使用:0次
2022-01-12更新
|
4811次组卷
|
5卷引用:海南省五指山中学2021-2022学年高二下学期期中考试化学试题
海南省五指山中学2021-2022学年高二下学期期中考试化学试题2022 年1月浙江省普通高校招生选考科目考试化学试题(已下线)2022年浙江1月高考真题变式题(26-31)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
3 . 随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以CO2和NH3为原料合成尿素2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
(1)有利于提高CO2平衡转化率的措施是_______(填序号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图甲所示:
第一步: 2NH3(g)+CO2(g) NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1
第二步:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ∆H2
CO(NH2)2(s)+H2O(g) ∆H2
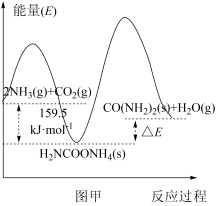
①图中ΔE=_______ kJ/mol。
②反应速率较快的是_______ 反应(填“第一步”或“第二步”),理由是_______ 。
II.以CO2和CH4催化重整制备合成气: CO2(g)+CH4(g) 2CO(g)+ 2H2(g)。
(3)在密闭容器中通入物质的量均为0.2 mol的CH4和CO2,在一定条件下发生反应CH4(g) +CO2 (g) 2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
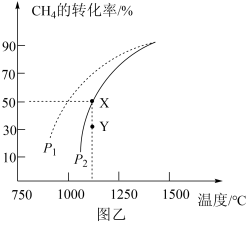
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是_______ (填序号)。
A容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C.反应速率: 2v正(CO2)=v正 (H2) D.同时断裂2molC- H键和1 molH-H键
②由图乙可知,压强P1_______ P2 (填“>”“<”或“=”,下同); Y点速率v正_______ v逆。
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,则X点对应温度下的Kp=_______ (用含P2的代数式表示)。
III. 电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:
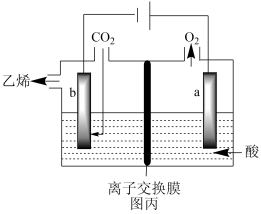
(4)阴极电极反应式为_______ ,该装置中使用的是_______ (填“阴”或“阳”)离子交换膜。
I.以CO2和NH3为原料合成尿素2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。
CO(NH2)2(s)+H2O(g) ∆H= -87 kJ/mol。(1)有利于提高CO2平衡转化率的措施是_______(填序号)。
| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
第一步: 2NH3(g)+CO2(g)
 NH2COONH4(s) ∆H1
NH2COONH4(s) ∆H1第二步:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ∆H2
CO(NH2)2(s)+H2O(g) ∆H2
①图中ΔE=
②反应速率较快的是
II.以CO2和CH4催化重整制备合成气: CO2(g)+CH4(g) 2CO(g)+ 2H2(g)。
(3)在密闭容器中通入物质的量均为0.2 mol的CH4和CO2,在一定条件下发生反应CH4(g) +CO2 (g)
 2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
2CO (g)+2H2(g),CH4的平衡转化率随温度、压强的变化关系如图乙所示。
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
A容器中混合气体的密度保持不变 B. 容器内混合气体的压强保持不变
C.反应速率: 2v正(CO2)=v正 (H2) D.同时断裂2molC- H键和1 molH-H键
②由图乙可知,压强P1
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,则X点对应温度下的Kp=
III. 电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应式为
您最近一年使用:0次
2022-05-12更新
|
3161次组卷
|
3卷引用:四川省眉山市仁寿县铧强中学2021-2022学年高二下学期期中考试化学试题
名校
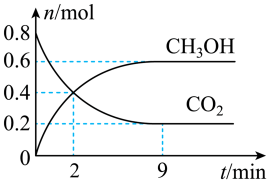
4 . 某温度下CO2加氢制甲醇的的总反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
(1)对于该反应,反应物的化学键断裂要吸收的能量_______ (填“大于”、“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)下列措施能加快反应速率的是_______ (填序号,下同)。
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为_______ ,2 min末时v正_______ v逆(填“<”“>”或“=”)。
(4)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为_______ 。
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为_______ 。
(1)对于该反应,反应物的化学键断裂要吸收的能量
(2)下列措施能加快反应速率的是
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为
(4)恒温恒容条件下,能说明反应已达平衡状态的是
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2
 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为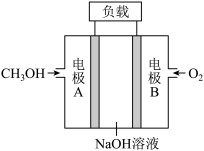
您最近一年使用:0次
2023-03-15更新
|
2165次组卷
|
7卷引用:【2023】【高一下】【其他】【余高1】【高中化学】【刘尼尼收集】
名校
5 . 在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。
(1) 是工业制硫酸的主要反应之一、该反应过程的能量变化如下图所示,则断开反应物中化学键吸收的能量
是工业制硫酸的主要反应之一、该反应过程的能量变化如下图所示,则断开反应物中化学键吸收的能量___________ 形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。 随时间的变化如下表:
随时间的变化如下表:
反应达到平衡时, 的转化率是
的转化率是___________ 。
(3)上图中表示 的变化的曲线是
的变化的曲线是___________ (填字母)。
(4)用 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
___________ 。
(5)下列能说明该反应已达化学平衡状态的是___________ 。
A.
B.单位时间内消耗2mol 的同时消耗1mol
的同时消耗1mol 
C.容器中 与
与 的物质的量之比
的物质的量之比
D.容器中 的体积分数不变
的体积分数不变
E.容器中气体的总物质的量不变
F.容器中气体的总质量不变
(6)能使该反应的反应速率增大的是___________。
(1)
 是工业制硫酸的主要反应之一、该反应过程的能量变化如下图所示,则断开反应物中化学键吸收的能量
是工业制硫酸的主要反应之一、该反应过程的能量变化如下图所示,则断开反应物中化学键吸收的能量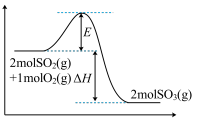
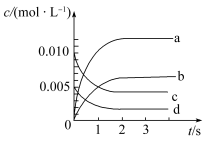
 随时间的变化如下表:
随时间的变化如下表:| 时间(S) | 0 | 1 | 2 | 3 | 4 | 5 |
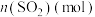 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 的转化率是
的转化率是(3)上图中表示
 的变化的曲线是
的变化的曲线是(4)用
 表示从0~2s内该反应的平均速率
表示从0~2s内该反应的平均速率
(5)下列能说明该反应已达化学平衡状态的是
A.

B.单位时间内消耗2mol
 的同时消耗1mol
的同时消耗1mol 
C.容器中
 与
与 的物质的量之比
的物质的量之比
D.容器中
 的体积分数不变
的体积分数不变E.容器中气体的总物质的量不变
F.容器中气体的总质量不变
(6)能使该反应的反应速率增大的是___________。
A.减少 气体的通入量 气体的通入量 | B.适当升高温度 |
| C.恒容下充入Ne | D.选择更高效催化剂 |
您最近一年使用:0次
2023-03-29更新
|
1788次组卷
|
8卷引用:福建省晋江市平山中学、内坑中学、磁灶中学、永春二中、永和中学2023-2024学年高二上学期期中联考化学试题
6 . 化学反应的速率与限度在社会生产、生活和科学研究中具有广泛的应用,对人类文明的进步和现代化建设具有重大的价值,与我们每个人息息相关。恒温条件下,在5L恒容密闭容器内充入1.5molX(g)与2.0molY(g),反应10min后达到平衡,此时X的物质的量减少1mol,Y的物质的量浓度为 ,0~10min内,生成Z的平均反应速率为
,0~10min内,生成Z的平均反应速率为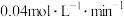 。请回答下列问题:
。请回答下列问题:
(1)该反应的化学方程式为__________________ 。
(2)0~10min内,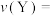
______ 
(3)反应达到平衡状态时,X、Y的转化率分别为______ (保留三位有效数字)。
(4)若改变下列一个条件,推测该反应的速率变化(填“增大”、“减小”或“不变”):
①将容器的体积扩大为10L,化学反应速率______ 。
②充入1mol氦气,化学反应速率______ 。
(5)下列说法能判断该反应达到平衡状态的是______(填标号)。
 ,0~10min内,生成Z的平均反应速率为
,0~10min内,生成Z的平均反应速率为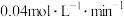 。请回答下列问题:
。请回答下列问题:(1)该反应的化学方程式为
(2)0~10min内,
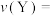

(3)反应达到平衡状态时,X、Y的转化率分别为
(4)若改变下列一个条件,推测该反应的速率变化(填“增大”、“减小”或“不变”):
①将容器的体积扩大为10L,化学反应速率
②充入1mol氦气,化学反应速率
(5)下列说法能判断该反应达到平衡状态的是______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 |
B. |
| C.容器内混合气体的压强不变 |
| D.容器内混合气体的密度不变 |
您最近一年使用:0次
2023-03-31更新
|
1810次组卷
|
5卷引用:期中模拟题(二)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)
(已下线)期中模拟题(二)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册) 宁夏回族自治区银川一中2022-2023学年高一下学期期中考试化学试题广东省部分名校2022-2023学年高一下学期3月大联考化学试题(已下线)期末模拟题(一)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)青海省西宁市第十四中学2023-2024学年高一下学期6月月考化学试卷
名校
7 . 物质在水中存在电离平衡、水解平衡。请根据所学知识回答:
(1)次磷酸( )是一种精细化工产品,向10mL
)是一种精细化工产品,向10mL  溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、
、 两种阴离子。
两种阴离子。
①写出 溶液与足量NaOH溶液反应后形成的正盐的化学式:
溶液与足量NaOH溶液反应后形成的正盐的化学式:___________ 。
②常温下, ,0.1mol/L的
,0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填序号)。
A. B.
B. C.
C.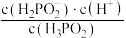
(2)25℃时,HF的电离常数为 ;
; 的电离常数为
的电离常数为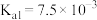 ,
, ,
, 。在
。在 溶液加入过量NaF溶液的离子反应方程式为
溶液加入过量NaF溶液的离子反应方程式为___________ 。
(3)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式说明);已知25℃时, 的
的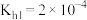 ,则当
,则当 溶液中
溶液中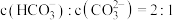 时,溶液的
时,溶液的
___________ 。
(4)某温度下,水的离子积常数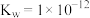 。该温度下,将
。该温度下,将 的HCl溶液与
的HCl溶液与 的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液
的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液 ,则盐酸溶液与NaOH溶液的体积比为
,则盐酸溶液与NaOH溶液的体积比为___________ 。
(5)相同物质的量浓度的五种溶液:① 、②氨水、③
、②氨水、③ 、④
、④ 、⑤
、⑤ ,
, 由大到小顺序是
由大到小顺序是___________ (用序号表示)。
(1)次磷酸(
 )是一种精细化工产品,向10mL
)是一种精细化工产品,向10mL  溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、
、 两种阴离子。
两种阴离子。①写出
 溶液与足量NaOH溶液反应后形成的正盐的化学式:
溶液与足量NaOH溶液反应后形成的正盐的化学式:②常温下,
 ,0.1mol/L的
,0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是A.
 B.
B. C.
C.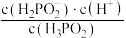
(2)25℃时,HF的电离常数为
 ;
; 的电离常数为
的电离常数为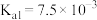 ,
, ,
, 。在
。在 溶液加入过量NaF溶液的离子反应方程式为
溶液加入过量NaF溶液的离子反应方程式为(3)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因: 的
的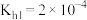 ,则当
,则当 溶液中
溶液中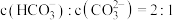 时,溶液的
时,溶液的
(4)某温度下,水的离子积常数
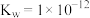 。该温度下,将
。该温度下,将 的HCl溶液与
的HCl溶液与 的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液
的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液 ,则盐酸溶液与NaOH溶液的体积比为
,则盐酸溶液与NaOH溶液的体积比为(5)相同物质的量浓度的五种溶液:①
 、②氨水、③
、②氨水、③ 、④
、④ 、⑤
、⑤ ,
, 由大到小顺序是
由大到小顺序是
您最近一年使用:0次
2023-10-13更新
|
1489次组卷
|
4卷引用:四川省成都外国语学校2023-2024学年高二上学期11月期中考试化学试题
名校
8 . 丙烯是重要的化工原料,可用于生产丙醇、卤代烃和塑料。
(1)工业上用丙烯加成法制各1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理为:
Ⅰ.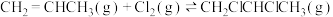
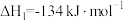
Ⅱ.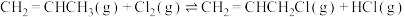
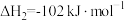
则

_______  。
。
(2)某研究小组向密闭容器中充入一定量的 和
和 ,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得
,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。
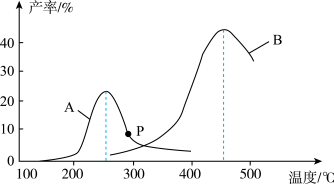
①下列说法错误的是_______ (填代号)
A.使用催化剂A的最佳温度约为250℃
B.相同条件下,改变压强不影响 的产率
的产率
C.两种催化剂均能降低反应的活化能,但△H不变
D.P点可能为对应温度下 的平衡产率
的平衡产率
②在催化剂A作用下,温度低于200℃时, 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是_______ 。
(3) 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。
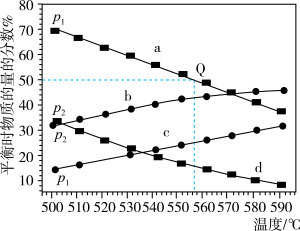
①a、d代表_______ (填“丙烷”或“丙烯”),
_______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
②起始时充入一定量丙烷,在恒压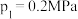 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为_______ (保留1位小数),该反应的平衡常数
_______ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)丙烷氧化脱氢法制备丙烯的反应: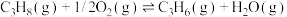
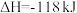
 ,过程中还生成CO、
,过程中还生成CO、 等副产物。
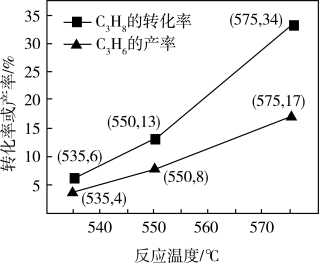
等副产物。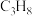 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。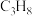 的转化率如图变化的原因是
的转化率如图变化的原因是_______ 。
(1)工业上用丙烯加成法制各1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理为:
Ⅰ.
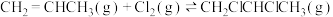
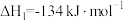
Ⅱ.
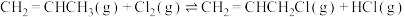
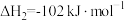
则


 。
。(2)某研究小组向密闭容器中充入一定量的
 和
和 ,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得
,分别在A、B两种不同催化剂作用下发生反应Ⅰ,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。
①下列说法错误的是
A.使用催化剂A的最佳温度约为250℃
B.相同条件下,改变压强不影响
 的产率
的产率C.两种催化剂均能降低反应的活化能,但△H不变
D.P点可能为对应温度下
 的平衡产率
的平衡产率②在催化剂A作用下,温度低于200℃时,
 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是(3)
 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。
①a、d代表

 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。②起始时充入一定量丙烷,在恒压
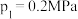 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为
(4)丙烷氧化脱氢法制备丙烯的反应:
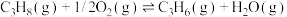
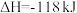
 ,过程中还生成CO、
,过程中还生成CO、 等副产物。
等副产物。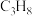 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。 的转化率如图变化的原因是
的转化率如图变化的原因是
您最近一年使用:0次
2022-11-15更新
|
2154次组卷
|
5卷引用:广东省广州市广雅中学2022-2023学年高二上学期期中考试化学试题
广东省广州市广雅中学2022-2023学年高二上学期期中考试化学试题(已下线)模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)广东省佛山市南海区狮山石门高级中学2022-2023学年高二下学期3月月考化学试题广东省广州天省实验学校2022-2023学年高二上学期期末考试化学试题(已下线)题型01 化学反应速率与化学平衡的图像分析-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
2023高一上·全国·专题练习
解题方法
9 . 配平下列方程式。
(1)____S+____KOH=____K2S+____K2SO3+____H2O;___________ 。
(2)____ +____H++____Cl-=____Mn2++____Cl2↑+____H2O;
+____H++____Cl-=____Mn2++____Cl2↑+____H2O;___________ 。
(1)____S+____KOH=____K2S+____K2SO3+____H2O;
(2)____
 +____H++____Cl-=____Mn2++____Cl2↑+____H2O;
+____H++____Cl-=____Mn2++____Cl2↑+____H2O;
您最近一年使用:0次
名校
解题方法
10 . I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过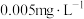 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉[ ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: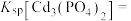
_______ 。
(2)一定温度下, 的
的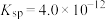 ,
, 的
的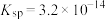 ,该温度下
,该温度下_______ [填“ ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。
(3)向某含镉废水中加入 ,当
,当 浓度达到
浓度达到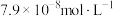 时,废水中
时,废水中 的浓度为
的浓度为____  [已知:
[已知: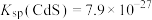 ],此时
],此时____ (填“符合”或“不符合”)《生活饮用水卫生标准》。
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,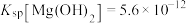 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为_______ 。
(5)常温下,向50mL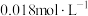 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。
①反应后,溶液中
_______  。
。
②反应后,溶液的
_______ 。
③如果向反应后的溶液中继续加入50mL 的盐酸,
的盐酸,____ (填“有”或“无”)白色沉淀生成。
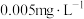 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。(1)写出磷酸镉[
 ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: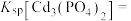
(2)一定温度下,
 的
的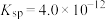 ,
, 的
的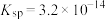 ,该温度下
,该温度下 ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。(3)向某含镉废水中加入
 ,当
,当 浓度达到
浓度达到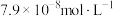 时,废水中
时,废水中 的浓度为
的浓度为 [已知:
[已知: ],此时
],此时II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,
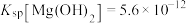 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:| pH |  | 8.0~9.6 | 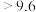 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为(5)常温下,向50mL
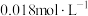 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。①反应后,溶液中

 。
。②反应后,溶液的

③如果向反应后的溶液中继续加入50mL
 的盐酸,
的盐酸,
您最近一年使用:0次
2022-09-04更新
|
1726次组卷
|
5卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期期中考试化学试题
黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期期中考试化学试题江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题第三章水溶液中的离子反应与平衡广东省揭阳市惠来县第一中学2022-2023学年高二上学期12月月考化学试题(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)



