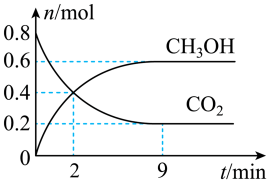
某温度下CO2加氢制甲醇的的总反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
(1)对于该反应,反应物的化学键断裂要吸收的能量_______ (填“大于”、“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)下列措施能加快反应速率的是_______ (填序号,下同)。
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为_______ ,2 min末时v正_______ v逆(填“<”“>”或“=”)。
(4)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为_______ 。
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为_______ 。
(1)对于该反应,反应物的化学键断裂要吸收的能量
(2)下列措施能加快反应速率的是
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为
(4)恒温恒容条件下,能说明反应已达平衡状态的是
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2
 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为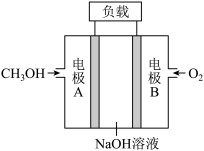
更新时间:2023-03-15 20:13:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,在容积为VL的密闭容器里进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中a∶b =__________________ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:__________________ 。
(3)t1时N的转化率为:_______________ ;
(4)下列①→⑩的说法中可以证明 H2(g)+I2(g) 2HI(g)已达平衡状态的是:
2HI(g)已达平衡状态的是:___________ 。
①单位时间内生成n molH2的同时生成n mol HI
②一个H-H 键断裂的同时有两个H-I键断裂
③质量分数:w(HI)=w(I2)
④容器内HI(g)、H2 (g) 、I2 (g)共存
⑤c(HI): c(H2): c(I2)=2:1:1
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,HI(g)浓度不再变化
⑧温度和压强一定时,混合气体的平均摩尔质量不再变化
⑨温度和压强一定时,混合气体的颜色不再发生变化
⑩温度和压强一定时,混合气体的密度不再变化
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中a∶b =
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)t1时N的转化率为:
(4)下列①→⑩的说法中可以证明 H2(g)+I2(g)
 2HI(g)已达平衡状态的是:
2HI(g)已达平衡状态的是:①单位时间内生成n molH2的同时生成n mol HI
②一个H-H 键断裂的同时有两个H-I键断裂
③质量分数:w(HI)=w(I2)
④容器内HI(g)、H2 (g) 、I2 (g)共存
⑤c(HI): c(H2): c(I2)=2:1:1
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,HI(g)浓度不再变化
⑧温度和压强一定时,混合气体的平均摩尔质量不再变化
⑨温度和压强一定时,混合气体的颜色不再发生变化
⑩温度和压强一定时,混合气体的密度不再变化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一体积为2L的密闭容器中充入1molN2、2molH2。在催化剂作用下发生可逆反应:N2(g)+3H2(g) 2NH3(g),NH3的物质的量随时间变化如图所示。回答下列问题:
2NH3(g),NH3的物质的量随时间变化如图所示。回答下列问题:

(1)0~1min的反应速率v1与2~3min的反应速率v2相比较,v1___ (填“>”“=”或“<”)v2,1~2min的反应速率v(H2)=___ mol·L-1·min-1.
(2)从图象可以看出,前3min内,1~2min反应速率最快,1~2min反应速率变快的原因是___ 。
(3)反应最大限度是在___ min时,此时密闭容器中总物质的量为___ mol。
(4)研究发现降低温度有利于平衡向生成NH3的方向移动,而工业实际采用在较高温度下进行反应的原因是___ 。
 2NH3(g),NH3的物质的量随时间变化如图所示。回答下列问题:
2NH3(g),NH3的物质的量随时间变化如图所示。回答下列问题:
(1)0~1min的反应速率v1与2~3min的反应速率v2相比较,v1
(2)从图象可以看出,前3min内,1~2min反应速率最快,1~2min反应速率变快的原因是
(3)反应最大限度是在
(4)研究发现降低温度有利于平衡向生成NH3的方向移动,而工业实际采用在较高温度下进行反应的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)  pC(g)+qD(g) 已知:平均反应速率vC=1/2vA;反应2 min时,A的浓度减少了1/3,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:
pC(g)+qD(g) 已知:平均反应速率vC=1/2vA;反应2 min时,A的浓度减少了1/3,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:
(1)反应2 min内,vA=___________ ,vB=___________ ;
(2)反应平衡时,D为2a mol,则B的转化率为___________ ;
(3)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH___________ 0(填“>”、“<” 或“=”);
(4) 如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:
①反应速率___________ (填“增大”、“减小”或“不变”)
②平衡时反应物的转化率___________ (填“增大”、“减小”或“不变”)
 pC(g)+qD(g) 已知:平均反应速率vC=1/2vA;反应2 min时,A的浓度减少了1/3,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:
pC(g)+qD(g) 已知:平均反应速率vC=1/2vA;反应2 min时,A的浓度减少了1/3,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:(1)反应2 min内,vA=
(2)反应平衡时,D为2a mol,则B的转化率为
(3)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH
(4) 如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:
①反应速率
②平衡时反应物的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)如图表示各物质浓度的变化曲线,A点处,v(正)___________ v(逆),A点正反应速率___________ B点正反应速率。(用“大于”“小于”或“等于”填空)。

(2)图中表示O2变化的曲线是___________ 。用NO2表示从0~2s内该反应的平均速率v=___________ 。
(3)能说明该反应已经达到平衡状态的是___________。
(4)能使该反应的反应速率增大的是___________。
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(2)图中表示O2变化的曲线是
(3)能说明该反应已经达到平衡状态的是___________。
| A.容器内颜色保持不变 | B.v(NO)=2v(O2) |
| C.容器内的密度保持不变 | D.NO的质量百分数不变 |
| A.适当升高温度 | B.选择高效的催化剂 |
| C.减小O2的浓度 | D.及时分离出NO2气体 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】浓度对反应速率影响得一般规律:增大反应物的浓度____ 化学反应速率,减小反应物的浓度____ 化学反应速率。
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐3】吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
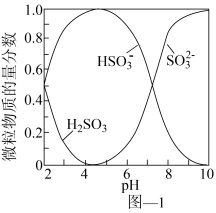
(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为___________ ;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是_____________ (填化学式)。
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是____________ (填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为_______________ 。

(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO 生成速率越大,其主要原因是
生成速率越大,其主要原因是__________ ;随着氧化的进行,溶液的pH将__________ (填“增大”、“减小”或“不变”)。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。

(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是

(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO
 生成速率越大,其主要原因是
生成速率越大,其主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】工业上利用 催化重整制
催化重整制 。在恒容密闭容器中发生反应:
。在恒容密闭容器中发生反应: 。
。
(1)在不改变物质浓度的条件下,加快该反应速率的措施有___________ (答出一点即可)。
(2)下列叙述中能说明该反应已达平衡状态的有___________。
(3)高温条件下,利用 还原
还原 的反应过程如图所示。该反应的催化剂是
的反应过程如图所示。该反应的催化剂是___________ 。写出反应ⅱ的化学方程式___________ 。

 催化重整制
催化重整制 。在恒容密闭容器中发生反应:
。在恒容密闭容器中发生反应: 。
。(1)在不改变物质浓度的条件下,加快该反应速率的措施有
(2)下列叙述中能说明该反应已达平衡状态的有___________。
A.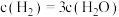 |
| B.混合气体的质量不再变化 |
C.单位时间内生成 ,同时消耗 ,同时消耗 |
| D.混合气体的压强不再变化 |
(3)高温条件下,利用
 还原
还原 的反应过程如图所示。该反应的催化剂是
的反应过程如图所示。该反应的催化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“三元催化转换器”是以汽油为燃料的汽车上的尾气处理装置,通过它可将汽车尾气中的有害物质转化为无害物质,发生的反应是2CO+2NO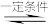 N2+2CO2。
N2+2CO2。
(1)T℃时,向5L容积固定的密闭容器中充入2molCO和2molNO发生以上反应,10min时测得容器中n(NO)=1mol,则在0~10min内,用N2的浓度变化表示的平均反应速率v(N2)=__ mol·L-1·min-1。
(2)能说明以上反应一定达到化学平衡的是__ (填序号)。
a.CO的浓度为0
b.NO的浓度不再改变
c.正反应速率与逆反应速率相等
d.CO与NO的物质的量之比为1∶1
(3)利用“三元催化转换器”可使以上反应的速率__ (填“增大”、“减小”或“无影响”),请再举出一种能起到相同作用的方法__ 。
(4)从图可以看出,影响上述反应进行程度的一个因素是__ ,为了促进NO更多地转化为生成物,可采取的措施是__ 。

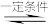 N2+2CO2。
N2+2CO2。(1)T℃时,向5L容积固定的密闭容器中充入2molCO和2molNO发生以上反应,10min时测得容器中n(NO)=1mol,则在0~10min内,用N2的浓度变化表示的平均反应速率v(N2)=
(2)能说明以上反应一定达到化学平衡的是
a.CO的浓度为0
b.NO的浓度不再改变
c.正反应速率与逆反应速率相等
d.CO与NO的物质的量之比为1∶1
(3)利用“三元催化转换器”可使以上反应的速率
(4)从图可以看出,影响上述反应进行程度的一个因素是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上制硝酸的主要反应是4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1
4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1
(1)该反应的平衡常数表达式为K=________ ;升高温度,K值______ (填“增大”或“减小”或 “不变”);升高温度,化学反应速率将______ (填“增大”或“减小” 或 “不变”)。
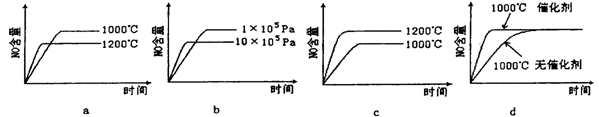
(2)若反应物起始的物质的量相同,下列关系图正确的是______ (填序号)。
(3)若达到平衡状态后升高温度则正反应速率和逆反应速率___________________ 。(填“同时增大”或“逆反应速率增大,正反应速率不变”)
(4)工业上合成氨气的反应N2(g)+3H2(g)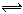 2NH3(g)ΔH<0 ,在密闭容器中反应达到平衡状态的标志是
2NH3(g)ΔH<0 ,在密闭容器中反应达到平衡状态的标志是_______ 。
①压强不再改变
②生成氨气的速率等于生成氮气的速率
③正反应速率等于零
④容器内气体的平均相对分子量不再改变
⑤单位时间内有3amolH-H的断裂的同时有6amolN-H断裂
 4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1
4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1(1)该反应的平衡常数表达式为K=
(2)若反应物起始的物质的量相同,下列关系图正确的是

(3)若达到平衡状态后升高温度则正反应速率和逆反应速率
(4)工业上合成氨气的反应N2(g)+3H2(g)
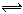 2NH3(g)ΔH<0 ,在密闭容器中反应达到平衡状态的标志是
2NH3(g)ΔH<0 ,在密闭容器中反应达到平衡状态的标志是①压强不再改变
②生成氨气的速率等于生成氮气的速率
③正反应速率等于零
④容器内气体的平均相对分子量不再改变
⑤单位时间内有3amolH-H的断裂的同时有6amolN-H断裂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:

(1)实验报告中记录合理的是___________ (填序号)。
(2)请写出该电池的负极反应式___________ 。
(3)若有1mol电子流过导线,则理论上产生H2的质量为___________ g。

| a.电流计指针偏转 |
| b.Cu极有H2产生 |
| c.H+向负极移动 |
| d.电流由Zn经导线流向Cu |
(1)实验报告中记录合理的是
(2)请写出该电池的负极反应式
(3)若有1mol电子流过导线,则理论上产生H2的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】目前汽车上使用的铅蓄电池如图所示,根据图示回答下列问题:

(1)铅蓄电池的负极是___________ ,铅蓄电池的正极是___________ 。
(2)铅蓄电池的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则负极发生___________ (填“氧化”或“还原”)反应,由___________ 生成___________ ;正极发生___________ (填“氧化”或“还原”)反应,由___________ 生成___________ 。
(3)电解质溶液是H2SO4,那么在铅蓄电池中H+向___________ (填“正”或“负”)极移动, 向
向___________ (填“正”或“负”)极移动。

(1)铅蓄电池的负极是
(2)铅蓄电池的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则负极发生
(3)电解质溶液是H2SO4,那么在铅蓄电池中H+向
 向
向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】从能量的变化和反应的快慢等角度研究反应:CH4+2O2=2H2O+CO2。
(1)下图能正确表示该反应中能量变化的是________ 。

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为________ ;正极发生________ 反应(填“氧化”或“还原”)。电路中每转移0.2 mol电子,标准状况下消耗O2的体积是________ L。
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是________ ,负极材料是 ________ ,电解质溶液是 ________ 。
②正极的电极反应式为________ 。
(1)下图能正确表示该反应中能量变化的是

(2)酸性甲烷燃料电池的总反应方程式为CH4+2O2 = 2H2O+CO2。其中,负极的电极反应式为
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池,请你利用下列反应Cu+2Ag+=Cu2++2Ag设计一个化学电池,并回答下列问题:
①该电池的正极材料是
②正极的电极反应式为
您最近一年使用:0次



