1 . 已知A、B、C、D、E、F、G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如下表所示。
完成下列问题:
(1)元素F在元素周期表中的位置是_______ 。这七种元素中,不属于主族元素的元素的名称是_______ 。
(2)在E、F、G三种元素中,原子半径最小的是_______ (填元素符号),其离子的电子式是_______ 。
(3)元素A与G可形成化合物AG4,在该化合物中含有的化学键类型为_______ ,分子的空间结构为_______ 。A与氧元素可形成化合物AO2,该化合物分子的结构式为_______ 。
(4)元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈_______ (填“酸”、“碱”或“中”)性,原因为_______ (用方程式表示)。B和G的气态氢化物相互反应的化学方程式为_______ 。
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第IIA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
(1)元素F在元素周期表中的位置是
(2)在E、F、G三种元素中,原子半径最小的是
(3)元素A与G可形成化合物AG4,在该化合物中含有的化学键类型为
(4)元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈
您最近一年使用:0次
2 . 现有4种短周期主族元素X、Y、Z和W,原子序数依次增大,其相关信息如表:
完成下列填空。
(1)元素X有多种核素,他们互称为_______ ,其中一种核素用于计算原子的相对原子质量,该核素的符号为_______ 。
(2)写出元素Y的氢化物(甲)的电子式_______ 。
(3)Z的单质在空气中燃烧时,火焰呈_______ 色,生成物中含有的化学键类型为_______ 。
(4)元素W位于元素周期表第_______ 周期_______ 族,与W同周期,原子半径最小的是_______ 。(填元素符号)
(5)X、W两元素非金属性较强的是_______ 。(填元素符号)写出能证明这一结论的一个实验事实_______ 。
| 元素 | 相关信息 |
| X | 原子核外最外层电子数是次外层的2倍 |
| Y | 氢化物(甲)常用作制冷剂,其水溶液呈碱性 |
| Z | 海水中含量最高的金属元素 |
| W | 单质为淡黄色固体,常存在于火山口附近 |
(1)元素X有多种核素,他们互称为
(2)写出元素Y的氢化物(甲)的电子式
(3)Z的单质在空气中燃烧时,火焰呈
(4)元素W位于元素周期表第
(5)X、W两元素非金属性较强的是
您最近一年使用:0次
名校
解题方法
3 . 短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的某种化合物(如图所示)是一种优良的防龋齿剂(用于制含氟牙膏),其中Z元素的内层电子数之和为最外层电子数的2倍。下列说法错误的是
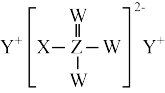
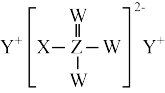
| A.Z的最高价氧化物对应的水化物为弱酸 | B.W、Y形成的化合物在熔融状态下能够导电 |
| C.X、Y形成的化合物为强电解质 | D.X、W、Z对应的单质熔沸点:X>W>Z |
您最近一年使用:0次
4 . X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误的是
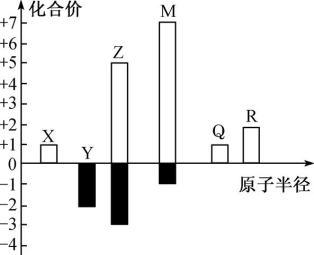

| A.X与Y组成的化合物中可能有非极性共价键 |
| B.X、Y、Z三种元素组成的化合物可能是酸、碱或盐 |
| C.简单离子半径:Q>Y |
| D.化合物R(YX)2是强碱 |
您最近一年使用:0次
名校
解题方法
5 . 短周期元素X、Y、Z、W原子序数依次增大。常温下,四种元素最高价氧化物对应水化物均能形成浓度为 的溶液,它们的
的溶液,它们的 分布如下图所示。下列说法正确的是
分布如下图所示。下列说法正确的是
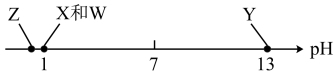
 的溶液,它们的
的溶液,它们的 分布如下图所示。下列说法正确的是
分布如下图所示。下列说法正确的是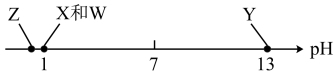
| A.X与W可能位于同一主族 |
B.最外层未成对电子数: |
| C.四种元素的简单离子中Y的半径最小 |
| D.四种元素的最高价氧化物对应水化物中Z的酸性最强 |
您最近一年使用:0次
2022-06-12更新
|
740次组卷
|
5卷引用:上海市虹口区2021-2022学年高三下学期学习能力诊断测试化学试题
上海市虹口区2021-2022学年高三下学期学习能力诊断测试化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(练)-2023年高考化学一轮复习讲练测(全国通用)广东省汕头市金山中学2022-2023学年高三上学期开学考试化学试题(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题河南省洛阳市第一高级中学2023-2024学年高三上学期开学摸底考试化学试题
名校
解题方法
6 . 某短周期元素X的最高价是+6,X的氢化物的化学式是
| A.HX | B.H2X | C.XH3 | D.XH4 |
您最近一年使用:0次
名校
解题方法
7 . 四种短周期元素的核电荷数依次增大,它们相关信息如下表。
完成下列填空:
(1)W所形成的负离子的电子式为_______ ,该离子核外能量最高的电子位于_______ (填电子层符号)层。
(2)X用于测定文物年代的X核素的符号为_______ ;该核素核内中子数与质子数之差为_______ 。
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。简述引发实验的操作。_______
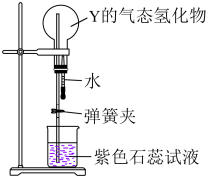
用相关化学方程式解释实验过程中紫色石蕊试液变色的原因:_______ 。
(4)Z在元素周期表中的位置是_______ ,比较X与Z原子半径的相对大小并说明理由。_______
(5)通过如下装置可以比较X、Y、Z三种元素的非金属性强弱。
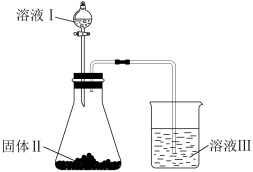
溶液Ⅰ的溶质是_______ (填化学式);进行实验时溶液Ⅲ中的现象是_______ 。有人认为上述装置存在缺陷,无法达到实验目的,请写出改进的措施。_______
| 元素代号 | W | X | Y | Z |
| 相关信息 | 原子得到1个电子后达到稀有气体稳定结构 | 某种核素常用于测定文物年代 | 气态氢化物极易溶于水 | 原子最外层电子是最内层电子的2倍 |
(1)W所形成的负离子的电子式为
(2)X用于测定文物年代的X核素的符号为
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。简述引发实验的操作。

用相关化学方程式解释实验过程中紫色石蕊试液变色的原因:
(4)Z在元素周期表中的位置是
(5)通过如下装置可以比较X、Y、Z三种元素的非金属性强弱。

溶液Ⅰ的溶质是
您最近一年使用:0次
名校
8 . 有R、W、X、Y、M五种原子序数依次增大的元素。R2是密度最小的气体。W与X可形成两种稳定的化合物WX和WX2。人类使用的化石燃料在燃烧过程中将大量WX2排入大气,导致地球表面平均温度升高。Y的原子序数是X的2倍。
(1)试写出R同位素中含有2个中子的核素符号:___________ ;W的原子结构示意图是___________ ,X的离子结构示意图是___________ ,Y负离子的电子式是___________ 。
(2)元素M所形成的气态分子M2有3种,其相对分子质量分别为70、72、74。它们物质的量之比是9∶6∶1,则质量数为37的核素的丰度为___________ 。
(3)W、Y和硝酸钾是黑火药的主要成分:
①请配平制备的反应方程式并标出电子转移的方向和数目:___________
_________+_______KNO3 +________ ________+______N2↑+________↑
________+______N2↑+________↑
②反应结束后,用___________ 清洗试管内壁残留的Y。
(4)回答下列问题:
①将n(YX2):n(M2)=1:1的混合气体通入品红溶液中,溶液___________ (填“褪色”或“不褪色”),反应的离子方程式为:___________ ;
②若n(YX2):n(M2)>1:1,溶液___________ (填“褪色”或“不褪色”);
③若n(YX2):n(M2)<1:1,溶液___________ (填“褪色”或“不褪色”),原因是___________ (用离子方程式表示)。
(1)试写出R同位素中含有2个中子的核素符号:
(2)元素M所形成的气态分子M2有3种,其相对分子质量分别为70、72、74。它们物质的量之比是9∶6∶1,则质量数为37的核素的丰度为
(3)W、Y和硝酸钾是黑火药的主要成分:
①请配平制备的反应方程式并标出电子转移的方向和数目:
_________+_______KNO3 +________
 ________+______N2↑+________↑
________+______N2↑+________↑②反应结束后,用
(4)回答下列问题:
①将n(YX2):n(M2)=1:1的混合气体通入品红溶液中,溶液
②若n(YX2):n(M2)>1:1,溶液
③若n(YX2):n(M2)<1:1,溶液
您最近一年使用:0次
名校
9 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。请回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第____ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ 。
(3)下列有关性质的比较能用元素周期律解释的是____ (填字母,下同)。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为____ 。
②X的氢化物的电子式:____ 。
③写出Y的最高价氧化物的一种用途____ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
名校
10 . 由短周期主族元素组成的化合物的一种表示方法如下图所示。图中短线表示共用电子对,省略孤电子对。其中元素X、Y、Z、W的原子序数依次增大且总和为33,W为金属元素。下列说法不正确的是
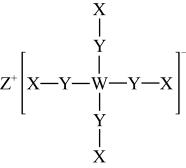
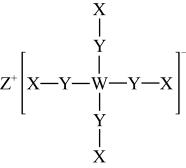
| A.该化合物属于离子化合物 |
| B.W、Z的简单离子半径:W<Z |
| C.Y、W两元素形成的化学键一定为离子键 |
| D.X、Y形成的一种化合物是常见的消毒剂 |
您最近一年使用:0次



