名校
1 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近一年使用:0次
2 . 现有原子序数依次增大的短周期主族元素P、Q、X、Y、Z、W。P元素的一种核素无中子,元素Q的最外层电子数是电子层数的2倍,Y原子是其所在周期中半径最大的原子,元素Z的最外层电子数是K层电子数的3倍,X能与Y可以形成一种淡黄色固体M。
(1)写出元素Q在元素周期表中的位置_______ 。
(2)写出元素P与元素X形成的18e-分子的电子式_______ 。
(3)研究发现M具有强氧化性,Z的一种氧化物具有较强的还原性,可相互反应。写出该反应的化学方程式:_______ 。
(4)为了证明非金属性W>Z,某小组设计如图装置探究元素非金属性的变化规律。C中装有Y2Z溶液,B中装有YWX3固体。A中试剂为_______ (填化学式)浓溶液,C中发生反应的离子方程式为_______ 。

(5)元素P与元素Q形成的一种物质Q2P4使溴水褪色,写出褪色过程中发生的化学反应方程式:_______ 。
(1)写出元素Q在元素周期表中的位置
(2)写出元素P与元素X形成的18e-分子的电子式
(3)研究发现M具有强氧化性,Z的一种氧化物具有较强的还原性,可相互反应。写出该反应的化学方程式:
(4)为了证明非金属性W>Z,某小组设计如图装置探究元素非金属性的变化规律。C中装有Y2Z溶液,B中装有YWX3固体。A中试剂为

(5)元素P与元素Q形成的一种物质Q2P4使溴水褪色,写出褪色过程中发生的化学反应方程式:
您最近一年使用:0次
名校
3 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。请回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第____ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ 。
(3)下列有关性质的比较能用元素周期律解释的是____ (填字母,下同)。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为____ 。
②X的氢化物的电子式:____ 。
③写出Y的最高价氧化物的一种用途____ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
4 . 如图为从元素周期表截取的短周期主族元素的一部分,Y是所在周期中原子半径最小的元素。下列说法正确的是


| A.Y的最高价氧化物对应的水化物酸性最强 |
| B.X的一种氢化物具有强氧化性 |
| C.W的最高价氧化物分子中所有原子的最外层都达到8电子稳定结构 |
D.简单离子的还原性: |
您最近一年使用:0次
名校
5 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中的位置为_______ ,B的离子结构示意图_______ 。
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)_______ 。C单质与水反应生成的具有漂白性物质的电子式_______
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):_______ 。
| 元素 | 相关信息 |
| A | 自然界中形成化学物种类最多的元素 |
| B | 单质的焰色反应为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | −2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中的位置为
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):
您最近一年使用:0次
名校
6 .  、
、 为第三周期元素,
为第三周期元素, 最高正价与最低负价的代数和为6,二者形成的一种化合物能以
最高正价与最低负价的代数和为6,二者形成的一种化合物能以 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是
 、
、 为第三周期元素,
为第三周期元素, 最高正价与最低负价的代数和为6,二者形成的一种化合物能以
最高正价与最低负价的代数和为6,二者形成的一种化合物能以 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是A.原子半径: | B.简单氢化物的还原性: |
C.同周期元素形成的单质中 氧化性最强 氧化性最强 | D.最高价含氧酸的酸性: |
您最近一年使用:0次
名校
解题方法
7 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
回答下列问题:
(1)W在元素周期表中的位置为_______ ,X的最高价氧化物对应水化物的化学式为_______ 。
(2)用电子式表示X2Q的形成过程:_______ 。
(3)金属性Y_______ (填“>”或“<”)X,从原子结构角度解释原因_______ 。
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
(5)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是_______ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰为紫色 |
| Z | 原子结构示意图为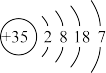 |
(1)W在元素周期表中的位置为
(2)用电子式表示X2Q的形成过程:
(3)金属性Y
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
| A.Z的化合价中只有+7价 |
| B.Z的最高价氧化物对应水化物的酸性弱于w的最高价氧化物对应水化物的酸性 |
| C.Z元素单质的氧化性强于W元素单质的氧化性 |
| D.Z与X形成的化合物中只存在离子键 |
您最近一年使用:0次
名校
解题方法
8 . 共价化合物分子中各原子有一定的连接方式,某分子可用球棍模型表示如图,A的原子半径最小,C、D位于同周期,D的常见单质常温下为气态,下列说法正确的是( )
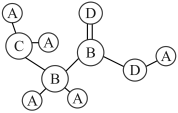

| A.B的同素异形体数目最多2种 |
| B.A与C不可以形成离子化合物 |
| C.通过含氧酸酸性可以比较元素B和C的非金属性 |
| D.C与D形成的阴离子CD2-既有氧化性,又有还原性 |
您最近一年使用:0次
2020-03-25更新
|
346次组卷
|
5卷引用:四川省成都外国语学校2021-2022学年高二下学期期中考试化学试题
解题方法
9 . 已知W、X、Y、Z均为短周期主族元素,常温下,它们的最高价氧化物对应的水化物溶液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是
)的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是

 )的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是
)的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是
| A.气态氢化物的热稳定性:Y<Z | B.Y的氧化物可能具有还原性、氧化性 |
| C.简单离子半径:Y>Z>W>X | D.化合物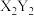 中含有极性共价键和非极性共价键 中含有极性共价键和非极性共价键 |
您最近一年使用:0次
2022-11-05更新
|
148次组卷
|
2卷引用:河南省南阳市2022-2023学年高三上学期期中质量评估化学试题
10 . LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成,结构如图,Y的最外层电子数等于X的核外电子总数,下列说法正确的是
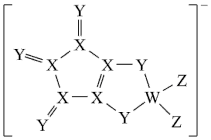

| A.同周期元素第一电离能小于Y的有5种 |
| B.简单氢化物的还原性:X<Y |
| C.四种元素中原子半径最大的是W |
| D.四种元素形成的单质中Y的氧化性最强 |
您最近一年使用:0次



