名校
解题方法
1 . X、Y、Z、W为原子序数依次增大的前20号元素,它们分别处于元素周期表的不同周期和不同主族,由它们形成的一种化合物结构如图,下列叙述不正确的是
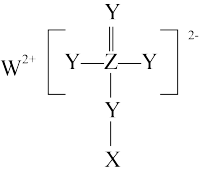

| A.原子半径: X<Y<Z<W |
| B.上述化合物中Z原子满足8电子稳定结构 |
| C.X和W形成的化合物可用于野外工作的应急燃料 |
| D.同主族简单氢化物中,Z的氢化物沸点最低 |
您最近半年使用:0次
名校
解题方法
2 . A、B、C、D、E为五种原子序数依次增大的短周期主族元素。已知B原子最外层电子数与核外电子总数之比为3:4;D原子最外层电子数与次外层电子数之比为3:4;E-、C+、A+离子的半径逐渐减小;化合物AE常温下为气体。据此回答:
(1)D、E的最高价氧化物对应水化物酸性较强的是___ (写出化学式)。
(2)用惰性电极电解化合物CE的饱和溶液,当电路中有0.2mol电子通过时两极产生的气体在标准状况下的体积共为___ L。
(3)A与B、A与D均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式___ ,并写出A与B形成的18电子分子的电子式___ 。
(4)均由A、B、C、D四种元素组成的两种盐发生反应的离子方程式是___ ;其中一种是强酸所成的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式___ 。
(1)D、E的最高价氧化物对应水化物酸性较强的是
(2)用惰性电极电解化合物CE的饱和溶液,当电路中有0.2mol电子通过时两极产生的气体在标准状况下的体积共为
(3)A与B、A与D均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式
(4)均由A、B、C、D四种元素组成的两种盐发生反应的离子方程式是
您最近半年使用:0次
名校
解题方法
3 . 短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是
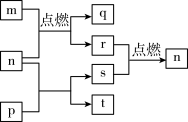

| A.离子半径:Z>X |
| B.2.4 gm在足量的n中充分燃烧,固体质量增加1.6 g |
| C.最简单气态氢化物的稳定性:W>X |
| D.n+p→s+t的过程中,有离子键、共价键的断裂,也有离子键、共价键的形成 |
您最近半年使用:0次
2020-08-06更新
|
1742次组卷
|
2卷引用:重庆市巴蜀中学2019-2020学年高一下学期期末考试化学试题
解题方法
4 . X、Y、Z、W为原子序数依次增大的四种短周期元素,b、a、d、c为上述四种元素形成的单质,m、n、p为四种元素形成的二元化合物,其转化关系如图所示。W与同周期原子半径最大的元素组成的化合物溶液呈中性,n为一种传递神经信息的“信使分子”。下列说法错误的是
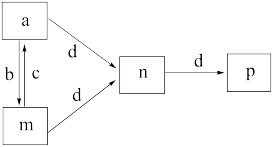

| A.a的熔点比d的熔点低 |
| B.Y、Z、W的简单离子半径大小顺序为:Y<Z<W |
| C.X、Z组成的分子可能既含有极性键,又含有非极性键 |
| D.在工业上c可大量用于制造有机溶剂和杀菌消毒剂 |
您最近半年使用:0次
2020-07-27更新
|
661次组卷
|
2卷引用:山东省枣庄市2019-2020学年高二下学期期末考试化学试题
名校
解题方法
5 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为_________________ 。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式________________________________ 。
(2)由A、B两种元素组成的18电子微粒的分子式为____________________ 。
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_________________________________________ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________ L(标准状况下)。
(1)E元素在周期表中的位置为
(2)由A、B两种元素组成的18电子微粒的分子式为
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是
您最近半年使用:0次
2020·全国·
名校
解题方法
6 . 元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R和Y位于同主族,R原子最外层电子数和X的原子序数之和等于Z的原子序数。由这四种元素组成一种化合物Q,在Q的溶液中滴加Ba(OH)2溶液,产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是( )
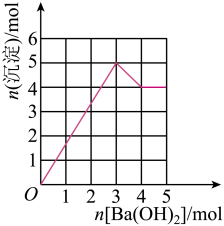
| A.简单离子半径:Z>X>Y>R |
| B.气态氢化物的热稳定性:R>Y |
| C.Q的溶液中两种阳离子浓度相等 |
| D.Z2R2是含一种极性键的离子化合物 |
您最近半年使用:0次
名校
7 . 短周期主族元素X、Y、Z和W的原子序数依次增大,X、Y、W位于不同周期,Y、Z、W的原子最外层电子数之和为14,Z的原子半径在短周期主族元素中最大。下列说法错误的是( )
| A.简单离子半径:W>Z>X |
| B.W的最高价氧化物对应的水化物为强酸 |
| C.Y与Z形成的化合物溶于水所得溶液呈碱性 |
| D.与X形成的简单化合物的还原性:Y>Z>W |
您最近半年使用:0次
2020-04-03更新
|
2670次组卷
|
4卷引用:福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题
福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题解题达人.化学选择题(2021全国卷)提升小卷16(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)江西省安义中学2022-2023学年高三上学期中考试化学试题
解题方法
8 . 现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:____________ ,元素Y的最简单氢化物的化学式为______________ 。
(2)Z元素原子的相对原子质量为____________ 。
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为______________ 。
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式为__________________ 。
| 元素编号 | 元素原子结构 |
| X | 原子结构示意图为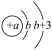 |
| Y | 最外层电子数是次外层电子数的2倍 |
| Z | 原子核内含有12个中子,且其离子的结构示意图为 |
(2)Z元素原子的相对原子质量为
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式为
您最近半年使用:0次
名校
9 . X、Y、Z为元素周期表中原子序数依次增大的三种短周期元素,Y与X、Z均相邻,X、Y与Z三种元素原子的最外层电子数之和为19;W的单质为生活中一种常见的金属,在Z元素的单质中燃烧产生棕黄色的烟,生成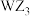 。回答下列问题:
。回答下列问题:
(1)Z元素在元素周期表中的第____ 周期。
(2) 与足量的
与足量的 的水溶液发生反应生成两种强酸,写出该反应的离子方程式
的水溶液发生反应生成两种强酸,写出该反应的离子方程式____ 。
(3)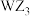 易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是
易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是__ ,判断的依据是____ 。
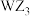 。回答下列问题:
。回答下列问题:(1)Z元素在元素周期表中的第
(2)
 与足量的
与足量的 的水溶液发生反应生成两种强酸,写出该反应的离子方程式
的水溶液发生反应生成两种强酸,写出该反应的离子方程式(3)
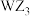 易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是
易升华,易溶于水,乙醇/丙酮等溶剂。据此推测其晶体熔化时克服的作用力是
您最近半年使用:0次
10 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E 元素的周期序数与主族序数相等。
(1)E 元素在周期表中的位置___________ 。
(2)写出A2W2的电子式为____________ 。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式________ 。
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是_________ (标准状况下)。
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为_____________ 。
(1)E 元素在周期表中的位置
(2)写出A2W2的电子式为
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为
您最近半年使用:0次
2019-07-02更新
|
330次组卷
|
2卷引用:江西省吉安市2018-2019学年高一下学期期末教学质量检测化学试题



