名校
解题方法
1 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)②的最高价氧化物的结构式为_____ ;⑦的最高价氧化物对应水化物的化学式为_____ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_____ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_____(填字母)。
(4)已知 元素位于元素周期表中第六周期第IA族,请回答下列问题:
元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_____ 。
②铯单质与 反应的离子方程式为
反应的离子方程式为_____ 。
③预测铯单质的还原性比钠单质的还原性_____ (填“弱”或“强”)。
④下列推断正确的是_____ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为 ,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数
,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数 与
与 所有可能的关系式为
所有可能的关系式为_____ 。

(1)②的最高价氧化物的结构式为
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_____(填字母)。
| A.在化合物中最高正化合价为+6 |
B.单质可以与 气体反应并置换出单质 气体反应并置换出单质 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
(4)已知
 元素位于元素周期表中第六周期第IA族,请回答下列问题:
元素位于元素周期表中第六周期第IA族,请回答下列问题:①铯的原子序数为
②铯单质与
 反应的离子方程式为
反应的离子方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为
 ,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数
,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数 与
与 所有可能的关系式为
所有可能的关系式为
您最近一年使用:0次
名校
2 . 下表是元素周期表的一部分,请参照元素 在表中的位置,回答下列问题:
在表中的位置,回答下列问题:
(1)写出由元素②和元素④形成原子个数比为 的化合物的电子式:
的化合物的电子式:_____ 。
(2) 四种元素的离子半径由大到小排序
四种元素的离子半径由大到小排序_____ (写离子符号)。
(3)元素 形成的简单气态氢化物的稳定性中较大的是
形成的简单气态氢化物的稳定性中较大的是_____ (填化学式)。
(4)元素⑤与⑦可形成离子化合物,用电子式表示其形成过程_____ 。
(5)下列事实能判断⑥和⑦的金属性强弱的是_____ (填字母,下同)。
a.常温下单质与水反应置换出氢气的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒 位于第四周期,与④同主族。下列推断正确的是
位于第四周期,与④同主族。下列推断正确的是_____ 。
a. 只具有还原性
只具有还原性
b. 的最低负化合价是
的最低负化合价是 价
价
c. 的最高价氧化物对应水化物的酸性比
的最高价氧化物对应水化物的酸性比 强
强
(7)同温同压下, 的
的 单质分别与
单质分别与 的盐酸充分反应,产生氢气的体积比为
的盐酸充分反应,产生氢气的体积比为_____ 。
 在表中的位置,回答下列问题:
在表中的位置,回答下列问题:| 族 周期 | 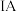 | 0 | ||||||
| 一 | ① | 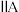 | 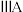 | 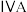 | 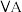 | 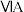 | 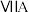 | |
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
 的化合物的电子式:
的化合物的电子式:(2)
 四种元素的离子半径由大到小排序
四种元素的离子半径由大到小排序(3)元素
 形成的简单气态氢化物的稳定性中较大的是
形成的简单气态氢化物的稳定性中较大的是(4)元素⑤与⑦可形成离子化合物,用电子式表示其形成过程
(5)下列事实能判断⑥和⑦的金属性强弱的是
a.常温下单质与水反应置换出氢气的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒
 位于第四周期,与④同主族。下列推断正确的是
位于第四周期,与④同主族。下列推断正确的是a.
 只具有还原性
只具有还原性b.
 的最低负化合价是
的最低负化合价是 价
价c.
 的最高价氧化物对应水化物的酸性比
的最高价氧化物对应水化物的酸性比 强
强(7)同温同压下,
 的
的 单质分别与
单质分别与 的盐酸充分反应,产生氢气的体积比为
的盐酸充分反应,产生氢气的体积比为
您最近一年使用:0次
名校
解题方法
3 . 下列说法中正确的是
| A.化学键包括离子键、共价键和氢键 |
| B.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C.同一周期中,ⅡA与ⅢA族元素原子的核电荷数都相差1 |
| D.新型高效催化剂多与过渡元素有关 |
您最近一年使用:0次
名校
解题方法
4 . 现有8种短周期元素的性质的数据如下表
(1)③与⑧的单质均能与烧碱溶液反应,且具有一定的相似性,写出单质③与烧碱溶液反应的化学方程式________ 。
(2)④与⑤形成的二元化合物X中所有原子均满足 稳定结构,X的电子式为
稳定结构,X的电子式为________ 。
(3)⑥的碳酸氢盐俗名为________ ,其与足量 反应的离子方程式为
反应的离子方程式为________ 。
(4)⑦的最高价氧化物为________ 性氧化物;以上8种元素的最高价氧化物的水化物中酸性最强的为________ (填化学式)。
元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径/( | 0.74 | 1.60 | 0.89 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
最高或最低化合价 | — | +2 | +2 | +5 | +7 | +1 | +5 | +3 |
-2 | — | — | -3 | -1 | — | -3 | — |
(2)④与⑤形成的二元化合物X中所有原子均满足
 稳定结构,X的电子式为
稳定结构,X的电子式为(3)⑥的碳酸氢盐俗名为
 反应的离子方程式为
反应的离子方程式为(4)⑦的最高价氧化物为
您最近一年使用:0次
名校
5 . 科学家利用原子序数依次递增的短周期主族元素W、X、Y、Z组合成一种“超分子”,具有高效的催化性能,其结构如图所示。W、X、Z分别位于不同周期,Z的金属性在同周期元素中最强。下列说法错误的是


| A.X、Y、Z形成的两种盐的水溶液均显碱性,可以做食用碱和工业用碱 |
B. 和 和 中阴、阳离子个数比均为1:2 中阴、阳离子个数比均为1:2 |
C.Z和 在不同条件下发生反应产物不同 在不同条件下发生反应产物不同 |
| D.L与Z同周期,且为同周期非金属性最强的元素,L、W、Y、Z能形成多种漂白性的物质 |
您最近一年使用:0次
名校
6 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丙>甲>乙 |
| B.甲的氢化物遇氯化氢一定有白烟产生 |
| C.非金属性:戊>丁>丙 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
名校
解题方法
7 . 有关元素周期表判断,下列叙述不正确的是
①短周期元素中,若两种元素的原子序数相差8,则它们一定是同主族元素
②第IA元素称为碱金属元素
③用中文“馍”命名的第115号元素在周期表中位于第七周期第15列
④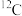 与
与 互为同位素,化学性质不同,但物理性质几乎完全相同
互为同位素,化学性质不同,但物理性质几乎完全相同
⑤除0族外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
⑥所含元素种类最多的族是第ⅢB,所含元素形成化合物种类最多的是第ⅣA
⑦主族金属元素都符合原子的最外层电子数≤4
⑧同一主族元素的最外层电子数相同,最外层电子数相同的元素位于同一主族
①短周期元素中,若两种元素的原子序数相差8,则它们一定是同主族元素
②第IA元素称为碱金属元素
③用中文“馍”命名的第115号元素在周期表中位于第七周期第15列
④
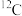 与
与 互为同位素,化学性质不同,但物理性质几乎完全相同
互为同位素,化学性质不同,但物理性质几乎完全相同⑤除0族外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
⑥所含元素种类最多的族是第ⅢB,所含元素形成化合物种类最多的是第ⅣA
⑦主族金属元素都符合原子的最外层电子数≤4
⑧同一主族元素的最外层电子数相同,最外层电子数相同的元素位于同一主族
| A.①②⑤⑥ | B.①②⑦⑧ | C.①②④⑤⑦⑧ | D.③④⑥⑦⑧ |
您最近一年使用:0次
名校
8 . 某学者绘制了一种八角星元素周期表,每个八角星代表一个周期(第1周期除外),每个“·”代表一种元素,“∙∙∙∙∙∙”相连代表同族元素。X、Y、Z、R、M为原子半径依次减小的五种短周期主族元素,Y的最外层电子总数比最内层电子总数多一个,下列说法正确的是

| A.原子序数由大到小:X>Y>Z |
| B.Z与M形成的化合物,各原子均满足8电子稳定结构 |
| C.X、Y、Z最高价氧化物的水化物之间均能两两反应 |
| D.X、R形成的两种常见化合物阴、阳离子个数比分别为1∶1、1∶2 |
您最近一年使用:0次
2024-01-11更新
|
243次组卷
|
4卷引用:黑龙江省实验中学2023-2024学年高一下学期开学测试化学试题
名校
9 . 如表为部分元素的特点
请回答下列问题:
(1)若火灾现场存放大量Y,需要用______ 灭火;化合物Y2X2中存在的化学键类型为______ 。
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈______ 色,说明还原性有:L2+______ I-(填“>”或“<”);
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:
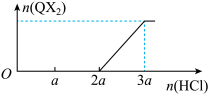
由此可知,混合物甲的组成为______ (填化学式),两者的物质的量之比为______ 。
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液
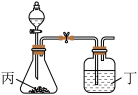
请选择装置丙、丁两处应该加入的药品代号:丙______ 、丁______ 。
| 特点 | 元素代号 |
| 地壳中含量最高的元素 | X |
| +1价阳离子L层充满电子 | Y |
| 原子半径最小的原子 | Z |
| 一种同位素可以用于考古 | Q |
| 与上述代号为Z的元素形成分子Z2R,其摩尔质量为34g/mol | R |
| 其合金用量最大,用途最广 | L |
(1)若火灾现场存放大量Y,需要用
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:

由此可知,混合物甲的组成为
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液

请选择装置丙、丁两处应该加入的药品代号:丙
您最近一年使用:0次
2023-03-09更新
|
269次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高一下学期开学化学试题
名校
解题方法
10 . 元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。如表是元素周期表的一部分,请按题目要求回答下列问题:
(1)表中用字母标出的9种元素中,金属性最强的是 _______ (用元素符号表示),m的族序数为_______ 。
(2)e、d、g简单离子半径由小到大的顺序为:_______ (用元素符号表示)
(3)在a到n元素中,其某种氧化物可用于呼吸面具中氧气来源,请写出该化合物的电子式_______ 。
(4)写出e、f两种元素的最高价氧化物对应水化物在溶液中相互反应的离子方程式:_______ 。
(5)下列表述中能证明g和n非金属性强弱比较这一事实的是_______ (填字母)。
①g的氢化物比n的氢化物稳定
②g最高价氧化物对应的水化物的酸性强于n最高价氧化物对应的水化物的酸性
③g的单质能将n从其钠盐溶液中置换出来
④g的氢化物酸性比n的氢化物酸性弱
a | |||||||||||||||||
b | c | d | |||||||||||||||
e | f | g | |||||||||||||||
m | n | ||||||||||||||||
(2)e、d、g简单离子半径由小到大的顺序为:
(3)在a到n元素中,其某种氧化物可用于呼吸面具中氧气来源,请写出该化合物的电子式
(4)写出e、f两种元素的最高价氧化物对应水化物在溶液中相互反应的离子方程式:
(5)下列表述中能证明g和n非金属性强弱比较这一事实的是
①g的氢化物比n的氢化物稳定
②g最高价氧化物对应的水化物的酸性强于n最高价氧化物对应的水化物的酸性
③g的单质能将n从其钠盐溶液中置换出来
④g的氢化物酸性比n的氢化物酸性弱
您最近一年使用:0次

 )
)

