21-22高一上·浙江·期末
解题方法
1 . 有A、B、C、D、E五种常见的短周期主族元素,它们的核电荷数依次增大,A元素原子的最外层只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;C元素原子的最外层电子数是D元素原子最外层电子数的一半。
(1)D在元素周期表中的位置___ 。
(2)A与B形成原子个数比为1:1的液体物质甲,甲的电子式___ ;A与B形成原子个数比为2:1的液体物质乙,液态物质乙中存在的作用力有___ (填序号):
①共价键 ②离子键 ③氢键 ④范德华力
(3)B、C、D、E离子半径由大到小的顺序是___ (用离子符号表示)。
(4)化合物丙由E和F两种元素组成,常大量用于面粉的消毒与漂白,常温下呈液态,极易分解得两种气体单质X和Y。现有12.05g化合物丙,将完全分解后所得混合气体通过足量NaOH溶液,最后只余标准状况下1.12L气体单质X共1.40g。
请回答:
①丙的化学式是___ 。
②丙遇水蒸气可形成一种常见的漂白性物质M同时放出气体N,该反应为非氧化还原反应,写出丙与水反应的化学方程式为___ 。
(1)D在元素周期表中的位置
(2)A与B形成原子个数比为1:1的液体物质甲,甲的电子式
①共价键 ②离子键 ③氢键 ④范德华力
(3)B、C、D、E离子半径由大到小的顺序是
(4)化合物丙由E和F两种元素组成,常大量用于面粉的消毒与漂白,常温下呈液态,极易分解得两种气体单质X和Y。现有12.05g化合物丙,将完全分解后所得混合气体通过足量NaOH溶液,最后只余标准状况下1.12L气体单质X共1.40g。
请回答:
①丙的化学式是
②丙遇水蒸气可形成一种常见的漂白性物质M同时放出气体N,该反应为非氧化还原反应,写出丙与水反应的化学方程式为
您最近一年使用:0次
2020·全国·
名校
解题方法
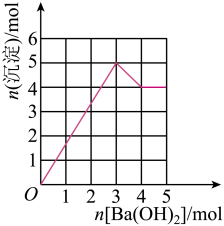
2 . 元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R和Y位于同主族,R原子最外层电子数和X的原子序数之和等于Z的原子序数。由这四种元素组成一种化合物Q,在Q的溶液中滴加Ba(OH)2溶液,产生沉淀的物质的量与Ba(OH)2的物质的量的关系如图所示,下列说法正确的是( )
| A.简单离子半径:Z>X>Y>R |
| B.气态氢化物的热稳定性:R>Y |
| C.Q的溶液中两种阳离子浓度相等 |
| D.Z2R2是含一种极性键的离子化合物 |
您最近一年使用:0次
名校
3 . 短周期主族元素X、Y、Z和W的原子序数依次增大,X、Y、W位于不同周期,Y、Z、W的原子最外层电子数之和为14,Z的原子半径在短周期主族元素中最大。下列说法错误的是( )
| A.简单离子半径:W>Z>X |
| B.W的最高价氧化物对应的水化物为强酸 |
| C.Y与Z形成的化合物溶于水所得溶液呈碱性 |
| D.与X形成的简单化合物的还原性:Y>Z>W |
您最近一年使用:0次
2020-04-03更新
|
2691次组卷
|
4卷引用:福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题
福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题解题达人.化学选择题(2021全国卷)提升小卷16(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)江西省安义中学2022-2023学年高三上学期中考试化学试题
4 . 下表为元素周期表的一部分。
(1)写出下列元素符号;②_______ 、⑮_______ ;表中在室温下呈液态的单质,其化学式为________ .
(2)表中元素⑦的原子结构示意图为____________ ;元素⑤的离子结构示意图为_________ ;元素⑫与元素⑯两者核电荷数之差是_______
(3)分别写出元素⑨的最高价氧化物的水化物与元素⑦、⑪的最高价氧化物的水化物反应的化学方程式_________________________________ ;________________________ .
(4)分别写出③与⑪、⑭与⑥组成的化合物的电子式__________ ;_________
(5)用电子式表示①与⑩组成的化合物的形成过程______________________
(6)表中元素⑩和⑪最高价氧化物对应水化物的酸性:______ >_____ (写化学式)。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ | ||
| 四 | ⑬ | ⑭ | ⑮ | ⑯ | ||||
(1)写出下列元素符号;②
(2)表中元素⑦的原子结构示意图为
(3)分别写出元素⑨的最高价氧化物的水化物与元素⑦、⑪的最高价氧化物的水化物反应的化学方程式
(4)分别写出③与⑪、⑭与⑥组成的化合物的电子式
(5)用电子式表示①与⑩组成的化合物的形成过程
(6)表中元素⑩和⑪最高价氧化物对应水化物的酸性:
您最近一年使用:0次
9-10高三·四川成都·阶段练习
解题方法
5 . A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
(1)A元素的名称是____ ,E元素在周期表中的位置是_____________________ ;
(2)B、D、F的气态氢化物稳定性由强到弱的顺序是______________ (填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是_______________ ;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于_____________ 化合物(填“离子”或“共价”);
②X与Y的水溶液相混合发生反应的离子方程式为__________________ ;
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为:___________________ 。
(1)A元素的名称是
(2)B、D、F的气态氢化物稳定性由强到弱的顺序是
(3)E单质在足量D单质中燃烧生成的化合物的电子式是
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于
②X与Y的水溶液相混合发生反应的离子方程式为
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为:
您最近一年使用:0次



