解题方法
1 . 下表中①~⑦表示元素周期表的部分元素。
(1)②元素最外层电子数比次外层电子数多______ 个,该元素的符号是_______ ;⑦元素的氢化物的电子式为____________________ 。
(2)由①③④三种元素组成的物质是______________ ,此物质的水溶液显_____ 性。
(3)⑥元素的原子半径大于③的理由是____________________________________ 。
(4)④元素的最高价氧化物对应的水化物的碱性强于⑤元素,用一个化学方程式来证明。________________________________________
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 1 | |||||||
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)②元素最外层电子数比次外层电子数多
(2)由①③④三种元素组成的物质是
(3)⑥元素的原子半径大于③的理由是
(4)④元素的最高价氧化物对应的水化物的碱性强于⑤元素,用一个化学方程式来证明。
您最近一年使用:0次
名校
2 . A、B、C、D 是同一周期的四种元素。A、B、C 的原子序数依次相差为 1,A 元素的单质的化学性质活泼,A元素的原子在本周期中第一电离能最小。B 元素的氧化物 2.0g 恰好跟100mL0.5mol·L−1硫酸完全反应。B 元素单质跟D元素单质反应生成化合物BD2。根据以上事实,填写下列空白:
(1)A的原子结构示意图:_____ ,C原子的电子式为_____ ;
(2)BD2的电子式为_____ ;若向C的氧化物的水化物中加入A的氧化物的水化物,则溶液显碱性。这一反应的离子方程式是_________ 。
(1)A的原子结构示意图:
(2)BD2的电子式为
您最近一年使用:0次
2018-04-20更新
|
62次组卷
|
2卷引用:山西省柳林县2020--2021学年高二下学期期中考试化学试题
10-11高二上·河北唐山·期中
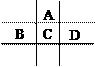
3 . 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同。
回答下列问题:
(1)A与E形成的化合物的化学式是__________________ 。
(2)B的最高价氧化物化学式为____________ ,C的元素名称为 ___________________ 。
(3)D的单质与水反应的方程式为____________________________________________________ 。

回答下列问题:
(1)A与E形成的化合物的化学式是
(2)B的最高价氧化物化学式为
(3)D的单质与水反应的方程式为
您最近一年使用:0次
名校
解题方法
4 . 有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)F的元素符号是__________ 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)F的元素符号是
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
2017-04-25更新
|
1871次组卷
|
4卷引用:吉林省白山市第七中学2018-2019学年高二下学期期中考试化学试题
解题方法
5 . 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同; D原子的核外成对电子数是未成对电子数的3倍。同时含有A、B、D三种元素的化合物M是一种居室污染气体,其分子中所有的原子共平面。A、B两种元素组成的原子个数比为1︰1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示 )
(1)下列叙述正确的是____________ (填字母)。
A.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
B.M和二氧化碳分子中的中心原子均采用sp2杂化
C.N分子中含有6个σ键和3个π键
D.N分子中所有原子共面
(2)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水,其中Fe为+2价) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式__________________ ,____________________ 。
(3)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是_______ 、_______ 。两者沸点的关系为X_____ Y(填 > 或 < )。
(1)下列叙述正确的是
A.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
B.M和二氧化碳分子中的中心原子均采用sp2杂化
C.N分子中含有6个σ键和3个π键
D.N分子中所有原子共面
(2)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水,其中Fe为+2价) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式
(3)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是
您最近一年使用:0次
10-11高二下·黑龙江·期中
6 . A、B、C、D四种短周期元素,0.5molA的元素的离子得到NA个电子后被还原为中性原子;0.4gA的氧化物恰好与100mL0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等。B元素原子核外电子数比A元素原子核外电子数多1;Cˉ离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层电子数的2倍。请填写下列空格:
(1)推断A、B、C、D四种元素的符号A______ ;B______ ;C______ ;D______ ;
(2)D元素的最高价氧化物的电子式是______ 结构式______ 该分子内含有______ 键(填极性或非极性)。
(1)推断A、B、C、D四种元素的符号A
(2)D元素的最高价氧化物的电子式是
您最近一年使用:0次



