名校
解题方法
1 . A,B,C,D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型:C,D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号)
(2)单质A有两种同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为_______ ,中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ ;晶胞中A原子的配位数为_______ ;列式计算晶体F的密度(g·cm-3)_______ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为

您最近半年使用:0次
2 . 短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示。其中X、Y、Z三种元素的质子数之和为21。
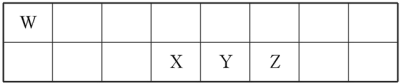
(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是_______ (用化学用语表示);该溶液中各种离子浓度由大到小的顺序为_______ 。
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为_____ 。
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
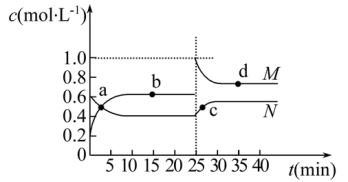
①a、b、c、d四个点中,化学反应处于平衡状态的是点_______ 。
②25min时,增加了_______ (填物质的化学式)_______ mol。
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______ (填字母)。

(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

①a、b、c、d四个点中,化学反应处于平衡状态的是点
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
您最近半年使用:0次
3 . 研究表明不含结晶水的X(由4种短周期元素组成),可作为氧化剂和漂白剂,被广泛应用于蓄电池工业等。为探究X的组成和性质,设计并完成了下列实验:
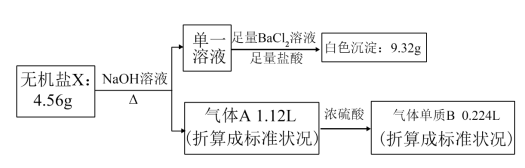
已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:_______ ,X中含有的元素为_______ 。
(2)请写出检验X中阳离子的方法:_______ 。
(3)已知X常用于检验 ,它可将
,它可将 氧化成
氧化成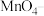 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。

已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:
(2)请写出检验X中阳离子的方法:
(3)已知X常用于检验
 ,它可将
,它可将 氧化成
氧化成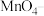 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近半年使用:0次
解题方法
4 . A、B、C、D、E、F六种元素,原子序数依次增大,A是周期表中原子半径最小的元素,B原子的最外层上有4个电子;D的阴离子和E的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体,F的L层电子数等于K、M两个电子层上的电子数之和。(用元素符号或化学式 填空回答以下问题)
(1)C元素在周期表中的位置_______ 。
(2)B、D两元素形成化合物属于(“离子”或“共价”)_______ 化合物。
(3)F原子结构示意图为_______ 。
(4)写出E2D2与BD2反应的化学方程式:_______ 。
(5)B、C、D的最简单氢化物稳定性由强到弱依次为:_______ 。(填化学式)
(6)写出F元素的最高价氧化物的水化物和B反应的化学方程式:_______ 。
(1)C元素在周期表中的位置
(2)B、D两元素形成化合物属于(“离子”或“共价”)
(3)F原子结构示意图为
(4)写出E2D2与BD2反应的化学方程式:
(5)B、C、D的最简单氢化物稳定性由强到弱依次为:
(6)写出F元素的最高价氧化物的水化物和B反应的化学方程式:
您最近半年使用:0次
2021-10-09更新
|
154次组卷
|
2卷引用:甘肃省庆阳市第六中学2020-2021学年高二下学期期末考试化学试题
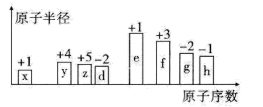
5 . 随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。
请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点___________ (填“高”或“低”),原因是:___________ ;x与e形成的化合物电子式为___________
(2)比较g、h常见离子的半径大小:___________ (填化学式,下同);比较e、f的最高价氧化物对应水化物的碱性强弱:___________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为___________ 。
②能形成共价化合物,写出其中一种的结构简式___________ 。

请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点
(2)比较g、h常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近半年使用:0次
名校
6 . 已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外电子层的p能级处于半充满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。回答下列问题:
(1)E元素基态原子的电子排布式为___________ 。
(2)用轨道表示式表示F元素原子的价电子排布:___________ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的是___________ (填化学式)。
(4)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为___________ 。试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:___________ 。
(1)E元素基态原子的电子排布式为
(2)用轨道表示式表示F元素原子的价电子排布:
(3)F、G元素对应的最高价含氧酸中酸性较强的是
(4)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
您最近半年使用:0次
7 . 已知 A、B、C、D、E五种元素中,原子序数依次增大,其中A、B、C、D为短周期元素。请根据下表中的信息回答有关问题:
(1)写出B基态原子的核外电子排布式____________________ .
(2)写出D原子价电子的轨道表示式为____________________ .
(3)E元素位于第______ 周期________ 族。
(4)写出A2B2的电子式___________ .
(5)写出C与D形成的化合物的化学式:_______________ 。
| 元素 | 结构或性质信息 |
| A | 原子半径最小的元素 |
| B | 原子最外能层的p能级中有一个轨道充填了2个电子。 |
| C | 原子的第一至第四电离能分别是:I1=841kJ/mol I2 = 1637 kJ/mol I3 = 3577kJ/mol I4 = 18540kJ/mol |
| D | 基态原子的核外电子共有17种运动状态 |
| E | 元素的价电子排布式为(n-l)dn+6ns2。 |
(2)写出D原子价电子的轨道表示式为
(3)E元素位于第
(4)写出A2B2的电子式
(5)写出C与D形成的化合物的化学式:
您最近半年使用:0次
2021-05-15更新
|
319次组卷
|
2卷引用:福建省宁德市高中同心顺联盟校2020-2021学年高二下学期期中考试化学试题
名校
8 . 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出下列元素的名称:A_______ ,B_______ ,C_______ ,D_______ 。
(2)D元素在周期表中的位置_______ 。
(3)室温下,由A、B、C三种元素形成的化合物水溶液pH为11,该溶液中由水电离出的OH-浓度为_______ ;该化合物的热溶液去油污能力更强的原因是_______  。
。
(4)由C、D两种元素形成的化合物水溶液呈_______ (填“酸”、“中”、“碱”)性,原因是_______ 。(用离子方程式表示)
(1)写出下列元素的名称:A
(2)D元素在周期表中的位置
(3)室温下,由A、B、C三种元素形成的化合物水溶液pH为11,该溶液中由水电离出的OH-浓度为
 。
。(4)由C、D两种元素形成的化合物水溶液呈
您最近半年使用:0次
20-21高二·全国·单元测试
9 . X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W位于元素周期表第_______ 周期第_______ 族;W的原子半径比X的_______ (填“大”或“小”)。
(2)Z的第一电离能比W的_______ (填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是_______ ;氢、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称_______ 。
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(2)Z的第一电离能比W的
您最近半年使用:0次
解题方法
10 . 硫元素有多种化合价,如图表示了含硫物质(甲~辛)与硫的化合价及相应物质类别物质类别之间的关系。
回答下列问题:
(1)物质甲的分子式为_______ 。
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是_________ (填标号)。
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:______ 。
| 物质类别 | ||||||
| 盐 | 戊 | 辛 | ||||
| 含氧酸 | 丁 | 庚 | ||||
| 氧化物 | 丙 | 己 | ||||
| 单质 | 乙 | |||||
| 氢化物 | 甲 | |||||
| -2 | 0 | +2 | +4 | +6 | 化合价 |
(1)物质甲的分子式为
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:
您最近半年使用:0次



