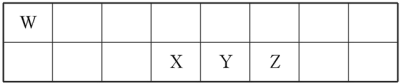
1 . 短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示。其中X、Y、Z三种元素的质子数之和为21。
(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是_______ (用化学用语表示);该溶液中各种离子浓度由大到小的顺序为_______ 。
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为_____ 。
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
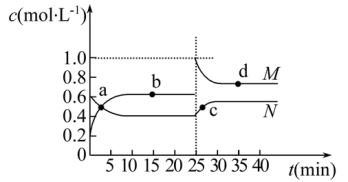
①a、b、c、d四个点中,化学反应处于平衡状态的是点_______ 。
②25min时,增加了_______ (填物质的化学式)_______ mol。
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______ (填字母)。

(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

①a、b、c、d四个点中,化学反应处于平衡状态的是点
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
您最近一年使用:0次
名校
解题方法
2 . 有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)F的元素符号是__________ 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)F的元素符号是
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
2017-04-25更新
|
1866次组卷
|
4卷引用:黑龙江省牡丹江市第一高级中学2017-2018学年高二4月月考化学试题
3 . 研究表明不含结晶水的X(由4种短周期元素组成),可作为氧化剂和漂白剂,被广泛应用于蓄电池工业等。为探究X的组成和性质,设计并完成了下列实验:
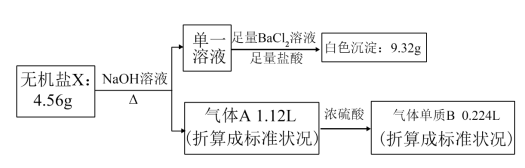
已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:_______ ,X中含有的元素为_______ 。
(2)请写出检验X中阳离子的方法:_______ 。
(3)已知X常用于检验 ,它可将
,它可将 氧化成
氧化成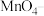 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。

已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:
(2)请写出检验X中阳离子的方法:
(3)已知X常用于检验
 ,它可将
,它可将 氧化成
氧化成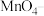 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
4 . 已知 A、B、C、D、E五种元素中,原子序数依次增大,其中A、B、C、D为短周期元素。请根据下表中的信息回答有关问题:
(1)写出B基态原子的核外电子排布式____________________ .
(2)写出D原子价电子的轨道表示式为____________________ .
(3)E元素位于第______ 周期________ 族。
(4)写出A2B2的电子式___________ .
(5)写出C与D形成的化合物的化学式:_______________ 。
| 元素 | 结构或性质信息 |
| A | 原子半径最小的元素 |
| B | 原子最外能层的p能级中有一个轨道充填了2个电子。 |
| C | 原子的第一至第四电离能分别是:I1=841kJ/mol I2 = 1637 kJ/mol I3 = 3577kJ/mol I4 = 18540kJ/mol |
| D | 基态原子的核外电子共有17种运动状态 |
| E | 元素的价电子排布式为(n-l)dn+6ns2。 |
(2)写出D原子价电子的轨道表示式为
(3)E元素位于第
(4)写出A2B2的电子式
(5)写出C与D形成的化合物的化学式:
您最近一年使用:0次
2021-05-15更新
|
321次组卷
|
2卷引用:福建省宁德市高中同心顺联盟校2020-2021学年高二下学期期中考试化学试题
名校
解题方法
5 . A,B,C,D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型:C,D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号)
(2)单质A有两种同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为_______ ,中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ ;晶胞中A原子的配位数为_______ ;列式计算晶体F的密度(g·cm-3)_______ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为

您最近一年使用:0次
6 . 夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌、鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色。请回答下列问题:
(1)火焰利用了部分金属元素特征的__________ 反应,该反应属于__________ (填“物理”或“化学”)变化。
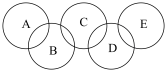
(2)如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含的电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:
,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,其主要的电离方程式可表示为___________________ ,D的化学式是___________________ 。
②A、B、E中均含有的一种元素为___________________ (填元素名称)。
③E的电子式为___________________ 。
④液态B与液态E反应可生成一种气态单质和一种常见液体,1mol B参加反应放出热量Q kJ,其反应的热化学方程式为___________________ 。
⑤ 分子中的N原子有一对孤对电子,能发生反应:
分子中的N原子有一对孤对电子,能发生反应: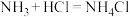 。试写出E与足量盐酸发生反应的化学方程式:
。试写出E与足量盐酸发生反应的化学方程式:______________________________________ 。

(1)火焰利用了部分金属元素特征的
(2)如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含的电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
 ,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:
,C可作光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,两元素的原子序数之比为2:1。根据以上信息回答下列问题:①B的水溶液呈弱酸性,其主要的电离方程式可表示为
②A、B、E中均含有的一种元素为
③E的电子式为
④液态B与液态E反应可生成一种气态单质和一种常见液体,1mol B参加反应放出热量Q kJ,其反应的热化学方程式为
⑤
 分子中的N原子有一对孤对电子,能发生反应:
分子中的N原子有一对孤对电子,能发生反应: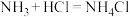 。试写出E与足量盐酸发生反应的化学方程式:
。试写出E与足量盐酸发生反应的化学方程式:
您最近一年使用:0次
20-21高二·全国·单元测试
7 . X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W位于元素周期表第_______ 周期第_______ 族;W的原子半径比X的_______ (填“大”或“小”)。
(2)Z的第一电离能比W的_______ (填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是_______ ;氢、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称_______ 。
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(2)Z的第一电离能比W的
您最近一年使用:0次
名校
8 . A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐X;D与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、F这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
请回答下列问题:
(1)写出B、C、E元素的名称B_________ 、C___________ 、E____________ ;
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为_______________ ;
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)_________________ ;
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为____________ 。
(5)A、C、D、F四种元素可以形成两种酸式盐 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为_____ 、______ ,这两种酸式盐相互反应的离子方程式为______________________ 。
请回答下列问题:
(1)写出B、C、E元素的名称B
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为
(5)A、C、D、F四种元素可以形成两种酸式盐
 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为
您最近一年使用:0次
2019-06-13更新
|
389次组卷
|
2卷引用:湖南省长沙市第一中学2020-2021学年高二上学期入学考试化学试题
解题方法
9 . A、B、C、D、E、F六种元素,原子序数依次增大,A是周期表中原子半径最小的元素,B原子的最外层上有4个电子;D的阴离子和E的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体,F的L层电子数等于K、M两个电子层上的电子数之和。(用元素符号或化学式 填空回答以下问题)
(1)C元素在周期表中的位置_______ 。
(2)B、D两元素形成化合物属于(“离子”或“共价”)_______ 化合物。
(3)F原子结构示意图为_______ 。
(4)写出E2D2与BD2反应的化学方程式:_______ 。
(5)B、C、D的最简单氢化物稳定性由强到弱依次为:_______ 。(填化学式)
(6)写出F元素的最高价氧化物的水化物和B反应的化学方程式:_______ 。
(1)C元素在周期表中的位置
(2)B、D两元素形成化合物属于(“离子”或“共价”)
(3)F原子结构示意图为
(4)写出E2D2与BD2反应的化学方程式:
(5)B、C、D的最简单氢化物稳定性由强到弱依次为:
(6)写出F元素的最高价氧化物的水化物和B反应的化学方程式:
您最近一年使用:0次
2021-10-09更新
|
154次组卷
|
2卷引用:甘肃省庆阳市第六中学2020-2021学年高二下学期期末考试化学试题
解题方法
10 . W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
2019-09-26更新
|
386次组卷
|
2卷引用:浙江省平阳县万全综合高级中学2022-2023学年高二下学期第一次月考化学试题



