名校
1 . 已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外电子层的p能级处于半充满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。回答下列问题:
(1)E元素基态原子的电子排布式为___________ 。
(2)用轨道表示式表示F元素原子的价电子排布:___________ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的是___________ (填化学式)。
(4)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为___________ 。试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:___________ 。
(1)E元素基态原子的电子排布式为
(2)用轨道表示式表示F元素原子的价电子排布:
(3)F、G元素对应的最高价含氧酸中酸性较强的是
(4)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
您最近一年使用:0次
名校
2 . 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出下列元素的名称:A_______ ,B_______ ,C_______ ,D_______ 。
(2)D元素在周期表中的位置_______ 。
(3)室温下,由A、B、C三种元素形成的化合物水溶液pH为11,该溶液中由水电离出的OH-浓度为_______ ;该化合物的热溶液去油污能力更强的原因是_______  。
。
(4)由C、D两种元素形成的化合物水溶液呈_______ (填“酸”、“中”、“碱”)性,原因是_______ 。(用离子方程式表示)
(1)写出下列元素的名称:A
(2)D元素在周期表中的位置
(3)室温下,由A、B、C三种元素形成的化合物水溶液pH为11,该溶液中由水电离出的OH-浓度为
 。
。(4)由C、D两种元素形成的化合物水溶液呈
您最近一年使用:0次
10-11高二上·浙江杭州·阶段练习
3 . 短周期主族元素R的族序数是其周期序数的2倍,R在其最高价氧化物中的质量分数为400/0。已知R原子核内的质子数与中子数相等。试通过计算:
(1)确定R是什么元素_______ ;
(2)确定R元素在周期表中的位置_______ 。
(1)确定R是什么元素
(2)确定R元素在周期表中的位置
您最近一年使用:0次
名校
解题方法
4 . A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A原子核内无中子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的 ,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.请回答下列问题:
,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.请回答下列问题:
(1)C元素在元素周期表中的位置是___ ;C、D、E三种元素简单离子半径由大到小的顺序为:___ (用离子符号表示)。
(2)写出分别由A、D与C形成的原子个数比为1:1的化合物的电子式___ 、___ 。
(3)A与C、E间分别形成甲、乙两种共价化合物,且甲有10个电子,乙有18个电子,则沸点较高的是___ (填化学式)。
(4)F含有的化学键类型是___ 、___ 。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该反应的离子方程式为___ 。
 ,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.请回答下列问题:
,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.请回答下列问题:(1)C元素在元素周期表中的位置是
(2)写出分别由A、D与C形成的原子个数比为1:1的化合物的电子式
(3)A与C、E间分别形成甲、乙两种共价化合物,且甲有10个电子,乙有18个电子,则沸点较高的是
(4)F含有的化学键类型是
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该反应的离子方程式为
您最近一年使用:0次
2020-05-11更新
|
156次组卷
|
3卷引用:湖北省襄阳五中2020-2021学年高二上学期入学考试化学试题
13-14高一下·浙江温州·期中
名校
解题方法
5 . A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族.
(1)D在周期表中的位置______ ;B的原子结构示意图______ ;
(2)E元素形成最高价氧化物对应的水化物的化学式为______ ;
(3)元素C、D、E形成的原子半径大小关系是______ (用元素符号表示).
(4)C、D可形成化合物D2C2,D2C2含有的化学键是______ ;
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式______ ,
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式_____ 。
(1)D在周期表中的位置
(2)E元素形成最高价氧化物对应的水化物的化学式为
(3)元素C、D、E形成的原子半径大小关系是
(4)C、D可形成化合物D2C2,D2C2含有的化学键是
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
2018-09-25更新
|
298次组卷
|
3卷引用:【全国百强校】安徽省合肥市一六八中学2018-2019学年高二开学考试化学试题
【全国百强校】安徽省合肥市一六八中学2018-2019学年高二开学考试化学试题(已下线)2013-2014学年浙江省温州市十校联合体高一下学期期中联考化学试卷新疆石河子第二中学2018-2019学年高一下学期第一次月考化学试题
6 . 随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。
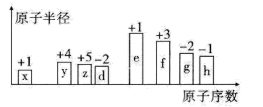
请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点___________ (填“高”或“低”),原因是:___________ ;x与e形成的化合物电子式为___________
(2)比较g、h常见离子的半径大小:___________ (填化学式,下同);比较e、f的最高价氧化物对应水化物的碱性强弱:___________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为___________ 。
②能形成共价化合物,写出其中一种的结构简式___________ 。

请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点
(2)比较g、h常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近一年使用:0次
解题方法
7 . 硫元素有多种化合价,如图表示了含硫物质(甲~辛)与硫的化合价及相应物质类别物质类别之间的关系。
回答下列问题:
(1)物质甲的分子式为_______ 。
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是_________ (填标号)。
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:______ 。
| 物质类别 | ||||||
| 盐 | 戊 | 辛 | ||||
| 含氧酸 | 丁 | 庚 | ||||
| 氧化物 | 丙 | 己 | ||||
| 单质 | 乙 | |||||
| 氢化物 | 甲 | |||||
| -2 | 0 | +2 | +4 | +6 | 化合价 |
(1)物质甲的分子式为
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:
您最近一年使用:0次
名校
8 . 如表是元素周期表的一部分,针对表中的①~⑩元素,回答下列问题:
(1)在这些元素中,非金属性最强的元素符号是______ ;
(2)⑧元素的氢化物的化学式为___________ ;
(3)金属性最活泼的元素的原子结构示意图为______________ ;
(4)能用来雕刻玻璃的氢化物的化学式是__________ ;
(5)④、⑨、⑩三种元素的原子半径由大到小的排列顺序为__________ (用元素符号表示);
(6)写出③元素的气态氢化物和⑨元素的最高价氧化物对应水化物相互反应的化学方程式_________________________ ;
(7)在⑤、⑥、⑦三种元素中,最高价氧化物对应的水化物的碱性最强的是_________ (用化学式表示);
(8)能证明元素⑩比元素⑨的非金属性强的事实是_____ (填序号).
A.常温下⑩单质的密度小于⑨单质的密度
B.⑩元素的气态氢化物比⑨元素的气态氢化物更稳定
C.⑩单质与氢气反应的程度比⑨单质与氢气反应的程度更剧烈
D.⑨元素的最高价氧化物对应的水化物酸性强于⑩元素的最高价氧化物对应的水化物.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)⑧元素的氢化物的化学式为
(3)金属性最活泼的元素的原子结构示意图为
(4)能用来雕刻玻璃的氢化物的化学式是
(5)④、⑨、⑩三种元素的原子半径由大到小的排列顺序为
(6)写出③元素的气态氢化物和⑨元素的最高价氧化物对应水化物相互反应的化学方程式
(7)在⑤、⑥、⑦三种元素中,最高价氧化物对应的水化物的碱性最强的是
(8)能证明元素⑩比元素⑨的非金属性强的事实是
A.常温下⑩单质的密度小于⑨单质的密度
B.⑩元素的气态氢化物比⑨元素的气态氢化物更稳定
C.⑩单质与氢气反应的程度比⑨单质与氢气反应的程度更剧烈
D.⑨元素的最高价氧化物对应的水化物酸性强于⑩元素的最高价氧化物对应的水化物.
您最近一年使用:0次
2016-12-09更新
|
495次组卷
|
2卷引用:福建省龙岩市武平县第一中学2020-2021学年高二下学期开学考试化学试题
解题方法
9 . A,B为两种短周期元素,A的原子序数大于B,且B原子的最外层电子数为A原子最外层电子数的3倍。A,B形成的化合物是中学化学常见的化合物,该化合物熔融时能导电。试回答下列问题:
(1)A,B的元素符号分别是________ 、________ 。
(2)用电子式表示A,B元素形成化合物的过程___________________________________________________ 。
(3)A,B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了________ 个阴离子;晶体中阴、阳离子数之比为________ 。
(4)A,B所形成化合物的晶体的熔点比NaF晶体的熔点________ ,其判断的理由是
________________________________________________________________________ 。
(1)A,B的元素符号分别是
(2)用电子式表示A,B元素形成化合物的过程
(3)A,B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了
(4)A,B所形成化合物的晶体的熔点比NaF晶体的熔点
您最近一年使用:0次
2019-02-26更新
|
162次组卷
|
2卷引用:云南省玉溪市江川区第二中学2018-2019学年高二上学期期末考试化学试题
2011·江西·二模
10 . 已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单元为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
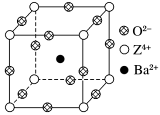
(1) Y在周期表中位于______________ ;Z4+的核外电子排布式为___________________ 。
(2)X的该种氢化物分子构型为________ ,X在该氢化物中以_______ 方式杂化。X和Y形成的化合物的熔点应该_______ (填“高于”或“低于”)X的氢化物的熔点。
(3)①制备M的化学方程式是_____________ 。
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的________ 。
③在M晶体中,Z4+的氧配位数为________ 。
④已知O2-半径为1.40×10-10 m,则Z4+半径为____ m。

(1) Y在周期表中位于
(2)X的该种氢化物分子构型为
(3)①制备M的化学方程式是
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的
③在M晶体中,Z4+的氧配位数为
④已知O2-半径为1.40×10-10 m,则Z4+半径为
您最近一年使用:0次
2016-12-09更新
|
1125次组卷
|
5卷引用:黑龙江省齐齐哈尔市第八中学2017-2018学年高二6月月考化学试题
黑龙江省齐齐哈尔市第八中学2017-2018学年高二6月月考化学试题新疆奎屯市第一高级中学2018-2019学年高二下学期第一次月考化学试题(已下线)2011届江西省重点中学协作体高三第二次联考(理综)化学部分苏教版2017届高三单元精练检测十一化学试题山东省章丘市第四中学2019届高三上学期第二次质量检测理综化学试题



