名校
解题方法
1 . 已知原子序数依次增大的前四周期五种常见元素X、Y、Z、W、R,其相关信息如下:X的原子结构中,最外层电子数是内层电子数的2倍;Z形成的多种同素异形体,其中之一是地球生物的“保护伞”;W的一种单质是黄色粉末,难溶于水,易溶于二硫化碳;R单质在氯气中燃烧会产生棕黄色的烟,该烟溶于少量水中显绿色。
(1)X在元素周期表中的位置:__ 。
(2)Y的简单氢化物遇到Cl2可以产生白烟现象,化工上常利用该性质检查氯气,该“白烟”的电子式:___ 。
(3)写出Y与Z形成的化合物对环境的影响:__ (写出一条即可)。
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,其原因是__ (用离子方程式表示)。
(5)W的简单氢化物与Z的单质在烧碱溶液中可以形成燃料电池(产物中无沉淀生成),写出负极反应式:__ 。
(6)R2Z投入足量的某浓度的硝酸中,所得气体产物为NO和NO2的混合物,且体积比为1:1,发生反应的化学方程式为:__ 。
(1)X在元素周期表中的位置:
(2)Y的简单氢化物遇到Cl2可以产生白烟现象,化工上常利用该性质检查氯气,该“白烟”的电子式:
(3)写出Y与Z形成的化合物对环境的影响:
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,其原因是
(5)W的简单氢化物与Z的单质在烧碱溶液中可以形成燃料电池(产物中无沉淀生成),写出负极反应式:
(6)R2Z投入足量的某浓度的硝酸中,所得气体产物为NO和NO2的混合物,且体积比为1:1,发生反应的化学方程式为:
您最近一年使用:0次
2020-04-09更新
|
46次组卷
|
2卷引用:江西省赣州市赣州县第三中学2019-2020学年高二下学期入学考试化学试题
2 . U、V、W、X、Y、Z 是原子序数依次增大的六种常见元素,Y 的单质在W2中燃烧的产物可使品红溶液褪色。Z 的单质在W2中燃烧的产物Z3W4具有磁性。U 的单质在W2中燃烧可生成UW 和 UW2两种气体。X 的单质是一种金属,该金属在 UW2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)V 的单质分子的电子式为______ 。
(2)U 元素形成的具有空间网状结构的单质,高温使其熔化断裂的化学键类型是______ 。
(3)U、V、W 形成的 10 电子氢化物中,稳定性最强的是:______ (写化学式)。
(4)金属X在UW2中剧烈燃烧的反应方程式为______ ;Z3W4与稀硫酸反应的离子方程式为 ______ 。
(1)V 的单质分子的电子式为
(2)U 元素形成的具有空间网状结构的单质,高温使其熔化断裂的化学键类型是
(3)U、V、W 形成的 10 电子氢化物中,稳定性最强的是:
(4)金属X在UW2中剧烈燃烧的反应方程式为
您最近一年使用:0次
解题方法
3 . 已知A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是__________ ;从轨道重叠的方式看,B分子中的共价键类型有__________ 。
(2)写出②中反应的化学方程式:___________________________________________ 。
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:_________________________________________________ 。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是
(2)写出②中反应的化学方程式:
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:
您最近一年使用:0次
2018-02-15更新
|
106次组卷
|
2卷引用:人教版2017-2018学年高二化学选修三同步训练:2.2 分子的立体构型(第1课时)
名校
4 . 现有部分元素的性质或原子结构信息如表,据此回答下列问题:
(1)元素X的基态原子核外共有________ 种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________ 。
(2)元素Y的价电子排布图为________________ ,元素Y与元素T相比,电负性较大的是________ (用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________ ,稳定性比较:W3+________ W2+(填“>”或“<”),原因是__________________________________________________________________________ 。
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有
(2)元素Y的价电子排布图为
(3)元素Z与元素T相比,非金属性强的是
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为
您最近一年使用:0次
5 . 下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
回答下列问题:
(1)上述元素中②元素的名称_______ ;⑤元素在周期表中的位置是________ 。
(2)在③、⑦、⑧的气态氢化物中最稳定的是_____ (用化学式表示);⑦的最高价氧化物对应水化物的化学式是________ 。
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是________ 。
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强________ 。
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。__________________________ 。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | V A | Ⅵ A | Ⅶ A | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中②元素的名称
(2)在③、⑦、⑧的气态氢化物中最稳定的是
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。
您最近一年使用:0次
6 . J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为__________ ;元素T在周期表中位于第________ 族。
(2)J元素名称是______ ,他和氢组成10电子的化合物,其分子式为______________ ,属___________ (填“离子化合物”或“共价化合物”)。
(3)R元素符号为_______ ,其最高能层符号是________ 。
| J | ||||
| R |
(2)J元素名称是
(3)R元素符号为
您最近一年使用:0次
名校
解题方法
7 . 现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A的氧化物能够造成温室效应;A、B、C三种元素都能形成10电子分子,且C与F位于同一主族;D与C可形成离子化合物DC;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第______ 周期第______ 族。
(2)请写出B的氢化物可能的电子式_________ 、_________ 。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为__________ (用化学式表示)。
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:_________ 。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为__________ (用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是____ (填字母序号)。
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是_______ 、_________ (写出化学式)。
(1)B位于周期表第
(2)请写出B的氢化物可能的电子式
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为
(6)下列实验方法能证明D与E的金属性强弱关系的是
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是
您最近一年使用:0次
8 . 下表为元素周期表中的一部分,列出10种元素在元素周期表中的位置.用化学符号回答下列各问题.
(1)10种元素中,化学性质最不活泼的是_________ .
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是_________ .
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_________ .
(4)元素⑦的简单氢化物的化学式为_____ ;若该氢化物和元素⑨的单质反应,则化学方程式为_______ .
(5)⑤和⑨的最高价氧化物对应水化物的化学式分别为_________ 和_________ .
(6)①和⑤最高价氧化物对应水化物相互反应的离子方程式为__________________ .
 族 族周期 | 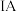 | 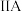 | 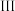 | 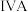 | 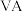 | 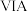 |  | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)10种元素中,化学性质最不活泼的是
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是
(4)元素⑦的简单氢化物的化学式为
(5)⑤和⑨的最高价氧化物对应水化物的化学式分别为
(6)①和⑤最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 随原子序数的递增,五种短周期元素原子半径与原子序数的关系如图所示。
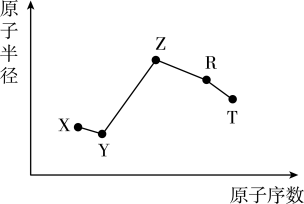
已知:TX2是现代光学及光纤制品的基本原料;
ZY 能破坏水的电离平衡;Z3RY6在工业上常用作助熔剂。
(1)R在元素周期表中的位置是___ 。
(2)上述元素中的某两种元素可组成一种五原子共价化合物,该化合物的结构式为___ 。
(3)请用一个化学方程式比较X和Y的非金属性的强弱_____ 。
(4)工业上以Z3RY6作助熔剂的目的是____ 。

已知:TX2是现代光学及光纤制品的基本原料;
ZY 能破坏水的电离平衡;Z3RY6在工业上常用作助熔剂。
(1)R在元素周期表中的位置是
(2)上述元素中的某两种元素可组成一种五原子共价化合物,该化合物的结构式为
(3)请用一个化学方程式比较X和Y的非金属性的强弱
(4)工业上以Z3RY6作助熔剂的目的是
您最近一年使用:0次
10-11高二下·浙江宁波·阶段练习
解题方法
10 . 有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物。
试根据以上叙述回答:
(1)元素名称: A______ B _____ C _____ D ______ 。
(2)D元素位于周期表中______ 周期___________ 族。
(3)写出AB2与C2B2反应的化学方程式________________________________________________ 。
(4)画出B的原子结构简图___________________ 。
(5)用电子式表示化合物 C2D 的形成过程:__________________________________ 。
试根据以上叙述回答:
(1)元素名称: A
(2)D元素位于周期表中
(3)写出AB2与C2B2反应的化学方程式
(4)画出B的原子结构简图
(5)用电子式表示化合物 C2D 的形成过程:
您最近一年使用:0次



