1 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示: 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
2023-06-10更新
|
20815次组卷
|
21卷引用:第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)暑假作业19 化学工艺流程题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)2023年高考新课标理综化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省滨州市2023-2024学年高三上学期11月期中考试化学试题新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建(已下线)专题15 工艺流程综合题-备战2025年高考化学真题题源解密(新高考通用)(已下线)第05讲 工业流程解题策略(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
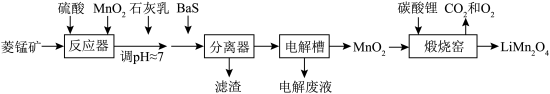
2 . LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如下:
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______ 。为提高溶矿速率,可采取的措施_______ (举1例)。
(2)加入少量MnO2的作用是_______ 。不宜使用H2O2替代MnO2,原因是_______ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______ mol·L-1;用石灰乳调节至pH≈7,除去的金属离子是_______ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______ 。
(5)在电解槽中,发生电解反应的离子方程式为_______ 。随着电解反应进行,为保持电解液成分稳定,应不断_______ 。电解废液可在反应器中循环利用。
(6)煅烧窑中,生成LiMn2O4反应的化学方程式是_______ 。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有
(5)在电解槽中,发生电解反应的离子方程式为
(6)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近一年使用:0次
2023-06-12更新
|
18137次组卷
|
16卷引用:第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)河北省石家庄市正定中学2022- 2023学年高二下学期期末考试化学试题(已下线)暑假作业06 以简单工艺流程突破元素化合物知识和应用-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)2023年高考全国乙卷化学真题(已下线)T27-工业流程题(已下线)2023年高考化学真题完全解读(全国乙卷)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)上海市曹杨第二中学2024届高三下学期五月份月考化学试题2024届河南省郑州市第一中学高三下学期考前全真模拟考试理科综合试题-高中化学(已下线)专题15 工艺流程综合题-备战2025年高考化学真题题源解密(新高考通用)(已下线)第05讲 工业流程解题策略(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
真题
名校
3 . 实验室由安息香制备二苯乙二酮的反应式如下:
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入 冰乙酸、
冰乙酸、 水及
水及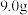
 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入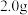 安息香,加热回流
安息香,加热回流 。
。
③加入 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色结晶
的乙醇重结晶,干燥后得淡黄色结晶 。
。
(1)仪器A中应加入_______ (填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______ ;冷却水应从_______ (填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______ 。
(4)在本实验中, 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为_______ ;某同学尝试改进本实验:采用催化量的 并通入空气制备二苯乙二酮。该方案是否可行
并通入空气制备二苯乙二酮。该方案是否可行_______ ?简述判断理由_______ 。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______ 。
(6)若粗品中混有少量未氧化的安息香,可用少量_______ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______ (填标号)。
a. b.
b. c.
c. d.
d.
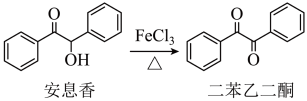
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
①在圆底烧瓶中加入
 冰乙酸、
冰乙酸、 水及
水及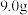
 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入
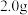 安息香,加热回流
安息香,加热回流 。
。③加入
 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用
 的乙醇重结晶,干燥后得淡黄色结晶
的乙醇重结晶,干燥后得淡黄色结晶 。
。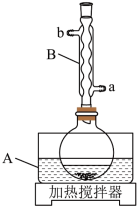
(1)仪器A中应加入
(2)仪器B的名称是
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(4)在本实验中,
 为氧化剂且过量,其还原产物为
为氧化剂且过量,其还原产物为 并通入空气制备二苯乙二酮。该方案是否可行
并通入空气制备二苯乙二酮。该方案是否可行(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是
(6)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于
a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2023-06-10更新
|
17645次组卷
|
22卷引用:第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)广东省广州市第二中学2022-2023学年高二下学期期末考试化学试题江西省宜春市丰城中学2023-2024学年高二上学期12月月考化学试题河南省新乡市九校联盟2023-2024学年高二下学期质量检测化学试题山东省东营市利津县高级中学2023-2024学年高二下学期5月月考化学试题青海省西宁市第十四中学2023-2024学年高二下学期期末考试化学试卷安徽省合肥一中肥东分校2023-2024学年高二下学期第二次月考化学试题福建省南安市蓝园高级中学2023-2024学年高二下学期期中考试化学试题四川省遂宁中学高新校区2023-2024学年高二下学期6月半月考试化学试题2023年高考新课标理综化学真题(已下线)T27-实验题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)T27-实验题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型三 以分离提纯为主的有机制备类实验-备战2024年高考化学答题技巧与模板构建湖南省株洲市第一中学2021届高三下学期第三次模拟检测化学试题(已下线)专题16 化学实验综合题-备战2025年高考化学真题题源解密(新高考通用)(已下线)第04讲 综合实验题型探究(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
4 . 硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(1)在 气氛中,
气氛中, 的脱水热分解过程如图所示:
的脱水热分解过程如图所示:
_______ ,
_______ 。
(2)已知下列热化学方程式:
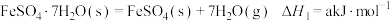


则 的
的
_______  。
。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: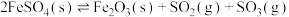 (Ⅰ)。平衡时
(Ⅰ)。平衡时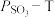 的关系如下图所示。
的关系如下图所示。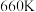 时,该反应的平衡总压
时,该反应的平衡总压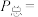
_______  、平衡常数
、平衡常数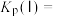
_______  。
。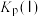 随反应温度升高而
随反应温度升高而_______ (填“增大”“减小”或“不变”)。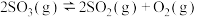 (Ⅱ),平衡时
(Ⅱ),平衡时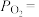
_______ (用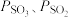 表示)。在
表示)。在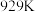 时,
时, ,则
,则
_______  ,
,
_______  (列出计算式)。
(列出计算式)。
(1)在
 气氛中,
气氛中, 的脱水热分解过程如图所示:
的脱水热分解过程如图所示: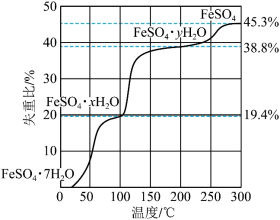


(2)已知下列热化学方程式:
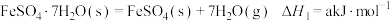


则
 的
的
 。
。(3)将
 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: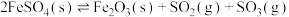 (Ⅰ)。平衡时
(Ⅰ)。平衡时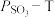 的关系如下图所示。
的关系如下图所示。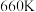 时,该反应的平衡总压
时,该反应的平衡总压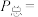
 、平衡常数
、平衡常数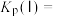
 。
。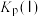 随反应温度升高而
随反应温度升高而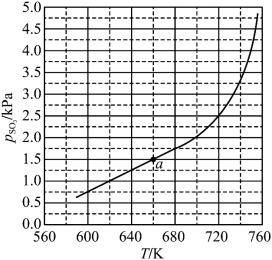
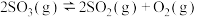 (Ⅱ),平衡时
(Ⅱ),平衡时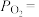
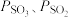 表示)。在
表示)。在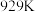 时,
时, ,则
,则
 ,
,
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2023-06-12更新
|
17691次组卷
|
12卷引用:第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)【知识图鉴】单元讲练测选择性必修1第2单元03巩固练(已下线)暑假作业15 突破化学反应原理综合题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)2023年高考全国乙卷化学真题(已下线)T28-原理综合题(已下线)2023年高考化学真题完全解读(全国乙卷)(PPT+Word)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题18 化学反应原理综合题-备战2025年高考化学真题题源解密(新高考通用)
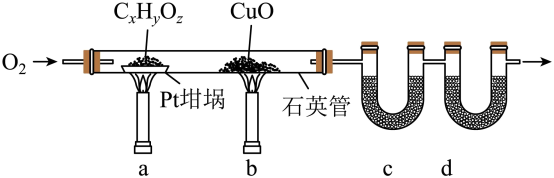
5 . 元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。
(1)将装有样品的Pt坩埚和CuO放入石英管中,先_______ ,而后将已称重的U型管c、d与石英管连接,检查_______ 。依次点燃煤气灯_______ ,进行实验。
(2)O2的作用有_______ 。CuO的作用是_______ (举1例,用化学方程式表示)。
(3)c和d中的试剂分别是_______ 、_______ (填标号)。c和d中的试剂不可调换,理由是_______ 。
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:_______ 。取下c和d管称重。
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为_______ 。
(1)将装有样品的Pt坩埚和CuO放入石英管中,先
(2)O2的作用有
(3)c和d中的试剂分别是
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为
您最近一年使用:0次
2023-06-12更新
|
15844次组卷
|
21卷引用:吉林省长春市第五中学2022-2023学年高二下学期第三学程(期末)化学试题
吉林省长春市第五中学2022-2023学年高二下学期第三学程(期末)化学试题吉林省长春市实验中学2022-2023学年高二下学期期末考试化学试题湖北省鄂东南省级示范高中教育教学改革联盟学校2023-2024学年高二下学期期中联考化学试卷山东省淄博市临淄中学2023-2024学年高二下学期阶段检测化学试题 黑龙江省黑河市第一中学2023-2024学年高二下学期6月月考化学试题2023年高考全国乙卷化学真题(已下线)T26-实验题(已下线)2023年高考化学真题完全解读(全国乙卷)(PPT+Word)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)第17讲实验方案的设计与评价新疆疏附县第一中学2023-2024学年高三上学期开学摸底测试化学试题(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型一 实验简答题答题规范-备战2024年高考化学答题技巧与模板构建河南省许昌市禹州市高级中学2023-2024学年高三下学期4月月考理综试题-高中化学(已下线)第04讲 金属材料及金属矿物的开发利用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)(已下线)专题16 化学实验综合题-备战2025年高考化学真题题源解密(新高考通用)(已下线)第04讲 综合实验题型探究(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
6 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(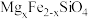 )。回答下列问题:
)。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ 。橄榄石中,各元素电负性大小顺序为_______ ,铁的化合价为_______ 。
(2)已知一些物质的熔点数据如下表:
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是_______ 。分析同族元素的氯化物 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因_______ 。 的空间结构为
的空间结构为_______ ,其中 的轨道杂化形式为
的轨道杂化形式为_______ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有_______ 个 。该物质化学式为
。该物质化学式为_______ ,B-B最近距离为_______ 。
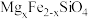 )。回答下列问题:
)。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
 | 800.7 |
 |  |
 | 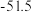 |
 |  |
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是 、
、 、
、 熔点变化趋势及其原因
熔点变化趋势及其原因 的空间结构为
的空间结构为 的轨道杂化形式为
的轨道杂化形式为(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有
 。该物质化学式为
。该物质化学式为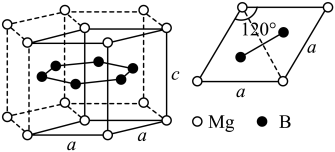
您最近一年使用:0次
2023-06-12更新
|
15944次组卷
|
18卷引用:第21练 物质结构与性质综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第21练 物质结构与性质综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)湖南省永州市第一中学2023-2024学年高二下学期开学考试化学试题重庆市荣昌中学校2023-2024学年高二下学期4月期中考试化学试题四川省射洪中学校2023-2024学年高二下学期5月期中化学试题(已下线)暑假作业16 掌握物质结构与性质综合题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)福建省泉州晋江二中等五校2023-2024学年高二下学期期末联考化学试卷 2023年高考全国乙卷化学真题(已下线)T35-结构与性质(已下线)2023年高考化学真题完全解读(全国乙卷)(PPT+Word)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)第22讲晶体结构与性质山东省潍坊市昌乐二中2023-2024学年高三上学期12月月考化学试题2024届四川省雅安市神州天立学校高三下学期高考冲刺考试理科综合试题-高中化学
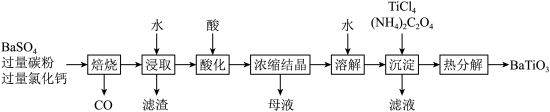
7 .  是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状 。
。
(1)“焙烧”步骤中碳粉的主要作用是_______ 。
(2)“焙烧”后固体产物有 、易溶于水的
、易溶于水的 和微溶于水的
和微溶于水的 。“浸取”时主要反应的离子方程式为
。“浸取”时主要反应的离子方程式为_______ 。
(3)“酸化”步骤应选用的酸是_______ (填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______ ,其原因是_______ 。
(5)“沉淀”步骤中生成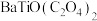 的化学方程式为
的化学方程式为_______ 。
(6)“热分解”生成粉状钛酸钡,产生的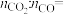
_______ 。
 是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状 。
。
(1)“焙烧”步骤中碳粉的主要作用是
(2)“焙烧”后固体产物有
 、易溶于水的
、易溶于水的 和微溶于水的
和微溶于水的 。“浸取”时主要反应的离子方程式为
。“浸取”时主要反应的离子方程式为(3)“酸化”步骤应选用的酸是
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?
(5)“沉淀”步骤中生成
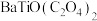 的化学方程式为
的化学方程式为(6)“热分解”生成粉状钛酸钡,产生的
您最近一年使用:0次
2023-06-09更新
|
15697次组卷
|
20卷引用:第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)暑假作业06 以简单工艺流程突破元素化合物知识和应用-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)(已下线)暑假作业19 化学工艺流程题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)山东省菏泽市定陶区第一中学2023-2024学年高二下学期期末模拟化学试题江苏省南京市第一中学(北校区)2023-2024学年高二上学期9月阶段性考试检测化学试卷2023年高考全国甲卷化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建四川省遂宁市射洪中学校2023-2024学年高一(强基班)下学期期末模拟考试化学试题山西省大同市浑源县第七中学校2023-2024学年高一下学期期末考试化学试题 (已下线)专题15 工艺流程综合题-备战2025年高考化学真题题源解密(新高考通用)(已下线)第05讲 工业流程解题策略(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
8 . 钴配合物 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备: 。
。
具体步骤如下:
Ⅰ.称取 ,用
,用 水溶解。
水溶解。
Ⅱ.分批加入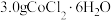 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入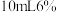 的双氧水。
的双氧水。
Ⅲ.加热至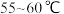 反应
反应 。冷却,过滤。
。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的 沸水中,趁热过滤。
沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。_______ 。加快NH4Cl溶解的操作有_______ 。
(2)步骤Ⅱ中,将温度降至10℃以下以避免_______ 、_______ ;可选用_______ 降低溶液温度。
(3)指出下列过滤操作中不规范之处:_______ 。_______ 。
(5)步骤Ⅴ中加入浓盐酸的目的是_______ 。
 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备: 。
。具体步骤如下:
Ⅰ.称取
 ,用
,用 水溶解。
水溶解。Ⅱ.分批加入
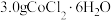 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入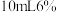 的双氧水。
的双氧水。Ⅲ.加热至
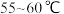 反应
反应 。冷却,过滤。
。冷却,过滤。Ⅳ.将滤得的固体转入含有少量盐酸的
 沸水中,趁热过滤。
沸水中,趁热过滤。Ⅴ.滤液转入烧杯,加入
 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。
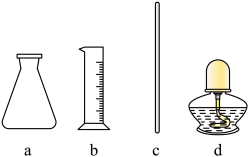
(2)步骤Ⅱ中,将温度降至10℃以下以避免
(3)指出下列过滤操作中不规范之处:
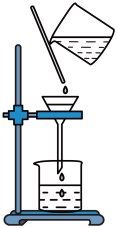
(5)步骤Ⅴ中加入浓盐酸的目的是
您最近一年使用:0次
2023-06-09更新
|
14858次组卷
|
19卷引用:第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)山东省青岛市即墨区第一中学2023-2024学年高二下学期6月月考化学试题(已下线)实验04简单配合物的形成-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修2)2023年高考全国甲卷化学真题(已下线)T27-实验题(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题19 实验综合题(已下线)2023年高考山东卷化学真题变式题(实验综合题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)考点巩固卷13 化学实验基础(二)(3个考点30题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)第14讲化学实验常用仪器及基本操作(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型一 实验简答题答题规范-备战2024年高考化学答题技巧与模板构建甘肃省平凉市泾川县第三中学2023-2024学年高三上学期第3次月考化学试题上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题(已下线)专题16 化学实验综合题-备战2025年高考化学真题题源解密(新高考通用)
9 . 甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①

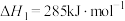
②

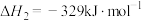
反应③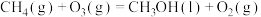 的
的
_______  ,平衡常数
,平衡常数
_______ (用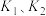 表示)。
表示)。
(2)电喷雾电离等方法得到的 (
(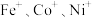 等)与
等)与 反应可得
反应可得 。
。 与
与 反应能高选择性地生成甲醇。分别在
反应能高选择性地生成甲醇。分别在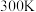 和
和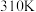 下(其他反应条件相同)进行反应
下(其他反应条件相同)进行反应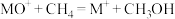 ,结果如下图所示。图中
,结果如下图所示。图中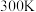 的曲线是
的曲线是_______ (填“a”或“b”。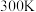 、
、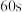 时
时 的转化率为
的转化率为_______ (列出算式)。 分别与
分别与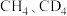 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示例)。
示例)。_______ (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则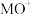 与
与 反应的能量变化应为图中曲线
反应的能量变化应为图中曲线_______ (填“c”或“d”)。
(ⅲ) 与
与 反应,氘代甲醇的产量
反应,氘代甲醇的产量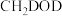
_______ 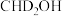 (填“>”“<”或“=”)。若
(填“>”“<”或“=”)。若 与
与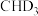 反应,生成的氘代甲醇有
反应,生成的氘代甲醇有_______ 种。
(1)已知下列反应的热化学方程式:
①


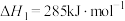
②


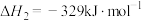
反应③
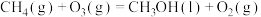 的
的
 ,平衡常数
,平衡常数
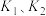 表示)。
表示)。(2)电喷雾电离等方法得到的
 (
(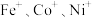 等)与
等)与 反应可得
反应可得 。
。 与
与 反应能高选择性地生成甲醇。分别在
反应能高选择性地生成甲醇。分别在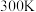 和
和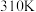 下(其他反应条件相同)进行反应
下(其他反应条件相同)进行反应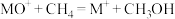 ,结果如下图所示。图中
,结果如下图所示。图中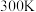 的曲线是
的曲线是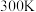 、
、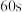 时
时 的转化率为
的转化率为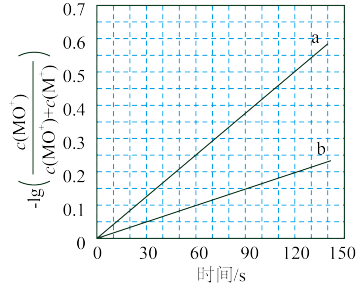
 分别与
分别与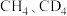 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示例)。
示例)。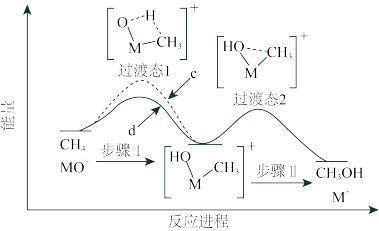
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则
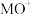 与
与 反应的能量变化应为图中曲线
反应的能量变化应为图中曲线(ⅲ)
 与
与 反应,氘代甲醇的产量
反应,氘代甲醇的产量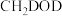
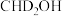 (填“>”“<”或“=”)。若
(填“>”“<”或“=”)。若 与
与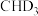 反应,生成的氘代甲醇有
反应,生成的氘代甲醇有
您最近一年使用:0次
2023-06-09更新
|
14479次组卷
|
13卷引用:第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)暑假作业15 突破化学反应原理综合题-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)(已下线)暑假作业08 突破有关反应热的综合考查-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)2023年高考全国甲卷化学真题(已下线)T28-原理综合题(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题17 原理综合题(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷1(已下线)专题18 化学反应原理综合题-备战2025年高考化学真题题源解密(新高考通用)
真题
解题方法
10 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
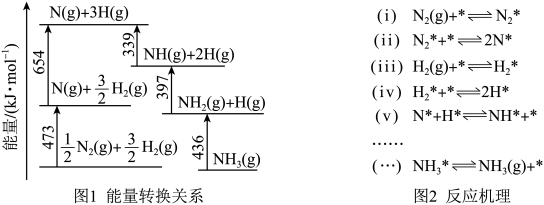
(1)根据图1数据计算反应 的
的
_______  。
。 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,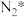 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为_______ (填步骤前的标号),理由是_______ 。
(3)合成氨催化剂前驱体(主要成分为 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为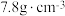 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,阿伏加德罗常数的值为 )。
)。
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为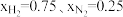 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)_______ ,判断的依据是_______ 。
②进料组成中含有惰性气体 的图是
的图是_______ 。
③图3中,当 、
、 时,氮气的转化率
时,氮气的转化率
_______ 。该温度时,反应 的平衡常数
的平衡常数
_______  (化为最简式)。
(化为最简式)。
(1)根据图1数据计算反应
 的
的
 。
。
 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,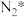 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为(3)合成氨催化剂前驱体(主要成分为
 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为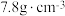 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为
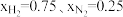 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)
②进料组成中含有惰性气体
 的图是
的图是③图3中,当
 、
、 时,氮气的转化率
时,氮气的转化率
 的平衡常数
的平衡常数
 (化为最简式)。
(化为最简式)。
您最近一年使用:0次



