名校
解题方法
1 . 已知有原子序数依次增大的A、B、C、D、E五种短周期元素和过度金属元素F,其相关信息如下:
①A与C形成的化合物的水溶液呈碱性
②B的最高正价和最低负价的代数和为0
③D的常见化合物的焰色反应为黄色
④E的氧化物属于两性氧化物。
(1)分子式为B5A12且其一氯代物只有一种的有机物的名称为____ .
(2)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈___ 性。
(3)1molD元素的最高价氧化物对应的水化物与2molE元素的单质反应产生气体体积为_______ L(标准状况下)
(4)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为______ .
①A与C形成的化合物的水溶液呈碱性
②B的最高正价和最低负价的代数和为0
③D的常见化合物的焰色反应为黄色
④E的氧化物属于两性氧化物。
(1)分子式为B5A12且其一氯代物只有一种的有机物的名称为
(2)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈
(3)1molD元素的最高价氧化物对应的水化物与2molE元素的单质反应产生气体体积为
(4)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为
您最近一年使用:0次
解题方法
2 . 由两种元素组成的化合物X,是现代工业的重要原料。为探究X的组成,设计并进行如下实验:
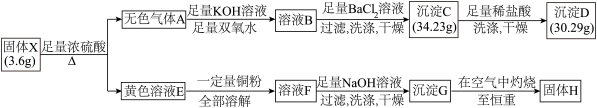
(1)将黄色溶液E稀释后通入无色气体A,发生反应的离子方程式为______________ 。
(2)除 外,溶液F中一定含有的金属阳离子为
外,溶液F中一定含有的金属阳离子为________ ,其检验方法为______________ 。
(3)固体X与浓硫酸反应的化学方程式是_________________ 。
(4)若测得固体H的质量为 ,则溶液E溶解的铜粉质量为
,则溶液E溶解的铜粉质量为________ 。

(1)将黄色溶液E稀释后通入无色气体A,发生反应的离子方程式为
(2)除
 外,溶液F中一定含有的金属阳离子为
外,溶液F中一定含有的金属阳离子为(3)固体X与浓硫酸反应的化学方程式是
(4)若测得固体H的质量为
 ,则溶液E溶解的铜粉质量为
,则溶液E溶解的铜粉质量为
您最近一年使用:0次
名校
解题方法
3 . 如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答:
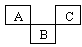
(1)写出元素符号:A____ ;C_____ 。
(2)B的最高价氧化物对应水化物的化学式为____ 。
(3)A的单质的电子式为___ ;A的氢化物的水溶液与其最高价氧化物的水化物反应的化学方程式____ 。

(1)写出元素符号:A
(2)B的最高价氧化物对应水化物的化学式为
(3)A的单质的电子式为
您最近一年使用:0次
2017-07-13更新
|
278次组卷
|
3卷引用:贵州省思南中学2018-2019学年高二下学期期末考试化学试题
名校
4 . 有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A的最外层电子数是次外层电子数的两倍,C是该周期中原子半径最大的元素,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻。试根据以上叙述回答:
(1)元素符号:B______ ;C______ ; E______ ;
(2)画出D的离子结构示意图_______________ ;AB2的结构式_______________ ;
(3)写出 C2B2与AB2反应的化学方程式___________________________________________ ;在该反应中,1mol C2B2参与反应,则转移电子数目为______ ;
(4)D、E的气态氢化物的稳定性_________ 大于_________ (填化学式)。
(1)元素符号:B
(2)画出D的离子结构示意图
(3)写出 C2B2与AB2反应的化学方程式
(4)D、E的气态氢化物的稳定性
您最近一年使用:0次
解题方法
5 . 现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________ 。
(2)写出B的氢化物的电子式_____________________________ 。
(3)由A、D两种元素形成的化合物是________ 化合物(填“离子”或“共价”),化合物内存在________ 键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________ ,它属于________ 化合物,化合物内存在________ 键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________ (多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
(1)试写出它们的元素符号。
(2)写出B的氢化物的电子式
(3)由A、D两种元素形成的化合物是
(4)由D、E两种元素形成的化合物的电子式为
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
您最近一年使用:0次
解题方法
6 . A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第________ 周期第________ 族。
(2)E元素形成的氧化物对应的水化物的化学式为____________________ 。
(3)元素C、D、E形成的简单离子半径大小关系是______ >______ >_____ (用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:____________________ 。C、D还可形成化合物D2C2,D2C2中含有的化学键是________________________ 。
(1)B在周期表中的位置为第
(2)E元素形成的氧化物对应的水化物的化学式为
(3)元素C、D、E形成的简单离子半径大小关系是
(4)用电子式表示化合物D2C的形成过程:
您最近一年使用:0次
11-12高一·全国·课时练习
解题方法
7 . A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
(1)写出A、B、C三元素名称:________ 、________ 、________ 。
(2)C在元素周期表中的位置是__________________________________ 。
(3)B的原子结构示意图为________ ,C的氢化物与B的氢化物的稳定性强弱顺序为________ >________ (填化学式)。
(4)比较A、C的原子半径:A________ (填“>”或“<”)C,写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式:________________________________________________ 。
| A | C | |
| B |
(2)C在元素周期表中的位置是
(3)B的原子结构示意图为
(4)比较A、C的原子半径:A
您最近一年使用:0次
2012-10-28更新
|
1336次组卷
|
9卷引用:黑龙江省青冈县一中2018-2019学年高二上学期开学考试化学试题
黑龙江省青冈县一中2018-2019学年高二上学期开学考试化学试题步步为赢 高二化学暑假作业:作业六 物质结构 元素周期律(已下线)2012年人教版高中化学必修二 1.2 元素周期律练习卷(已下线)2014学年高一化学人教版必修2 1.2.1电子的排布元素周期律练习卷云南省河口县民中2017-2018学年高一下学期期中考试化学试题云南省华宁县第二中学2018-2019学年高一下学期开学考试化学试题甘肃省武威市第五中学2018-2019学年高一下学期第一次月考化学试题安徽省合肥市2019—2020学年高一下学期期中考试化学试题山东省东平明湖中学2022-2023学年高一下学期学情调研化学试题
名校
解题方法
8 . 有三种物质AC2(气体)、B2C2、AD4,元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则:
(1)AC2、AD4的化学式分别为______ 、______ 。
(2)AD4分子其中含有的σ键类型为_______ (填“s-s σ键”“s-p σ键”或“p-p σ键”)。
(3)D的负一价阴离子的电子排布式为_________ ,B2C2的电子式为__________ ,属___________ (填“离子化合物”或“共价化合物”)。
(4)写出一种与AC互为等电子体的分子______________
(1)AC2、AD4的化学式分别为
(2)AD4分子其中含有的σ键类型为
(3)D的负一价阴离子的电子排布式为
(4)写出一种与AC互为等电子体的分子
您最近一年使用:0次
2019-04-22更新
|
82次组卷
|
3卷引用:云南省景谷一中2018-2019学年高二下学期第一次月考化学试题
10-11高二上·河北唐山·期中
9 . 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同。
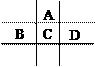
回答下列问题:
(1)A与E形成的化合物的化学式是__________________ 。
(2)B的最高价氧化物化学式为____________ ,C的元素名称为 ___________________ 。
(3)D的单质与水反应的方程式为____________________________________________________ 。

回答下列问题:
(1)A与E形成的化合物的化学式是
(2)B的最高价氧化物化学式为
(3)D的单质与水反应的方程式为
您最近一年使用:0次
解题方法
10 . 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同; D原子的核外成对电子数是未成对电子数的3倍。同时含有A、B、D三种元素的化合物M是一种居室污染气体,其分子中所有的原子共平面。A、B两种元素组成的原子个数比为1︰1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示 )
(1)下列叙述正确的是____________ (填字母)。
A.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
B.M和二氧化碳分子中的中心原子均采用sp2杂化
C.N分子中含有6个σ键和3个π键
D.N分子中所有原子共面
(2)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水,其中Fe为+2价) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式__________________ ,____________________ 。
(3)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是_______ 、_______ 。两者沸点的关系为X_____ Y(填 > 或 < )。
(1)下列叙述正确的是
A.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
B.M和二氧化碳分子中的中心原子均采用sp2杂化
C.N分子中含有6个σ键和3个π键
D.N分子中所有原子共面
(2)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水,其中Fe为+2价) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式
(3)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是
您最近一年使用:0次



