名校
1 . 元素周期表和元素周期律是我们高中化学中的重要理论知识,试回答下列问题:
(1)X元素原子的核电荷数为8,其原子核内的质子数为_____ ,该元素原子的二价阴离子中,核外电子数为_____ ,离子结构示意图为______ ,中子数为9的核素表示为______ 。
(2)向 溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl_____ S(填“>”或“<”),反应的离子方程式为___________ 。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
①铷在元素周期表中的位置是___________ 。
②下列关于铷的说法不正确的是___________ (填序号)。
a.与水反应比钠更剧烈 b.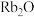 在空气中易吸收水和二氧化碳
在空气中易吸收水和二氧化碳
c.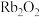 与水能剧烈反应并释放出
与水能剧烈反应并释放出 d.单质具有很强的氧化性
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(4)关于元素周期表、周期律,下列说法正确的是___________(填序号)。
(1)X元素原子的核电荷数为8,其原子核内的质子数为
(2)向
 溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
①铷在元素周期表中的位置是
②下列关于铷的说法不正确的是
a.与水反应比钠更剧烈 b.
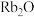 在空气中易吸收水和二氧化碳
在空气中易吸收水和二氧化碳c.
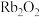 与水能剧烈反应并释放出
与水能剧烈反应并释放出 d.单质具有很强的氧化性
d.单质具有很强的氧化性e.RbOH的碱性比同浓度的NaOH弱
(4)关于元素周期表、周期律,下列说法正确的是___________(填序号)。
| A.在金属和非金属分界处可以找到半导体材料 |
| B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素 |
| C.通常农药所含有的元素位于元素周期表左下方区域 |
| D.稀有气体原子都满足8电子稳定结构 |
您最近半年使用:0次
2 . A、B、C、D是四种元素的原子,质子数都小于20。A原子与B原子的最外层电子数相同,B原子与C原子的核外电子层数相同,0.2 mol C单质与足量稀硫酸反应时放出H2 6.72 L(标准状况),A原子最外层上的电子数比次外层上的电子数多5个,C原子与D原子的质子数之和为32。
(1)A、B、C、D的元素符号分别为_______ 、_______ 、_______ 、_______ 。
(2)A的离子结构示意图为_______ ,C的原子结构示意图为_______ 。
(3)C的硫酸盐的化学式为_______ ,C单质与稀硫酸反应的化学方程式为_______ 。
(1)A、B、C、D的元素符号分别为
(2)A的离子结构示意图为
(3)C的硫酸盐的化学式为
您最近半年使用:0次
解题方法
3 . A、B、C、D、E、F、G是原子序数依次增大的短周期元素,它们的相关信息如表所示。
请回答下列问题:
(1)A的原子结构示意图为______ 。
(2)简单气态氢化物的稳定性A______ B(填“>”“<”或“=”)。
(3)C的简单气态氢化物的空间结构呈______ 形。
(4)C、E、F三种元素对应的简单离子半径由大到小的顺序为______ (用元素的离子符号表示)。
(5)C与D形成的含有非极性共价键的化合物的电子式为______ 。
(6)E的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式为______ 。
(7)下列各项能说明非金属性F<G的是______ (填标号)。
a.含氧酸的酸性:F<G
b.G的单质能与F的简单气态氢化物反应,置换出F的单质
c.单质与Fe发生化合反应,生成物中Fe的化合价:F<G
d.单质的熔沸点:F>G
| 序号 | 相关信息 |
| ① | A的一种同位素常在考古时测定文物的年代 |
| ② | B的最高正价与最低负价的代数和等于2 |
| ③ | C的核电荷数是F的核电荷数的一半 |
| ④ | D、E、F的最高价氧化物对应的水化物两两之间均可反应 |
| ⑤ | G的最外层电子数比次外层电子数少1 |
(1)A的原子结构示意图为
(2)简单气态氢化物的稳定性A
(3)C的简单气态氢化物的空间结构呈
(4)C、E、F三种元素对应的简单离子半径由大到小的顺序为
(5)C与D形成的含有非极性共价键的化合物的电子式为
(6)E的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式为
(7)下列各项能说明非金属性F<G的是
a.含氧酸的酸性:F<G
b.G的单质能与F的简单气态氢化物反应,置换出F的单质
c.单质与Fe发生化合反应,生成物中Fe的化合价:F<G
d.单质的熔沸点:F>G
您最近半年使用:0次
解题方法
4 . 有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体。
⑤D的气态氢化物有臭鸡蛋气味。请写出:
(1)A元素的最高价氧化物的结构式_______
(2)C元素在周期表中的位置_______
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有_______
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为_______
(5)元素D与元素E相比,非金属性较弱的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ (填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物水溶液酸性比D的氢化物水溶液酸性强
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质。
(6)C分别与B、E形成的简单化合物中,熔沸点较高的是_______
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体。
⑤D的气态氢化物有臭鸡蛋气味。请写出:
(1)A元素的最高价氧化物的结构式
(2)C元素在周期表中的位置
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
(5)元素D与元素E相比,非金属性较弱的是
a.常温下D的单质和E的单质状态不同
b.E的氢化物水溶液酸性比D的氢化物水溶液酸性强
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质。
(6)C分别与B、E形成的简单化合物中,熔沸点较高的是
您最近半年使用:0次
名校
解题方法
5 . A,B,C,D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型:C,D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号)
(2)单质A有两种同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为_______ ,中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ ;晶胞中A原子的配位数为_______ ;列式计算晶体F的密度(g·cm-3)_______ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为

您最近半年使用:0次
6 . 短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示。其中X、Y、Z三种元素的质子数之和为21。
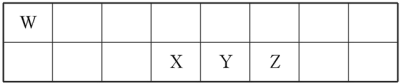
(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是_______ (用化学用语表示);该溶液中各种离子浓度由大到小的顺序为_______ 。
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为_____ 。
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
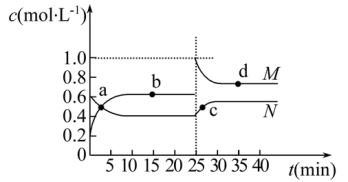
①a、b、c、d四个点中,化学反应处于平衡状态的是点_______ 。
②25min时,增加了_______ (填物质的化学式)_______ mol。
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______ (填字母)。

(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

①a、b、c、d四个点中,化学反应处于平衡状态的是点
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
您最近半年使用:0次
7 . 研究表明不含结晶水的X(由4种短周期元素组成),可作为氧化剂和漂白剂,被广泛应用于蓄电池工业等。为探究X的组成和性质,设计并完成了下列实验:
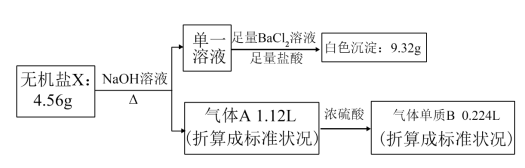
已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:_______ ,X中含有的元素为_______ 。
(2)请写出检验X中阳离子的方法:_______ 。
(3)已知X常用于检验 ,它可将
,它可将 氧化成
氧化成 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。

已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:
(2)请写出检验X中阳离子的方法:
(3)已知X常用于检验
 ,它可将
,它可将 氧化成
氧化成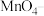 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近半年使用:0次
解题方法
8 . 固体X由4种元素组成的化合物,它是一种重要的催化剂。某学习小组开展了如图实验进行探究:
实验一:
实验二:
已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素___ ,X的化学式____ 。
(2)写出固体X与氢氧化钠溶液反应的化学方程式____ 。
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式____ 。
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是____ 。为了观察溶液A中的水合金属阳离子为浅紫色,可以采取____ 的措施。
实验一:

实验二:

已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素
(2)写出固体X与氢氧化钠溶液反应的化学方程式
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是
您最近半年使用:0次
名校
9 . A、 、
、 、
、 、
、 为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,
为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素, 单质是自然界中密度最小的气体,
单质是自然界中密度最小的气体, 和
和 最外层电子数相同;
最外层电子数相同; 、E和
、E和 在周期表中相邻,且
在周期表中相邻,且 、
、 同主族。B、
同主族。B、 的最外层电子数之和等于
的最外层电子数之和等于 的原子核外电子数,
的原子核外电子数, 和
和 可形成
可形成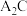 和
和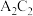 两种常见的液态化合物
两种常见的液态化合物 请回答下列问题:
请回答下列问题:
(1)A元素的名称是_______ , 在周期表中的位置
在周期表中的位置_______  的离子结构示意图
的离子结构示意图_______ 。
(2) 分子的电子式:
分子的电子式:_______ ,A2C2的结构式:_______ 。
(3)用电子式表示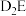 化合物的形成过程为
化合物的形成过程为_______ 。
(4)用含 元素最简单的有机化合物与赤热的氧化铜反应生成一种单质、液态氧化物(10电子微粒)和一可以使澄清石灰水变浑浊的气体,其化学方程式为
元素最简单的有机化合物与赤热的氧化铜反应生成一种单质、液态氧化物(10电子微粒)和一可以使澄清石灰水变浑浊的气体,其化学方程式为_______ 。
(5)在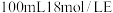 的最高价氧化物对应水化物的溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解
的最高价氧化物对应水化物的溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解 产生的气体在标准状况下的体积可能是
产生的气体在标准状况下的体积可能是_______  填序号
填序号

 、
、 、
、 、
、 为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,
为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素, 单质是自然界中密度最小的气体,
单质是自然界中密度最小的气体, 和
和 最外层电子数相同;
最外层电子数相同; 、E和
、E和 在周期表中相邻,且
在周期表中相邻,且 、
、 同主族。B、
同主族。B、 的最外层电子数之和等于
的最外层电子数之和等于 的原子核外电子数,
的原子核外电子数, 和
和 可形成
可形成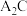 和
和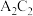 两种常见的液态化合物
两种常见的液态化合物 请回答下列问题:
请回答下列问题:(1)A元素的名称是
 在周期表中的位置
在周期表中的位置 的离子结构示意图
的离子结构示意图(2)
 分子的电子式:
分子的电子式:(3)用电子式表示
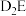 化合物的形成过程为
化合物的形成过程为(4)用含
 元素最简单的有机化合物与赤热的氧化铜反应生成一种单质、液态氧化物(10电子微粒)和一可以使澄清石灰水变浑浊的气体,其化学方程式为
元素最简单的有机化合物与赤热的氧化铜反应生成一种单质、液态氧化物(10电子微粒)和一可以使澄清石灰水变浑浊的气体,其化学方程式为(5)在
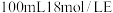 的最高价氧化物对应水化物的溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解
的最高价氧化物对应水化物的溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解 产生的气体在标准状况下的体积可能是
产生的气体在标准状况下的体积可能是 填序号
填序号

您最近半年使用:0次
名校
解题方法
10 . 如图是某元素形成物质的“价—类”图,图中显示各物质之间的转化关系。其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D的大16,回答下列问题:
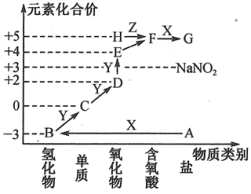
(1)写出下列物质的化学式:C.____ ;H_____ 。
(2)实验室制取B的化学方程式为_____ ,可用____ 试纸检验B是否集满。在B的催化氧化反应中,氧化剂与还原剂的物质的量之比为_____ 。
(3) 都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:
都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:____ 。
(4)写出 溶液与F的稀溶液反应的离子方程式:
溶液与F的稀溶液反应的离子方程式:_____ 。
(5)已知 在空气中会氧化变质(部分转化为G),取部分变质后的固体样品
在空气中会氧化变质(部分转化为G),取部分变质后的固体样品 与
与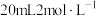 的酸性
的酸性 溶液恰好完全反应(
溶液恰好完全反应( 全部转化为
全部转化为 ),则样品中
),则样品中 的纯度为
的纯度为___ 。

(1)写出下列物质的化学式:C.
(2)实验室制取B的化学方程式为
(3)
 都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:
都是大气污染物,在有催化剂加热的条件下二者可反应生成无污染的物质,写出该反应的化学方程式:(4)写出
 溶液与F的稀溶液反应的离子方程式:
溶液与F的稀溶液反应的离子方程式:(5)已知
 在空气中会氧化变质(部分转化为G),取部分变质后的固体样品
在空气中会氧化变质(部分转化为G),取部分变质后的固体样品 与
与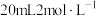 的酸性
的酸性 溶液恰好完全反应(
溶液恰好完全反应( 全部转化为
全部转化为 ),则样品中
),则样品中 的纯度为
的纯度为
您最近半年使用:0次
2022-05-04更新
|
134次组卷
|
2卷引用:辽宁省凌源市三校2021-2022学年高一下学期4月检测化学试题



