名校
1 . 实验室制取HF的原理为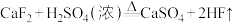 ,氢氟酸可用来刻蚀玻璃,发生反应:
,氢氟酸可用来刻蚀玻璃,发生反应: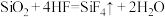 。
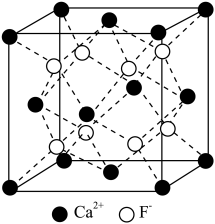
。 的立方晶胞如图所示,其晶胞参数为a pm。下列说法错误的是
的立方晶胞如图所示,其晶胞参数为a pm。下列说法错误的是
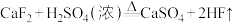 ,氢氟酸可用来刻蚀玻璃,发生反应:
,氢氟酸可用来刻蚀玻璃,发生反应: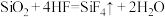 。
。 的立方晶胞如图所示,其晶胞参数为a pm。下列说法错误的是
的立方晶胞如图所示,其晶胞参数为a pm。下列说法错误的是
A.氢化物的稳定性: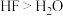 |
B. 、 、 、 、 三者的中心原子价层电子对数相等 三者的中心原子价层电子对数相等 |
C. 的晶体密度为 的晶体密度为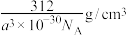 ( ( 为阿伏加德罗常数的值) 为阿伏加德罗常数的值) |
D. 晶体中 晶体中 与 与 之间的最近距离为 之间的最近距离为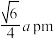 |
您最近半年使用:0次
2023-09-01更新
|
1255次组卷
|
11卷引用:江西省宜春市丰城中学2023-2024学年高二上学期12月月考化学试题
江西省宜春市丰城中学2023-2024学年高二上学期12月月考化学试题湖南省名校大联考2024届高三上学期第一次质量检测化学试题湖南四大名校2024届高三上学期第一次联考化学试题湖南省长沙市长郡中学、衡阳市第八中学2024届高三8月大联考化学试题湖南省炎德英才联考2024届高三上学期第一次质量检测化学试题广西柳州高级中学2023-2024学年高三上学期10月月考化学试题湖南省长沙市湖南师范大学附属中学2023-2024学年高三上学期第一次质量检测化学试题新疆石河子第一中学2023-2024学年高三上学期11月月考化学试题2024届河南省郑州市宇华实验学校高三一模化学试题湖南省衡阳市衡阳县第四中学2023-2024学年高三上学期11月期中化学试题江西省宜春市丰城市第九中学2023-2024学年高三上学期期末考试化学试题
解题方法
2 . 前20号主族元素X、Y、Z、W的原子序数依次增大,它们的原子序数之和等于35,最外层电子数之和为13。分析试剂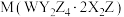 的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知
的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知 时固体的分子式为
时固体的分子式为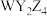 。下列叙述正确的是
。下列叙述正确的是

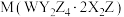 的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知
的相对分子质量为164,常用于稀土金属分离的载体、陶瓷上釉等。M的失重图像如图所示,已知 时固体的分子式为
时固体的分子式为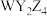 。下列叙述正确的是
。下列叙述正确的是
A.电负性: |
| B.Y的氢化物沸点一定低于Z的氢化物 |
C. 阶段失去1个 阶段失去1个 分子 分子 |
D.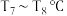 阶段生成的固体为WZ 阶段生成的固体为WZ |
您最近半年使用:0次
2023-06-01更新
|
50次组卷
|
2卷引用:江西省2022-2023学年高二下学期5月统一调研测试化学试题
名校
解题方法
3 . 甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中均含18个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断正确的是
| A.甲通入硫酸铜溶液中无明显现象,但甲能与碱反应 |
| B.乙被称为“绿色氧化剂”,则乙分子空间构型为直线形 |
| C.若丙中含有第二周期IVA族的元素,则丙可能与甲烷中碳氢个数比相同 |
| D.丁的溶液为强酸,用铜做电极电解丁溶液两极都有气体产生 |
您最近半年使用:0次
名校
解题方法
4 . A,B,C,D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型:C,D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号)
(2)单质A有两种同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为_______ ,中心原子的杂化轨道类型为_______ 。
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_______ ;晶胞中A原子的配位数为_______ ;列式计算晶体F的密度(g·cm-3)_______ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为

您最近半年使用:0次
名校
解题方法
5 . 无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在科技发展中发挥着重要的作用。完成下列填空:
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指_______ ,58是指_______ 。
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是_______ ,SiH4的空间构型为_______ 。
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为_______ ,T的电子式为_______ 。
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是_______ (选填编号)
a.SiO + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.
c.SiH4 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑
d.Si+O2 SiO2;C+O2
SiO2;C+O2 CO2
CO2
I.新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。
(1)自然界一共存在四种稳定的铁原子,计算铁元素的近似相对原子质量的计算式为:54×a1%+56×a2%+57×a3%+58×a4%,其中a1%是指
(2)已知铁位于周期表第四周期,与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
II.硅元素是无机非金属材料的主角。
(3)硅在周期表中的位置是
III.Nierite是一种高熔点高硬度的陶瓷材料,摩尔质量为140 g/mol,硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。
(4)Nierite的化学式为
(5)碳化硅(SiC)单晶是目前技术最成熟的第三代半导体材料, 下列能说明碳的非金属性强于硅的反应(或反应组)是
a.SiO
 + 2CO2 + 2H2O = H2SiO3 + 2HCO
+ 2CO2 + 2H2O = H2SiO3 + 2HCO
b.

c.SiH4
 Si+2H2↑;CH4
Si+2H2↑;CH4 C+2H2↑
C+2H2↑d.Si+O2
 SiO2;C+O2
SiO2;C+O2 CO2
CO2
您最近半年使用:0次
名校
解题方法
6 . 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是
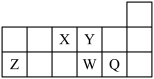

| A.离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| B.元素X与元素Z的最高正化合价之和的数值等于8 |
| C.元素W的最高价氧化物对应的水化物酸性比Q的强X |
D.W元素基态原子最外层电子的电子排布图为 |
您最近半年使用:0次
2022-10-27更新
|
652次组卷
|
4卷引用:河北省石家庄市正中实验中学东校区2022-2023学年高二上学期10月月考化学试题
河北省石家庄市正中实验中学东校区2022-2023学年高二上学期10月月考化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第1章02基础练安徽省合肥市第七中学2022-2023学年高二下学期期中检测化学试题(已下线)第一章 原子结构与性质(A卷)
解题方法
7 . 短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是
A.第一电离能: |
B.简单离子半径: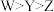 |
C.Z与W形成的化合物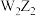 和 和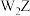 中,阳离子与阴离子个数之比均为2∶1 中,阳离子与阴离子个数之比均为2∶1 |
| D.X、Y、Z形成的化合物中不可能含离子键 |
您最近半年使用:0次
8 . 短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示。其中X、Y、Z三种元素的质子数之和为21。
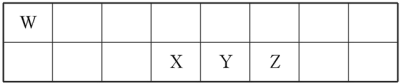
(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是_______ (用化学用语表示);该溶液中各种离子浓度由大到小的顺序为_______ 。
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为_____ 。
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
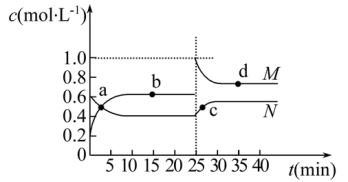
①a、b、c、d四个点中,化学反应处于平衡状态的是点_______ 。
②25min时,增加了_______ (填物质的化学式)_______ mol。
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______ (填字母)。

(1)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是
(2)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
(3)已知:2YZ2(g)⇌Y2Z4(g) ΔH<0。在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

①a、b、c、d四个点中,化学反应处于平衡状态的是点
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
您最近半年使用:0次
9 . 研究表明不含结晶水的X(由4种短周期元素组成),可作为氧化剂和漂白剂,被广泛应用于蓄电池工业等。为探究X的组成和性质,设计并完成了下列实验:
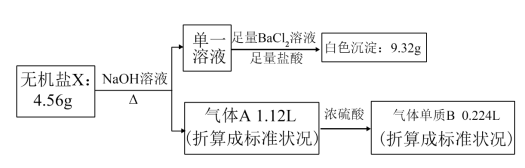
已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:_______ ,X中含有的元素为_______ 。
(2)请写出检验X中阳离子的方法:_______ 。
(3)已知X常用于检验 ,它可将
,它可将 氧化成
氧化成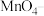 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。

已知:气体单质B可使带火星的木条复燃。
(1)A中所含气体的分子式:
(2)请写出检验X中阳离子的方法:
(3)已知X常用于检验
 ,它可将
,它可将 氧化成
氧化成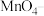 。请写出X溶液和少量
。请写出X溶液和少量 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近半年使用:0次
21-22高一下·河南郑州·期中
名校
解题方法
10 . W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数之和,Z的最外层电子数为K层的一半,W与Y可形成原子个数比为1:1的18e-分子,下列说法正确的是
| A.简单离子半径:Z>X>Y |
| B.W与X也可形成含18e-分子的化合物 |
| C.X和Y的最简单氢化物的沸点:X>Y |
| D.由W、X、Y三种元素所组成化合物的水溶液均显酸性 |
您最近半年使用:0次
2022-05-29更新
|
279次组卷
|
3卷引用:第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)
(已下线)第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)河南省郑州市十校2021-2022学年高一下学期期中联考化学试题云南省昆明市第三中学2021-2022学年高一下学期期中考试化学试题



