解题方法
1 . 某实验小组以含铁污泥(主要成分为 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
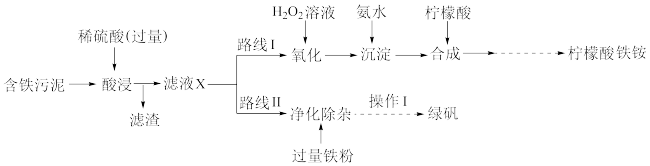
根据所学知识,回答下列问题:
(1) 有多种同位素,其中
有多种同位素,其中 核素中中子数与质子数之差为
核素中中子数与质子数之差为_______ 。
(2)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:_______ 。
(3)“滤液X”中一定含有的阳离子为_______ 。
(4)路线Ⅰ中,加入 溶液的目的是
溶液的目的是_______ 。
(5)写出加入氨水“沉淀”时的离子方程式:_______ 。
(6)写出加入过量铁粉时发生反应的离子方程式:_______ 。
(7)“酸浸”时加入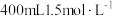 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为_______ g。
 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)
 有多种同位素,其中
有多种同位素,其中 核素中中子数与质子数之差为
核素中中子数与质子数之差为(2)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(3)“滤液X”中一定含有的阳离子为
(4)路线Ⅰ中,加入
 溶液的目的是
溶液的目的是(5)写出加入氨水“沉淀”时的离子方程式:
(6)写出加入过量铁粉时发生反应的离子方程式:
(7)“酸浸”时加入
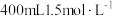 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近半年使用:0次
解题方法
2 . 研究生命现象的化学机理对促进人类健康的重要作用
(1)___________ 为现代分子生物学的建立奠定了基础。
(2)探寻人类和生物的生命运动的化学机理是21世纪化学科学亟待解决的重大课题之一、研究___________ 和___________ 相互作用的机理,人们就能进行药物设计,有助于合成高效无毒副作用的药物;合成具有___________ 的分子,可以帮助人类揭示生命的奥秘;了解___________ 和___________ ,创造“新陈代谢”的目标能得以实现。
(1)
(2)探寻人类和生物的生命运动的化学机理是21世纪化学科学亟待解决的重大课题之一、研究
您最近半年使用:0次
名校
解题方法
3 . 硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起了广泛关注。
(1)Se与S是相邻周期的同主族元素,则Se在元素周期表中的位置为___________ ,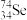 和
和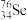 这两种原子的中子数之差的绝对值为
这两种原子的中子数之差的绝对值为___________ 。
(2)H2Se是一种有恶臭的气体,与H2O相比,沸点:H2Se___________ H2O(填“>”或“<”,下同),热稳定性:H2Se___________ H2O。
(3)较高浓度的Na2SeO3能促进细胞DNA的增殖活性,延缓细胞衰老,但无机硒的毒性逐渐成为限制它使用的一个非常重要的因素。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ (填离子符号)。
(4)一种合成含Se的新型AIE分子的原料结构如图:
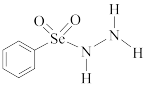
肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为___________ 。
(1)Se与S是相邻周期的同主族元素,则Se在元素周期表中的位置为
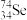 和
和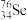 这两种原子的中子数之差的绝对值为
这两种原子的中子数之差的绝对值为(2)H2Se是一种有恶臭的气体,与H2O相比,沸点:H2Se
(3)较高浓度的Na2SeO3能促进细胞DNA的增殖活性,延缓细胞衰老,但无机硒的毒性逐渐成为限制它使用的一个非常重要的因素。Na、Se、O形成的简单离子的半径由大到小的顺序为
(4)一种合成含Se的新型AIE分子的原料结构如图:

肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为
您最近半年使用:0次
解题方法
4 . 硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料,生物医学等领域引起广泛关注。
(1)Se在元素周期表中的位置为______ ,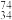 Se和
Se和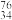 Se互为
Se互为______ ,这两种原子中子数之差的绝对值为_______ 。
(2)H2Se是一种有恶臭的气体,与H2O相比,沸点H2Se_______ H2O(填“>”或“<”,下同),原因是______ ;热稳定性:H2Se_______ H2O。
(3)较高浓度的Na2SeO2能促进细胞DNA的增殖活性,延缓细胞衰老。Na、Se、O形成的简单离子的半径由大到小的顺序为______ (填离子符号)。
(4)一种合成含Se的新型AIE分子的原料结构如图:
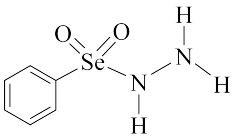
肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为_______ 。
(1)Se在元素周期表中的位置为
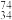 Se和
Se和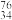 Se互为
Se互为(2)H2Se是一种有恶臭的气体,与H2O相比,沸点H2Se
(3)较高浓度的Na2SeO2能促进细胞DNA的增殖活性,延缓细胞衰老。Na、Se、O形成的简单离子的半径由大到小的顺序为
(4)一种合成含Se的新型AIE分子的原料结构如图:

肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为
您最近半年使用:0次
名校
5 . 填空:
(1)有下列微粒或物质:① O、
O、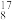 O、
O、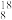 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥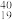 K、
K、 Ca、
Ca、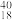 Ar,回答下列问题:
Ar,回答下列问题:
a.互为同位素的是_______ ;
b.互为同素异形体的是_______ ;
c.上述微粒中出现的核素符号有_______ 种;
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为_______ 种,相对分子质量最大的是_______ (写化学式)。
(2)相同质量的 H2
H2 O与
O与 H2
H2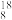 O所含中子数之比为
O所含中子数之比为_______ 。
(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为_______ 。
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。
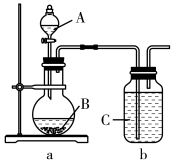
甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:_______ 。
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由_______ ,并提出改进实验方案_______ 。
(1)有下列微粒或物质:①
 O、
O、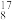 O、
O、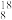 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥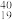 K、
K、 Ca、
Ca、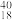 Ar,回答下列问题:
Ar,回答下列问题:a.互为同位素的是
b.互为同素异形体的是
c.上述微粒中出现的核素符号有
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为
(2)相同质量的
 H2
H2 O与
O与 H2
H2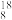 O所含中子数之比为
O所含中子数之比为(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。

甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由
您最近半年使用:0次
名校
6 . 次氯酸可以和丙烯发生加成反应CH3CH=CH2+HClO→CH3CH(OH)CH2Cl,以CH3CH(OH)CH2Cl为原料可以合成CH3CH(OH)COOH,进一步合成新型降解材料聚乳酸。下列化学用语表示正确的是
A.原子核内有8个中子的碳原子: | B.丙烯分子的球棍模型: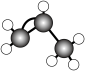 |
C.次氯酸的电子式: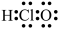 | D.聚乳酸的结构简式: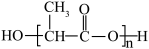 |
您最近半年使用:0次



