名校
1 . 反应 可用于冶金。设
可用于冶金。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 可用于冶金。设
可用于冶金。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.2.0g 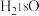 与 与 的混合物中所含质子数与中子数均为 的混合物中所含质子数与中子数均为 |
B.100mL 1 NaCN溶液中阴离子数为0.1 NaCN溶液中阴离子数为0.1 |
C.1mol 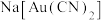 中含 中含 键数目为6 键数目为6 |
D.该反应消耗22.4L  ,转移电子数为4 ,转移电子数为4 |
您最近半年使用:0次
名校
2 . 卢瑟福发现质子的核反应为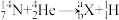 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为 。下列说法错误的是
。下列说法错误的是
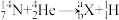 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为 。下列说法错误的是
。下列说法错误的是| A.Y元素的第一电离能高于同周期相邻元素 |
| B.元素的电负性:X>Y>H |
| C.X和Z的简单氢化物中中心原子的价层电子对数目相同 |
| D.ZX2的空间结构为直线形 |
您最近半年使用:0次
名校
3 .  分子与
分子与 结合形成配离子
结合形成配离子 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 分子与
分子与 结合形成配离子
结合形成配离子 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,3.4g 中所含的电子总数为 中所含的电子总数为 |
B.1mol 中σ键的数目为 中σ键的数目为 |
C.0.1mol 中,中心离子的配位数的数目为 中,中心离子的配位数的数目为 |
D.0.2mol 中所含的中子数为 中所含的中子数为 |
您最近半年使用:0次
2024-04-02更新
|
84次组卷
|
2卷引用:河北省保定市清苑中学等校2023-2024学年高二下学期3月月考化学试题
名校
4 . 钼( )在合金中有着重要的应用。下列说法正确的是
)在合金中有着重要的应用。下列说法正确的是
| A.钼及其化合物均为金属材料 |
B.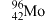 的中子数为42 的中子数为42 |
C. 与非金属单质反应时可能作氧化剂也可能作还原剂 与非金属单质反应时可能作氧化剂也可能作还原剂 |
D.向钢中添加适量 可提高钢的高温强度 可提高钢的高温强度 |
您最近半年使用:0次
名校
解题方法
5 . 中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,并被采用为国际新标准。铟与铷(37Rb)同周期,下列说法错误的是
| A.In是第五周期第ⅢA族元素 | B.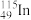 的中子数与电子数的差值为66 的中子数与电子数的差值为66 |
C.原子半径: | D.碱性: |
您最近半年使用:0次
名校
解题方法
6 . 下列有关化学用语描述不正确的是
A. 在水溶液中电离方程式为 在水溶液中电离方程式为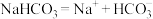 |
B. 的中子数为8 的中子数为8 |
C.Cl原子的结构示意图为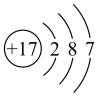 |
D.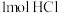 含有 含有 数为 数为 |
您最近半年使用:0次
解题方法
7 . 许多元素有多种核素,而且各种核素在自然界中所占的比例相对固定,其中氢元素有 、
、 、
、 三种核素,钛元素有
三种核素,钛元素有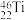 、
、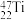 、
、 、
、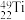 、
、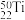 五种核素,有关核素的说法错误的是
五种核素,有关核素的说法错误的是
 、
、 、
、 三种核素,钛元素有
三种核素,钛元素有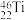 、
、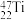 、
、 、
、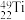 、
、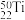 五种核素,有关核素的说法错误的是
五种核素,有关核素的说法错误的是A. 、 、 、 、 三种核素与 三种核素与 最多可以形成6种不同的水分子 最多可以形成6种不同的水分子 |
B.放射性的氡(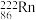 )内中子数与质子数之差为136 )内中子数与质子数之差为136 |
C.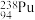 与 与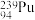 具有相同的最外层电子数 具有相同的最外层电子数 |
| D.钛元素的相对原子质量介于46~50之间 |
您最近半年使用:0次
名校
8 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的元素周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构。性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
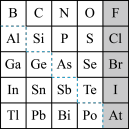
(1) 的结构示意图是
的结构示意图是___________ 。
(2)元素In在元素周期表中的位置是___________ 。
(3)P的最高价氧化物的化学式为___________ ,Al元素的最高价氧化物对应的水化物与S元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(4) 的中子数与电子数的差值是
的中子数与电子数的差值是___________ ;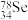 和
和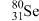 的物理性质
的物理性质___________ (填“相同”或“不同”),化学性质___________ (填“相同”或“不同”)。
(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是___________ 。
A.
B.
C.
②氢化物的还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)
 的结构示意图是
的结构示意图是(2)元素In在元素周期表中的位置是
(3)P的最高价氧化物的化学式为
(4)
 的中子数与电子数的差值是
的中子数与电子数的差值是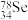 和
和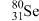 的物理性质
的物理性质(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是
A.

B.

C.

②氢化物的还原性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近半年使用:0次
名校
解题方法
9 . “十五”时期,碲化镉(Cde)薄膜电池研究被列入国家高技术研究发展计划(863计划)重点项目。碲化镉太阳能电池较单晶硅太阳能电池有制作方便、成本低廉和重量较轻等优点。下列说法错误的是
A.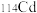 和 和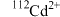 的核外电子数之差为2 的核外电子数之差为2 |
B.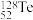 的中子数比质子数多24个 的中子数比质子数多24个 |
C.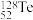 和 和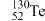 互为同素异形体 互为同素异形体 |
| D.硅位于元素周期表中金属元素区与非金属元素区的分界线处,常用作半导体材料 |
您最近半年使用:0次
2024-02-28更新
|
196次组卷
|
3卷引用:河北省衡水中学2023-2024学年高一下学期2月开学检测化学试题
名校
10 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 的浓硫酸中所含氧原子数目为 的浓硫酸中所含氧原子数目为 |
B.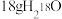 含有的中子数为 含有的中子数为 |
C.常温常压下,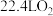 所含氧原子数为 所含氧原子数为 |
D. 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近半年使用:0次



