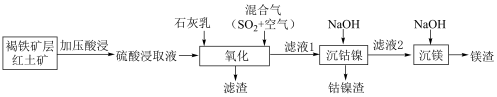
16. 镍、钴、镁的氢氧化物在化工生产中有着重要的应用。某褐铁矿层红土矿(其含有金属元素Fe,Ni、Mg,Mn和少量Co)。某工厂以此为原料,制备镍、钴、镁的氢氧化物等产品的工艺流程如下:
已知:①常温下,相关金属离子形成氢氧化物沉淀的pH范围如下表:
| 金属离子 | Fe3+ | Co2+ | Ni2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 7.15 | 7.2 | 9.6 |
| 完全沉淀的pH | 3.7 | 9.15 | 9.2 | 11.1 |
②Co(OH)
2在空气中可被氧化成CoO(OH)。
③“氧化”过程中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H
2SO
5),过一硫酸(H
2SO
5)溶液中含硫微粒有
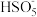
、
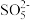
。
回答下列问题:
(1)“加压酸浸”过程中,为增大褐铁矿层红土矿在硫酸中的浸出速率,可采取的措施为
___________。
(2)根据化合价判断lmolH
2SO
5中含有O—O的数目为
___________;用石灰乳调节pH=4,Mn
2+被H
2SO
5氧化为MnO
2,该反应的离子方程式为
___________。
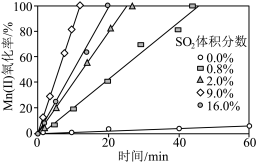
(3)“氧化”过程中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下图所示。SO
2体积分数为
___________时,Mn(Ⅱ)氧化速率最大;继续增大SO
2体积分数时,Mn(Ⅱ)氧化速率减小的原因是
___________。
(4)“沉钴镍”过程中加入NaOH溶液,调节pH的范围是
___________,得到的Co(Ⅱ)在空气中被氧化成Co(Ⅲ)的化学方程式为
___________。
(5)钴镍渣中钴含量的测定:处理钴镍渣使Co(Ⅱ)完全被氧化成Co(Ⅲ),在稀硫酸中加入0.1000g处理后的样品,待样品完全溶解后加入足量KI固体。充分反应后,调节溶液pH为3~4,以淀粉作指示剂,用0.01000mol·L
-1Na
2S
2O
3标准液滴定至终点,消耗标准溶液25.00mL(已知:2Co
3++2I
-=2Co
2++I
2;I
2+2

=2I
-+

)。样品中含Co(Ⅲ)元素的质量分数为
___________。